Способ получения иммуностимулятора пептидной природы (варианты) и бад на его основе
Иллюстрации
Показать всеИзобретение относится к области пищевой и медицинской промышленности и может быть использовано для получения иммуностимулятора пептидной природы из нервной ткани морских гидробионтов. Для этого проводят размораживание, измельчение сырья, экстрагирование его 3%-ным раствором уксусной кислоты, получение и отделение надосадочной жидкости, выделение конечного продукта. При этом сырье экстрагируют в течение 35-48 ч при перемешивании в течение 15 мин через каждые 1,5 часа, затем подщелачивают раствором бикарбоната натрия до рН=8,0-8,5, добавляют 0,3% раствор хитозана в 3% уксусной кислоте, выдерживают в течение одного часа, полученную массу центрифугируют на центрифуге 5000 об/мин в течение 20 мин, к надосадочной жидкости добавляют сульфат аммония до 30% концентрации раствора, выдерживают при помешивании в течение двух часов, снова центрифугируют на центрифуге 5000 об/мин в течение 20 мин, надосадочную жидкость диафильтруют на кассетной мембране с пределом разделения 1000 Да четырежды с добавлением к получаемому концентрату дистиллированной воды в соотношении концентрат : вода 1:2 до получения раствора с конечным веществом от 1000 до 15000 Да. Также предложена биологически активная добавка. Группа изобретений обеспечивает получение иммуностимулятора пептидной природы с повышенной биологической активностью за счет увеличения содержания в нем пептидов, обладающих иммуностимулирующим действием. 3 н. и 4 з.п. ф-лы, 2 табл., 6 пр.
Реферат
Изобретение относится к области пищевой и медицинской промышленности, а именно к способу получения иммуностимулятора из нервной ткани морских гидробионтов. Полученный предлагаемыми способами препарат может применяться, как биологически активная добавка, и предназначен для приема внутрь (перорально).
Известен способ получения иммуностимулятора из молок лососевых рыб (патент РФ 2091073, A61K 35/60), представляющий собой замораживание сырья, измельчение, экстрагирование 3%-ным раствором уксусной кислоты с добавлением хлористого цинка, центрифугирование, ультра- и диафильтрацию экстракта в растворе 0,9% хлорида натрия с pH 6,0-6,5 через пористый материал с пределом разделения 5000 Да, стерилизацию и лиофильное высушивание.
Известен способ получения иммуностимулятора из ганглий кальмара и каракатицы (патент РФ 2091072, A61K 35/60), включающий гомогенизацию сырья в воде, подкисленной уксусной кислотой до pH 3,5-4,5 и содержащей 0,1% хлористого цинка, отделение надосадочной жидкости, стерилизующую фильтрацию через мембранные фильтры с размером пор 0,8; 0,45; 0,22 мкм, концентрирование стерильного фильтрата в 5,5 раз на ультрафильтрационной установке через пористый материал с пределом разделения 1000-5000 Да с последующей очисткой в подщелоченной до pH 9-10 воде, повторное концентрирование на том же пористом материале и стерилизацию, лиофильное высушивание.
Недостатками этих способов являются:
- применение дорогостоящего ультрафильтрационного оборудования;
- отсутствие технологической операции по отделению веществ с молекулярной массой более 10000-15000 Да, что приводит к присутствию в препарате высокомолекулярных примесей, снижающих активность препарата и проявляющих аллергический эффект.
Известен способ получения иммуностимулирующего препарата из тимуса (патент РФ 1112606, A61K 38/22), заключающийся в очистке сырья, замораживании, измельчении сырья, экстракции 5-6 объемами 3%-ного раствора уксусной кислоты, содержащей хлористый цинк при соотношении хлористого цинка и уксусной кислоты 1:1000 в течение 48-72 ч, отделении надосадочной жидкости и выделении целевого продукта осаждением пятью объемами ацетона при t=(-3)-(-5)°С, экстракции полученного осадка водой при рН 6-7 и комнатной температуре в течение 1-3 ч.
Известен способ получения иммуностимулятора для повышения функции миндалин (патент РФ 1522485, A61K 35/30), включающий очистку сырья, замораживание, измельчение, экстракцию в 20-25 объемах 3%-ным раствором уксусной кислоты с добавлением хлористого цинка, фильтрование, обработку надосадочной жидкости ацетоном, отделение осадка, растворение и лиофилизацию целевого продукта, в качестве сырья используют миндалины человека.
Известен способ получения иммуностимулирующего вещества (авторское свидетельство СССР №1103392), заключающийся в том, что ганглии кальмара или каракатицы (нервную ткань) промывают водой и ацетоном, затем помещают в ацетон и выдерживают в ацетоне при температуре 4-10°С, гомогенизируют в воде, содержащей 0,1%-ного раствора хлористого цинка, подкисляют до рН 3,5-4,5 и выдерживают 24-48 ч, затем отделяют надосадочную жидкость, которую обрабатывают ацетоном при соотношении надосадочной жидкости и ацетона 1:6 по объему, при температуре 3-5°С, отделяют осадок, высушивают его, растворяют в воде с рН 6,0-7,0 и фильтруют.
Недостатками этих способов являются использование больших объемов дорогостоящего огнеопасного реактива (ацетона), неполное удаление высокомолекулярных белков и введение дополнительной стадии растворения осадка целевого продукта перед его высушиванием, что приводит к снижению выхода.
Наиболее близким по технической сущности к заявленному способу является способ получения иммуностимулятора из нервной ткани морских гидробионтов (патент РФ 2222337, A61K 35/30, A61K 35/60, A23L 1/333), включающий разморозку замороженного сырья (нервную ткань головоногих моллюсков: кальмаров, каракатиц, осьминогов; мозг морских млекопитающих: белух, кашалотов, китов, моржей, ларги, нерпы, лахтака, акибы; мозг рыб: лососевых, осетровых, сельдевых, тресковых, камбаловых, окуневых), измельчение, экстрагирование 3%-ным раствором уксусной кислоты с добавлением хлористого цинка, центрифугирование, отделение надосадочной жидкости и выделение целевого продукта путем ультрафильтрации и диафильтрации, которые проводят в две стадии на двух мембранах с различным пределом разделения по молекулярной массе. Иммуностимулятор, полученный по предлагаемому способу, имеет четко ограниченные пределы молекулярной массы 1000 - 10000-15000 Да.
Недостатками прототипа - способа являются:
- использование дорогостоящего ультрафильтрационного оборудования;
- отсутствие стадии обезжиривания экстракта и как следствие - конечного продукта, что приводит к снижению срока хранения препарата из-за окисления липидов;
Известно, что ткани мозга различных животных содержат от 5 (серое вещество) до 17 (белое вещество) процентов липидов, часть которых представлены конъюгатами с белками и пептидами и могут легко попасть в концентрат раствора конечного продукта, полученный путем ступенчатой ультрафильтрации.
Аналоги и прототип по БАД.
Известно иммуномодулирующее средство Риботаб (патент РФ 2257216, A61K 35/12, A61K 35/55), имеющее в своем составе препарат полипептидной природы, полученный из тимуса животных (тактивин, или тималин, или тимоген) - 0,15-0,3 мас. %, нуклеинат натрия - 6,0-8,0 мас. %, а также крахмал картофельный, молочный сахар, тальк, желатин, поливинилпирролидон и стеариновую кислоту.
Известен лечебно-профилактический продукт для людей и животных с иммуностимулирующим действием (патент РФ 2065707, A23L 1/305, A23L 1/325), содержащий мясо теплокровных животных, рыб, беспозвоночных и/или отходы их переработки - 99,99965-99,99950 мас. %, иммуностимуляторы пептидной природы, преимущественно ганглиин, тималин, тимоген, Т-активин, вилозен, - 0,00035-0,0005 мас. %.
Недостатком данных патентов является использование в качестве сырья тканей сельскохозяйственных животных без термической обработки, что является риском распространения вирусных заболеваний и бешенства прионовой природы.
Известна иммуностимулирующая композиция (патент РФ №2110254, A61K 9/14, A61K 45/06), включающая препараты в следующем соотношении, мг: иммунокорректор (ганглиин или молокин или гепалин) - 0,5-6, парацетамол 200-500, витамин С - 50-100, антигистаминное средство - 0,5-25, глюкозу - 300-500.
Наиболее близким техническим решением для продукта является пищевая биологически активная добавка «Тинростим-С» (патент РФ 2105504, A23L 1/305, A23L 1/29, A61K 38/17), содержащая в качестве пептидов ганглиин 0,2-0,4%, полученный из нервной ткани кальмара или каракатицы, аскорбиновую кислоту - 9-11%, остальное - глюкоза.
Недостатком прототипа - продукта является ограниченная сырьевая база, небольшое содержание пептидов.
Основной задачей, на решение которой направлены заявляемые способ получения иммуностимулятора пептидной природы (варианты) и БАД на его основе, является увеличение выхода конечного продукта, удешевление и упрощение способа его получения, повышение биологической активности добавок, содержащих конечный продукт.
Единый технический результат, достигаемый при осуществлении заявляемой группы изобретений, состоит в получении БАД с повышенной биологической активностью за счет увеличения содержания в ней пептидов, обладающих иммуностимулирующим действием.
Вариант 1. Указанный технический результат достигается тем, что в известном способе получения иммуностимулятора пептидной природы из нервной ткани морских гидробионтов, включающем размораживание сырья, его измельчение, экстрагирование в 3% уксусной кислоте, получение и отделение надосадочной жидкости, выделение конечного продукта, согласно изобретению, сырье экстрагируют в течение 35-48 ч при перемешивании в течение 15 мин через каждые 1,5 ч, затем смесь подщелачивают бикарбонатом натрия до pH=8,0-8,5, добавляют 0,3% раствор хитозана в 3% растворе уксусной кислоты и выдерживают в течение одного часа, полученную массу центрифугируют на центрифуге 5000 об/мин в течение 20 мин, к полученной надосадочной жидкости добавляют сульфат аммония до 30% концентрации раствора, смесь выдерживают при помешивании в течение двух часов, снова центрифугируют на центрифуге 5000 об/мин в течение 20 мин, надосадочную жидкость диафильтруют на кассетной мембране с пределом разделения 1000 Да, при этом диафильтрацию осуществляют четырежды с добавлением к получаемому концентрату дистиллированной воды в соотношении концентрат : вода 1:2 до получения раствора с конечным веществом от 1000 до 15000 Да, концентрат подвергают лиофильной сушке с последующим ультрафиолетовым облучением и стерильно упаковывают.
В качестве сырья используют замороженную нервную ткань морских гидробионтов, а именно: головоногих моллюсков - кальмаров, каракатиц, осьминогов; мозг морских млекопитающих - белух, кашалотов, китов, моржей, ларги, нерпы, лахтака, акибы; мозг рыб - лососевых, осетровых, сельдевых, тресковых, камбаловых, окуневых.
Обработка экстракта раствором хитозана до стадии отделения осадка измельченной ткани позволяет удалить липидные примеси и тем самым обеспечить надлежащую хранимоспособность конечного продукта.
Добавление сульфата аммония способствует удалению высокомолекулярных белков из надосадочной жидкости. Ограничение высокомолекулярных веществ в препарате необходимо не только для получения продукта с наибольшей активностью, но и для обеспечения антиаллергического эффекта.
Применяемый сульфат аммония является веществом нетоксичным, безопасным в пожарном отношении и недорогим.
Этот способ позволяет сконцентрировать раствор целевого продукта (низкомолекулярных пептидов) до небольшого объема, что облегчает последующую сушку. Очищенный концентрат содержит низкомолекулярные пептиды с молекулярной массой от 1000 до 10000-15000 Да. При применении данного способа получения препарата отделяются все балластные вещества с молекулярной массой более 10000-15000 Да, а при диафильтрации - все примеси менее 1000 Да. Выход иммуностимулятора, полученного этим способом, составляет 85-110 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала(95%), остальное - неорганические соли.
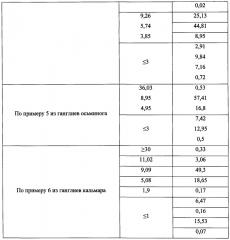
Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Как следует из представленных данных, все препараты, полученные по заявленному способу, содержат следовые количества пептидного материала с молекулярной массой более 10 кДа, либо не содержат его совсем.
Сущность изобретения состоит в том, что иммуностимулятор получают следующим образом: сырье размораживают на воздухе до температуры минус 4°С, измельчают на электромясорубке с диаметром пропускающих отверстий 2-3 мм. Измельченное сырье помещают в емкость, заливают 3% уксусной кислотой и экстрагируют в течение 35-48 ч при перемешивании в течение 15 мин через каждые 1,5 ч, затем смесь подщелачивают бикарбонатом натрия до рН=8,0-8,5, добавляют 0,3% раствор хитозана в 3% уксусной кислоте (одна часть раствора хитозана на 20 частей экстракта по объему) и выдерживают в течение одного часа. Полученную массу центрифугируют на центрифуге 5000 об/мин в течение 20 мин, к полученной надосадочной жидкости добавляют сульфат аммония до 30% концентрации раствора, смесь выдерживают при помешивании в течение двух часов, снова центрифугируют на центрифуге 5000 об/мин в течение 20 мин, надосадочную жидкость диафильтруют на кассетной мембране (установка Pellicon фирмы Millipore, Франция или Т66.00.00.000ПС Научно-производственная фирма «Гелла-ТЭКО», РФ, г. Москва) с пределом разделения 1000 Да, при этом диафильтрацию осуществляют четырежды с добавлением к получаемому концентрату дистиллированной воды в соотношении концентрат : вода 1:2 до получения раствора с конечным веществом от 1000 до 15000 Да. Далее концентрат подвергают лиофильной сушке, а затем стерилизуют ультрафиолетом в течение 15 мин и стерильно упаковывают.
Примеры осуществления способа по данному варианту приведены в примерах конкретного выполнения №1, 2.
Вариант 2. Указанный технический результат достигается тем, что в известном способе получения иммуностимулятора пептидной природы из нервной ткани морских гидробионтов, включающем размораживание сырья, его измельчение, экстрагирование в 3% уксусной кислоте, получение и отделение надосадочной жидкости, выделение конечного продукта, согласно изобретению, сырье экстрагируют в течение 35-48 ч при перемешивании в течение 15 мин через каждые 1,5 ч, затем смесь подщелачивают бикарбонатом натрия до рН=8,0-8,5, добавляют 0,3% раствор хитозана в 3% растворе уксусной кислоты и выдерживают в течение одного часа, добавляют неорганический адсорбент природного происхождения, периодически перемешивая в течение 20 мин, затем отстаивают смесь в течение 4 часов, надосадочную жидкость декантируют и высушивают на вакуумной ротационной или распылительной сушках, в условиях исключающих нагрев выше 30-40°C, сухой продукт облучают ультрафиолетовой лампой и стерильно упаковывают.
В качестве сырья используют замороженную нервную ткань морских гидробионтов, а именно: головоногих моллюсков - кальмаров, каракатиц, осьминогов; мозг морских млекопитающих - белух, кашалотов, китов, моржей, ларги, нерпы, лахтака, акибы; мозг рыб - лососевых, осетровых, сельдевых, тресковых, камбаловых, окуневых.
Добавление адсорбента в экстракт сразу после раствора хитозана до стадии отделения осадка измельченной ткани обеспечивает удаление высокомолекулярных белков.
В качестве адсорбентов используют сухой фильтроперлит (ГОСТ 30566-98, разрешен к использованию для очистки пищевых продуктов) или 20% суспензию бентонита (ОСТ 18-49-71, для винодельческой промышленности, пищевая добавка Е 558), либо любой пищевой сорбент, адсорбирующий высокомолекулярные белковые фракции.
Надосадочную жидкость декантируют без использования центрифугирования или сепарирования, так как используемые адсорбенты хорошо осветляют раствор, не оставляя в нем мелкодисперсных взвесей. Выход иммуностимулятора, полученного данным способом, составляет 45-100 г.
После высушивания в вышеуказанных условиях конечный препарат представляет собой аморфный порошок белого цвета, состоящий из пептидного материала (95%), остальное - неорганические соли. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Сущность изобретения состоит в том, что иммуностимулятор получают следующим образом: сырье размораживают на воздухе до температуры минус 4°C, измельчают на электромясорубке с диаметром пропускающих отверстий 2-3 мм. Измельченное сырье помещают в емкость, заливают 3% уксусной кислотой и экстрагируют в течение 40 ч при перемешивании в течение 15 мин через каждые 1,5 ч, затем смесь подщелачивают бикарбонатом натрия до рН=8,0-8,5, добавляют 0,3% раствор хитозана в 3% уксусной кислоте (одна часть раствора хитозана на 20 частей экстракта по объему) и выдерживают в течение одного часа. В смесь добавляют неорганический адсорбент природного происхождения в количестве, зависящем от начального объема экстракта, периодически перемешивая в течение 20 мин, затем отстаивают смесь в течение 4 часов. Надосадочную жидкость декантируют и высушивают на вакуумной ротационной или распылительной сушках, в условиях исключающих нагрев выше 30-40°C, сухой продукт облучают ультрафиолетовой лампой и стерильно упаковывают.
Примеры осуществления способа по данному варианту приведены в примерах конкретного выполнения №3, 4, 5, 6.
Преимущества вышеуказанных способов по сравнению с прототипом:
1. Применяется раствор хитозана, позволяющий очистить экстракт от липидных примесей;
2. Для удаления высокомолекулярных белков используют:
а) высаливание надосадочной жидкости сульфатом аммония после отделения осадка исходного измельченного сырья с последующей диафильтрацией через мембрану с порогом удерживания 1000 Да (вариант 1):
б) обработку экстракта неорганическими адсорбентами природного происхождения с последующим декантированием надосадочной жидкости (вариант 2).
3. Технологии не требуют многоступенчатой ультрафильтрации и стерилизующей фильтрации;
4. В варианте 2 не используются центрифуги или сепараторы, что значительно упрощает и удешевляет способ получения иммуностимулятора;
5. Способы исключают добавление хлористого цинка.
6. Получают иммуностимулятор с высокой биологической активностью.
Первый вариант заявляемого способа более длительный, чем второй, но позволяет получить высокий выход конечного продукта, в то время как второй вариант более дешевый и упрощенный с выходом конечного продукта ниже, чем первый вариант.
Указанный технический результат достигается тем, что предлагаемыми вариантами способа получают иммуностимулятор пептидной природы, входящий в состав биологически активной добавки, имеющей две формы выпуска: порошок и таблетки, и содержащей следующие компоненты:
Форма выпуска - порошок (в 1 порошке, %)
Пептиды - 0,1-0,5,
Аскорбиновая кислота - 8-16,
D-глюкоза или
кристаллическая глюкоза - остальное.
Форма выпуска - таблетки (в 1 таблетке, мг)
Пептиды - 1,0-1,5,
Аскорбиновая кислота - 8-10,
D-глюкоза или
кристаллическая глюкоза - 118-125,
Целлюлоза микрокристаллическая или крахмал картофельный - 68,8,
Кальция стеарат - 2,0.
Повышенная биологическая ценность пептида доказана проведением иммунологических исследований иммуностимулятора, сырьем для которого явились оптические ганглии кальмара, полученного по одному из вариантов заявляемых способов. В исследование включали добровольцев из числа студентов 2-го курса ШБМ ДВФУ в возрасте 19-22 лет, не имеющих в анамнезе указаний на гиперчувствительность или аллергические реакции на компоненты препарата, хронические заболевания (сахарный диабет, туберкулез, хронические заболевания печени и почек, онкологические заболевания, ВИЧ, др.), беременность, а также не страдающих острыми инфекционными заболеваниями на момент исследования. Кроме того, в исследование не включали людей, принимавших иммуномодулирующие препараты в течение 4 недель до начала исследования. Проведение исследования было одобрено биоэтическим комитетом ШБМ ДВФУ.
При испытаниях использовались препараты в форме порошка и таблеток.
Добровольцы принимали препараты по одной дозе, содержащей 2 мг иммуностимулятора, в сутки в утренние часы до еды в течение 1 месяца.
Иммунофенотипирование лимфоцитов крови проводили на проточном цитофлуориметре Beckman Coulter Epics XL в соответствии со стандартизированной технологией (Хайдуков СВ., Байдун Л.А., Зурочка А.В., Тотолян Арег А. Исследование субпопуляционного состава лимфоцитов периферической крови с применением проточных цитофлуориметров-анализаторов // Медицинская иммунология.- 2012.- Т. 14.-№3. - С. 255-268). Для оценки функциональной активности фагоцитирующих клеток крови у добровольцев на фоне применения препаратов использована реакция восстановления нитросинего тетразолия (НСТ-тест) (Виксман М.Е., Маянский А.Н. Способ оценки функциональной активности нейтрофилов человека по реакции восстановления нитросинего тетразолия: Методические рекомендации - Казань: КазанскийНИИЭМ. - 2011. - 11 с). Для определения фагоцитарной активности нейтрофилов использовали Staphilococcus aureus с подсчетом фагоцитарного индекса (процентное содержание фагоцитирующих нейтрофилов) - ФИ и фагоцитарного числа (среднее число микроорганизмов, поглощенных одним нейтрофилом) - ФЧ.
Применение препаратов оказало положительное влияние на количественный и качественный состав периферической крови у лиц на фоне стандартного курса приема препаратов с увеличением абсолютного количества лейкоцитов на 10,8-17,3%, лимфоцитов на 18,8%.
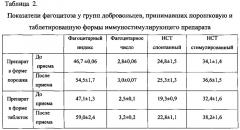
Была установлена способность препаратов стимулировать функциональную активность и поглотительную способность фагоцитирующих клеток крови добровольцев с увеличением фагоцитарного индекса на 16,7-25,3%, фагоцитарного числа на 7,14-28,0%, стимулированного НСТ-теста на 7,3-17,9% (Таблица 2).
При динамическом наблюдении субпопуляционного состава лимфоцитов периферической крови у добровольцев после приема препаратов было выявлено достоверное увеличение количества CD3+, CD4+, CD3+HLA-DR+ клеток. Положительная динамика свидетельствует об иммуностимулирующем влиянии препаратов, как в форме порошка, так и в форме таблеток.
Приведенные данные свидетельствуют о том, что употребление обоих форм препаратов приводит к достоверному увеличению фагоцитарного индекса на 17-25%, фагоцитарного числа на 7-28%, стимулированного НСТ-теста на 7-18%.
Известная БАД «Тинростим-С», выпускаемая также в порошках, имеет в своем составе небольшое количество пептидов, за счет чего снижается ее биологическая ценность.
При сравнительном анализе результатов исследований БАД, полученного по способу-прототипу, было установлено, что включение препарата в комплексную терапию обеспечивает увеличение фагоцитарного индекса на 1-10% (Н.Н. Беседнова, Л.М. Эпштейн «Биологически активная добавка к пище ТИНРОСТИМ» (в помощь практикующему врачу), Владивосток: ТИНРО-Центр, 2003, с. 47), а это несколько ниже, чем установлено для заявляемых форм.
Таким образом, иммуностимулятор, полученный заявляемым способом (варианты), в отличие от прототипа, содержит повышенное содержание пептидов, что позволяет усилить иммуностимулирующее действие у продукта и повысить его эффективность.
Кроме того, предложена таблетированная форма выпуска, которая удобна для перорального приема.
Содержание аскорбиновой кислоты в предлагаемой биологически активной добавке соответствует допустимой суточной норме, но увеличено по сравнению с прототипом, усиливая иммуностимулирующий эффект пептидов.
Использовать БАД возможно в качестве профилактического продукта в осенне-весенний период, как вспомогательное средство при лечении простудных и вирусных заболеваний, при вторичных иммунодефицитных состояниях различного генеза.
Изобретение подтверждается примерами конкретного выполнения:
Пример 1
10 кг замороженных ганглий кальмара размораживают до температуры минус 4°C в центре брикета и измельчают на электромясорубке. Экстракцию измельченных ганглий проводят в 50 л 3%-ного раствора уксусной кислоты. Время экстракции составляет 40 ч при периодическом перемешивании в течение 15 мин через каждые 1,5 ч. По завершении этого времени смесь подщелачивают концентрированным раствором бикарбоната натрия до рН=8,5, добавляют 0,5 л 0,3% раствора хитозана в 3% уксусной кислоте и продолжают периодическое перемешивание в течение 1 часа. Экстракционную массу центрифугируют на центрифуге при 5000 об/мин в течение 20 мин. Надосадочную жидкость, которая является раствором с целевым веществом, отделяют и добавляют к ней 3,2 кг сульфата аммония, т.е. до достижения 30% концентрации. Периодически перемешивают смесь в течение двух часов, затем центрифугируют на центрифуге при 5000 об/мин в течение 20 мин. Надосадочную жидкость подвергают диафильтрации на кассетной мембране с пределом разделения 1000 Да (установка Pellicon фирмы Millipore, Франция). После того как объем концентрата достигнет 3-4 л добавляют к нему 10 л дистиллированной воды и продолжают диафильтрацию. Процедуру с добавлением воды к концентрату повторяют 4 раза. Раствор с целевым веществом от 1000 до 15000 Да (концентрат) направляют на лиофильную сушку, сухой продукт облучают при перемешивании ультрафиолетом в течение 15 минут для стерилизации. Выход иммуностимулятора составил 110 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала, кроме того содержащий 6% минеральных веществ и 1,5% влаги, нерастворимый в ацетоне и этиловом спирте. Растворимость в воде составляет 20 мг/мл, спектральный максимум поглощения наблюдается при 268±3 нм. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Часть полученного препарата была использована для изготовления БАД в виде порошка следующего состава:
Пептиды - 0,3%,
Аскорбиновая кислота - 10%,
D-глюкоза - остальное.
Пример 2
9 кг замороженного мозга кеты размораживают на воздухе до температуры минус 4°С в центре брикета и измельчают. Экстракцию измельченного мозга проводят в 45 литрах 3%-ного раствора уксусной кислоты. Время экстракции составляет 36 ч при периодическом перемешивании в течение 15 мин через каждые 1,5 ч. По завершении этого времени смесь подщелачивают концентрированным раствором бикарбоната натрия до рН=8,5, добавляют 450 мл 0,3% раствора хитозана в 3% уксусной кислоте и продолжают периодическое перемешивание в течение 1 часа. Экстракционную массу разделяют на сепараторе и добавляют к фильтрату 3 кг сульфата аммония, т.е. до достижения 30% концентрации. Периодически перемешивают смесь в течение двух часов, затем фильтруют на нутч-фильтре. Надосадочную жидкость подвергают диафильтрации на установке Т66.00.00.000ПС Научно-производственная фирма «Гелла-ТЭКО», РФ, г. Москва) с керамическим мембранным элементом КУФЭ-1, предел разделения 1000 Да. После того как объем концентрата достигнет 3-4 л добавляют к нему 10 л дистиллированной воды и продолжают диафильтрацию. Процедуру с добавлением воды к концентрату повторяют 4 раза. Раствор с целевым веществом от 1000 до 15000 Да (концентрат) направляют на лиофильную сушку, сухой продукт облучают при перемешивании ультрафиолетом в течение 15 минут для стерилизации. Выход иммуностимулятора составил 87 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала, кроме того содержащий 7% минеральных веществ и 1,8% влаги, нерастворимый в ацетоне и этиловом спирте. Растворимость в воде составляет 20 мг/мл, спектральный максимум поглощения наблюдается при 268±3 нм. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Часть полученного препарата была использована для изготовления БАД в таблетированной форме, одна таблетка которой содержит:
Пептиды - 1,3 мг,
Аскорбиновая кислота - 10 мг,
D-глюкоза - 118 мг,
Целлюлоза микрокристаллическая - 68,8 мг,
Кальция стеарата - 2 мг.
Пример 3
10 кг замороженного мозга ларги размораживают на воздухе до температуры минус 4°C в центре брикета и измельчают на электромясорубке. Экстракцию измельченного мозга ларги проводят в 50 литрах 3%-ного раствора уксусной кислоты. Время экстракции 48 ч при периодическом перемешивании в течение 15 мин через каждый час. По завершении этого времени смесь подщелачивают концентрированным раствором бикарбоната натрия до рН=8,5, добавляют 0,5 л 0,3% раствора хитозана в 3% уксусной кислоте и продолжают периодическое перемешивание в течение 1 часа. Затем добавляют 1,5 кг сухого фильтроперлита, периодически перемешивают в течение 20 минут, после чего дают смеси отстояться в течение 4 часов. Надосадочную жидкость декантируют и высушивают на вакуумной ротационной сушке, сухой продукт облучают ультрафиолетовой лампой и стерильно упаковывают. Выход препарата составил 90 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала, кроме того содержащий 3% минеральных веществ и 3,5% влаги, нерастворимый в ацетоне и этиловом спирте. Растворимость в воде составляет 20 мг/мл, спектральный максимум поглощения наблюдается при 268±3 нм. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Часть полученного препарата была использована для изготовления БАД в виде порошка следующего состава:
Пептиды - 0,4%,
Аскорбиновая кислота - 12%,
Кристаллическая глюкоза - остальное.
Пример 4
5 кг замороженного мозга горбуши размораживают на воздухе до температуры минус 4°С в центре брикета и измельчают. Экстракцию измельченного мозга проводят в 25 литрах 3%-ного раствора уксусной кислоты. Время экстракции составляет 35 ч при периодическом перемешивании в течение 15 мин через каждые 1,5 ч. По завершении этого времени смесь подщелачивают концентрированным раствором бикарбоната натрия до рН=8,5, добавляют 250 мл 0,3% раствора хитозана в 3% уксусной кислоте и продолжают периодическое перемешивание в течение 1 часа. Затем добавляют 800 г сухого фильтроперлита, периодически перемешивают в течение 20 минут, после чего дают смеси отстояться в течение 4 часов. Надосадочную жидкость декантируют и высушивают на распылительной сушке, сухой продукт облучают ультрафиолетовой лампой и стерильно упаковывают. Выход препарата составил 45 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала, кроме того содержащий 2,2% минеральных веществ и 3,0% влаги, нерастворимый в ацетоне и этиловом спирте. Растворимость в воде составляет 18 мг/мл, спектральный максимум поглощения наблюдается при 269±3 нм. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Часть полученного препарата была использована для изготовления БАД в виде порошка следующего состава:
Пептиды - 0,2%,
Аскорбиновая кислота - 11%,
D-глюкоза - остальное.
Пример 5
8 кг замороженных оптических ганглиев осьминога размораживают на воздухе до температуры минус 4°C в центре брикета и измельчают. Экстракцию измельченного материала проводят в 40 литрах 3%-ного раствора уксусной кислоты в течение 40 ч при периодическом перемешивании в течение 15 мин через каждые 2 ч. По завершении этого времени смесь подщелачивают концентрированным раствором бикарбоната натрия до рН=8,5, добавляют 400 мл 0,3% раствора хитозана в 3% уксусной кислоте и продолжают периодическое перемешивание в течение 1 часа. Затем добавляют 4,4 л 20% водной суспензии бентонита, периодически перемешивают в течение 20 минут, после чего дают смеси отстояться в течение 4 часов. Прозрачную часть надосадочной жидкости декантируют и высушивают на распылительной сушке, сухой продукт облучают ультрафиолетовой лампой и стерильно упаковывают. Выход препарата составил 76 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала, кроме того содержащий 2,7% минеральных веществ и 4% влаги, нерастворимый в ацетоне и этиловом спирте. Растворимость в воде составляет 18 мг/мл, спектральный максимум поглощения наблюдается при 267±3 нм. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Часть полученного препарата была использована для изготовления БАД в таблетированной форме, одна таблетка которой содержит:
Пептиды - 1,5 мг,
Аскорбиновая кислота - 9 мг,
D-глюкоза - 125 мг,
Картофельный крахмал -68,8 мг,
Кальция стеарата - 2 мг.
Пример 6
12 кг замороженных оптических ганглиев кальмара размораживают на воздухе до температуры минус 4°C в центре брикета и измельчают. Экстракцию измельченных ганглиев проводят в 60 литрах 3%-ного раствора уксусной кислоты в течение 40 ч при периодическом перемешивании в течение 15 мин через каждые 2 ч. По завершении этого времени смесь подщелачивают концентрированным раствором бикарбоната натрия до рН=8,5, добавляют 600 мл 0,3% раствора хитозана в 3% уксусной кислоте и продолжают периодическое перемешивание в течение 1 часа. Затем добавляют 7 л 20% водной суспензии бентонита, периодически перемешивают в течение 20 минут, после чего дают смеси отстояться в течение 4 часов. Прозрачную часть надосадочной жидкости декантируют, остальное отделяют на нутч-фильтре, супернатанты объединяют и высушивают на вакуумной ротационной сушке, сухой продукт облучают ультрафиолетовой лампой и стерильно упаковывают. Выход препарата составил 110 г.
Конечный препарат представляет собой аморфный порошок белого цвета, состоящий в основном из пептидного материала, кроме того содержащий 3% минеральных веществ и 3% влаги, нерастворимый в ацетоне и этиловом спирте. Растворимость в воде составляет 20 мг/мл, спектральный максимум поглощения наблюдается при 268±3 нм. Распределение пептидных компонентов по молекулярной массе, определенное с помощью гель-проникающей хроматографии, показано в таблице 1.
Часть полученного препарата была использована для изготовления БАД в таблетированной форме, одна таблетка которой содержит:
Пептиды - 1,5 мг,
Аскорбиновая кислота - 10 мг,
D-глюкоза - 120 мг,
Целлюлоза микрокристаллическая - 68,8 мг,
Кальция стеарата - 2 мг.
1. Способ получения иммуностимулятора пептидной природы из нервной ткани морских гидробионтов, включающий размораживание, измельчение сырья, экстрагирование его 3%-ным раствором уксусной кислоты, получение и отделение надосадочной жидкости, выделение конечного продукта, отличающийся тем, что сырье экстрагируют в течение 35-48 ч при перемешивании в течение 15 мин через каждые 1,5 часа, затем подщелачивают раствором бикарбоната натрия до рН=8,0-8,5, добавляют 0,3% раствор хитозана в 3% уксусной кислоте, выдерживают в течение одного часа, полученную массу центрифугируют на центрифуге 5000 об/мин в течение 20 мин, к надосадочной жидкости добавляют сульфат аммония до 30% концентрации раствора, выдерживают при помешивании в течение двух часов, снова центрифугируют на центрифуге 5000 об/мин в течение 20 мин, надосадочную жидкость диафильтруют на кассетной мембране с пределом разделения 1000 Да четырежды с добавлением к получаемому концентрату дистиллированной воды в соотношении концентрат : вода 1:2 до получения раствора с конечным веществом от 1000 до 15000 Да.
2. Способ по п. 1, отличающийся тем, что концентрат подвергают лиофильной сушке с последующим ультрафиолетовым облучением.
3. Способ получения иммуностимулятора пептидной природы из нервной ткани морских гидробионтов, включающий размораживание и измельчение сырья, экстрагирование его 3%-ным раствором уксусной кислоты, получение и отделение надосадочной жидкости, выделение конечного продукта, отличающийся тем, что сырье экстрагируют в течение 35-48 ч при перемешивании в течение 15 мин через каждые 1,5 часа, затем подщелачивают раствором бикарбоната натрия до рН=8,0-8,5, добавляют 0,3% раствор хитозана в 3% уксусной кислоте, выдерживают в течение одного часа, добавляют неорганический адсорбент природного происхождения, периодически перемешивая в течение 20 мин, затем отстаивают смесь в течение 4 часов, надосадочную жидкость декантируют.
4. Способ по п. 3, отличающийся тем, что концентрат высушивают на вакуумной ротационной или распылительной сушках, в условиях, исключающих нагрев выше 30-40°C, сухой продукт облучают ультрафиолетовой лампой.
5. Биологически активная добавка, содержащая природный пептид, аскорбиновую кислоту, глюкозу, отличающаяся тем, что в качестве пептида используют иммуностимулятор пептидной природы, полученный способом по пп. 1 и 3.
6. Биологически активная добавка по п. 5, отличающаяся тем, что биологически активная добавка имеет форму выпуска порошок при следующем соотношении компонентов (в 1 порошке, %):
Пептиды - 0,1-0,5,
Аскорбиновая кислота - 8-16,
D-глюкоза или кристаллическая глюкоза - остальное.
7. Биологически активная добавка по п. 5, отличающаяся тем, что биологически активная добавка имеет форму выпуска таблетку при следующем соотношении компонентов (в 1 таблетке, мг):
Пептиды - 1,0-1,5,
Аскорбиновая кислота - 8-10,
D-глюкоза или кристаллическая глюкоза - 118-125,
Целлюлоза микрокристаллическая
или крахмал картофельный - 68,8,
Кальция стеарат - 2,0.