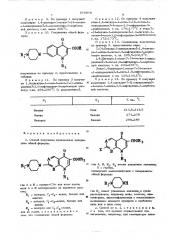
Способ получения производных пиперазина или их солей
Иллюстрации
Показать всеРеферат
ОП ИСАНИЕ
ИЗОБРЕТЕН Ия к nATEHTV
Союз Советских
Социалистимеских Республик (11) 578875 (61) Дополнительный к патенту (51) М. Кл.-"
С 07. Б 241/04
С 07D 215/16
//А 61 К 31/495 (22) Заявлено 17,12.73(21) 1979632/04
18.12.72;21.12.72; (23) Приоритет — (3-) 17 04 73;26 10 73
1 26968/72, 1 28441 /72
43388/73;121058/73 (43) Опубликовано30.10.77.Бюллетень №40
Гасударственный комитет
Совета Министров СССР по делам изобретений и открытий (53) УДК547. 861. ,3.07:547. 831. .07 (088,8) (45) Дата опубликования описания 10.12.77
Иностранцы
Синсаку Минами, Юн-Ити Мацумото, Минору Сугита, Масанао Симицу, Есиюки Таказе и Синити Накамура (Япония) (72) Авторы изобретения
Иностранная фирма
Дайннппон Фармасьютикал Ко, ЛТД" (Япония) (71) Заявитель (54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИПЕРАЗИНА
ИЛИ ИХ СОЛЕЙ
/ \
R=N Х
СООR 3 ОО З
1
Изобретение относится к способу получе-. ния новых производных пиперазнна, которые обладают высокой биологической активностью и могут найти применение в фармацевтической промышленности. 0
Использование известной в органической химии реакции взаимодействия галоидных арилов со вторичными аминами (1). с обра.зованием ароматических третичных аминов применительно к галоидным производным тп пиридина и замешенному пиперазину позволило получить новые производные пипераэина общей формулы где А и В - группа = CH - или атом азота, если А и В одновременно не.ттвляются азотом;
R» - водород, с;» -С4-алкил, бензнл или ацетил;
Яе- водород, С» »С4 -алкил, бензил или винил;
Р - водород или С -С -алкил, а также нх соли, обладающие высокой биологической активностью.
Предложенный способ получения производ» ных пипераэина обшей формулы Т или их оо
1 лей заключается в том, что соединение общей формулы где А, В, R>, R имеют укаэанные значения, Х - галоид, подвергают взаимодействию с пиперазином общей формулы где 1 1 имеет указанные значения, в среде растворителя, например воды, зтанопа, аце тонитрида, диметипформамида, предпочти
1О тельно при нагревании, например при тем пературе кипения реакционной массы или о при 170 С, в замкнутом реакционном сосуде с последующим выделением целевого продукта в свободном виде или в виде соли.
По предложенному способу получают пред почтительно следук пие, соединения обшей формулы:
1,4- дигидро-1-атил-7-(4-метил-1-пидеразинил)-4-охсохинолин-3-карбоновая кисло20 та
1,4-дигидро 1-атил 7-(1-пиперазинип)-4-оксохинолин-3-карбоновая кислота
1,4-дигидро-1-атил-7-(4-метил-1-пипера зинил)-4-окса-1,6-нафтиридин-Ç-карбоновая кислота
1,4-дигидро-1-атил-7-(1-пиперазинип)-4-оксо-1,6-нафтндридин-З-карбоновая кислота
1,4-дигидро-1-этип-7-(1-пиперазинип)-4» -оксо-1,8-нафтиридин-З-карбоновая кислота
1,4-дигидро-7-(ч-метил з.-пиперазинил)-4-оксо-1-винил-1,8-нафтирндин 3-карбоновая кислота
1,4-дигидро-7-(4-метил-1-пиперазинил)-4оксо-1-винил-1,6-нафтиридин-Ç-карбоновая хиспота
1,4-дигидро 7-(4-метил-1-пиперазинип)-4 -оксо-1-винилхинолин-3-карбоновая кислота
Ъ
1,4-диги дро-7-(1-пиперазинил)-4,оксо-1-винил-l,8-нафтиридин«З-карбоновая кислота
1,4-дигидро 7-(1-пиперазиннл)-4-оксо-1-винил-1,6-нафтиридин-Ç-карбоновая кислота
1,4-дигидро-7-(1-пнперазинип)-4-оксо-1 винилхинэлин-З-.карбоневая хиспота..
Реакцию осушествляют путем нагревания соединений 11 u III вместе с растворителем, прн необходимости, в закрытом реакционном сосуде. Предпочтительно проводят реакцию в присутствии в качестве дегидрогапогенирр->О ющего агента такого основании, как карбонат натрия, карбонат калия ипи триатиламин.
Обычно соединения Я и Jll применяют в сте
„: химетрических количествах, испопъзование избытка соединений Ц и Ш действует так же, хак дегидрогалоидирующий агент. Соединение Я может использоваться в виде гидрата или сопи, Предпочтительная температура реакции о находится в области от 60 до 200 С.
Используемый в данной реакции растворитель должен выбираться в соответствии со свойствами применяемых исходных материалов. Примерами растворителя являются спирты, такие как атанол ипи пропанол, аромати ческие углеводороды,: такие как бензол ипи топуоп, гапоидоапканы, такие как дихпоратан или хлороформ, простые эфиры, такие как тетрагидрофуран, диоксан или дифениловый простой афир, ацетонитрил, диметилсульфохсид, -диметилформамид, н вода. Они могут использоваться либо отдельно, либо в смеси, Предложенные соединении могут быть изолированы и очищены обычными методами. Соединения I могут быть получены в свободном состоянии или в виде соли, в зави симости от выбора исходных соединений и реакционных условий. Кроме того, соединения Т могут быть превращены в пригодные соли аминов или соли карбоновой кислоты обработкой кислотой или щелочью. Кислотой могут служить различные органические и неорганичесхие кислоты, примерами которых являются: хлористоводородная, уксусная, мо лочная, янтарная, шевелевая и метансупьфо новая кислоты.
Пример 1. 1,4-Лигидро-1-атил-4-оксо-7-(1-пиперазинил)-хинолин-З»харбоновая .кислота и ее хпоргидрат.
Смесь, содержащую 1,5 r 7-хлор-1,4-дигидро-1-атил-4-оксохинолин-3-карбоновой кислоты, 5,0 г пиперазингексагидрата и 8 мп воды, нагревают в запаянной трубо ке при 170 С в течение 18 ч. Реакционную смесь встряхивают с хлороформом дпя уда пения растворимого в органическом раство» рителе материала. Конечный водный слой обрабатывают обесцвечиваюшим древесным углем и подкисляют хпористоводородной кислотой до получения осадка, который собирают и перекристаллизовывают из смеси атанопа и воды до выхода 1,35 г хлоргид» о
para, т.пл. выше 300 С.
Хлоргидрат растворяют в горячей воде и раствор доводят до рН 7,5-8,0 с помощью 107.нбго водного раствора гидроохиси натрия. Конечную свободную карбоновую кислоту собирают и .перекристаппизовывают из смеси диметилформамида с водой; т.пп.
272-275 С.
Пример 2. 1,4-йигидро1-атил-7»
»(4-метил-1-пине разинил}-4оксохинолин-3-харбоновая кислота.
Смесь, содержащую 0,95 г 7-хлор-1-erma-1,4-дигидро-4-оксохинолин-3-карбо новой хислоты, 0,85 r 1-метиппиперазина и
6 мл воды нагревают в запаянной трубке о при 170 С в течение 18 ч. И я удаления растворимого в органическом растворителе ма гериапа реакционную смесь встряхивают
578875 с хлороформом. Полученный водный слой нейтрализуют уксусной кислотой до получения твердого вещества, которое собирают, промйвают водой и перекристаллиэовыва:от из смеси диметилформамида и воды до выхода 0,81 r; т.пл. 220,5-225,5 С.
Пример 3. 1,4-Лигидро-1-этил1
-7-(4-метил-1- пиперазинил}-4-оксо-1,6-нафтиридин-З«карбоновая кислота.
К суспензии из 1,27 г 7-хлор-1,4-ди- Ip гидро-1-этил-4 «оксо-1,6-нафтиридина-Ç-карбоновой кислоты в 35 мл этанола добав ляют 1,25 г 1-метилпиперазина и смесь на1ревают до кипения в течение 15 ч. Полученный осадок собирают и перекристаллиэовы- IS вают из этанола с получением в виде продукта желтых игольчатых кристаллов, т.пл.
238-240 С.
Пример 4. Этил 1,4-дигидро-1-этил-4-оксс7-(1-пиперазинил) -1,6-нафти- 20 ридин-З-карбоксилат.
Смесь, содержашую 1,40 г этил 7-хлор-1,4-дигидро-1-этил-4-оксо-1, 6-нафтиридин-3-карбоксилата, 2,0 r пиперазингексагидрата и 50 мл этанола, нагревают до темпе- 25 ратуры кипения в течение 12 ч. Реакционную смесь концентрируют и охлаждают до получения твердого вешества, которое собирают и перекристаллиэовывают из этилацетата до выхода в качестве продукта 1,53 г о желтого порошка, т.пл. 169-170 С.
Пример 5. 1,4-йигидро-1-этил-4-оксо-7-{1-пипераэинил)-1,8-нафтиридин-З-карбоновая клслота, К суспензии иэ 2,53 r 7-хлор-1-этил-l,4-дигидро-4-оксо-1,8-нафтиридин-З-карбоновой кислоты в 90 мл ацетонитрила добавляют 5,82 r пиперазингексагидрата.
Смесь выдерживают с перемешиванием при
40 комнатной температуре в течение 3 ч и затем концентрируют досуха в вакууме. Получаюшийся твердый остаток помешают в
15 мл 1 0%ного водного раствора гидооокиси калия. Раствор доводят ao pH 8-9
45 при охлаждении с выходом твердого вешества, которое собирают, промывают водой и перекристаллизовывают из воды с получением в виде продукта 2,3 r бесцветных игольчатых кристаллов; т.пл. 271-272 С.
Пример 6. Гидрохлорид 1,4-дигидро-4-оксо-7-(1-пипераэинил)-1-винилхинилин-3-карбоновой кислоты.
Смесь, содержашую 1,0 r 7-хлор-1,4-дигидро-4-оксо-1-винилхинолин-3-карбоноS5 вой кислоты, 6,2 r пиперазингексагидрата и о
30 мл диметилформамида, греют при 110 С с перемешиванием в течение 4 ч. Реакционную смесь концентрируют досуха в вакууме и к полученному остатку последовательно
60 добавляют 50 мл воды и 5 мл уксусной кислоты. Кислую смесь в течение 3-5 мин греют на паровой бане и фильтруют для удаления нерастворимого материала. f!îñíå концентрирования фильтрата досух» полученный остаток помешают в 40 мл воды. К водному раствору добавляк>т около 5 мл 2 3",.ной хлористоводородной кислоты и раствор затем охлаждают vIB выделения тьердого вешества. Собранное твердое вешество перелристаллизовывают иэ смеси метанола и воды, содержашей каплю 20%ной хлористоводородной кислоты, с получением 0,55 и продукта; т.пл. 283-287 С с разложением.
Пример 7.
1,4-йигидро- i -(4-метил-1-липе разини л)-4-оксо-1-винилхинолин-3-карбоновая кислота и ее гидрохлорид.
Смесь, содержашую 5,0 r 7-хлор-1,4«
-дигидро-4-оксо-1-винилхинолин-3-карбоновую кислоту, 75 мл диметилс „льфоксида и 15 мл 1-метилпипепазина выдерживают при температуре 110 С в течение 3 ч с перемешиванием, после чего ее концентрируют до сухого состояния при пониженном давлении. Остаток растирают в порошок с метанолом с получением кристаллов. которые затем собирают и перекристаллизовывают из диметилформамида в смеси с водой (в соотношении 1:1) с получением 2,85 г о гидрохлорида; т.пл. выше 300 С.
1,5 г этого гидрохлорида растворяют в
200 мл горячей воды и нейтрализуют нормальным раствором гидрата окиси натрия.
Кристаллы, выделившиеся при охлаждьнии, собирают и перекристаллизовывают из ацетонитрила с получением 1,2 г соединения в виде гигроскопических бледно-желтых о игловидных кристаллов, т.пл. 224-225 С.
If р и м е р 8. 1,4-Дигидро-4-оксо-7-(1-пиперазинил)-1-винил-1,d-нафтиридин-3-карбоновая кислота, гидрохлорид.
В раствор 2,5 г 7-хлор-1,4-дигидро-4-оксо 1-винил-1,8-нафтиридин-Ç-карбоновой
Ю кислоты в 80 мл этанола добавляют 5,8 г пине разингексагидрата.
Эту смесь нагревают при кипячении с об ратным холодильником в течение 2 ч и концентрируют до сухого состояния при пониженном давлении. К конечному остатку добавляют 10 мл 1 н. соляной кислоты. Кристаллы, которые при охлаждении выделяются, собирают и растворяют в 40 мл горячей воды.
Раствор с 0,5 г древесного угля выдерживают при слабом нагревании в течение нескольких минут с последуюшим фильтрованием.
После добавления 6 мл 1 н. соляной кислоты фильтр охлаждают с получением 2,7 г продукта в виде бесцветных игловидных и кристаллов; т. пл. 285-287 С (с разложе нием), 578875
О
И
eOOlK 10
R - Ì
1 о
T. пл., С
213,5 214,5
277-279
2 88-289
Этил
Бензил
Бензил
Бензил
Метил
Водород
35 ОО 3
45
Л р н м е р 9. По примеру 1 получают хлоргидрат 1,.4-дигидрс-l-антил»7-(4-метил-1-пиперазинил)-4-оксохинолин-3-карбоноо вой кислоты; т.пл. выше 300 С.
Пример 10. Соединения обшей формулы полученные по примеру 2, представлены в таблице.
Пример 11. По примеру 3 получают 1,4-дигидро-l-этил-4-оксо-7-(1-пипе- 20 разинил)- 1,6-нафтиридин-Ç-карбоновую кислоту; т.пл. 294-296 С (с разложением).
Формула изобретения
1. Способ получения производных пиперазина обшей формулы. где А и В - группа=СН- или атом азота, если А и В одновременно не являются азо том;
Я - водород, С -С4- алкил, бензил или аде тил;
R - водород, С -С4-алкил, бензил или
3 винил
Ы водород или С -С -алкил, 3 или их солей, с т л и ч а ю ш и и с я тем, что соединение общей формулы
Пример 12. По примеру 4 получают атил-l,4-дигидро-l-атил-7-(4-метил-l-пиперазинил)-4-оксо-l,б-нафтиридин-Çо
-карбоксилат, т. пл. 176-177 С и этил-7-(4-бензил-l-пиперазинил)-1,4-диги др-1-этил-4-оксо-l,б-нафтиридин-З карбоксилат; о т. пл. 172-173 С.
Пример 13. Соединения, полученные по примеру 5, представлены ниже.
7-(4-Бензил-l-пиперазинил)-1,4-дигидро-l-атил-4-оксо-l, 8-нафтиридин-3-карбс о новую кислоты, т. пл. 205,5-206,5 С.
1,4-йигидро-l»этил-7- (4 метил-1-пипе» разинил)-4-оксо-1,8-нафтиридин-З-карбоновую кислоты; т. пл. 233-235 С.
Этил-1,4 дигидро-1-этил-7-(4-метил-l-пиперазинил)-4-оксо-1,8-нафтиридин-З« о
-карбоксилат; т. пл. 130-130,5 C.
Пример 14. По примеру 6 получают хлоргидрат 1,4-дигидрс-7-(1-пиперазинил)»4-оксо- -винил-l,á-нафтиридин-З-карбоно вой кислоты. где А, В, R>, К имеют указанные значения;
Х - галоид, подвергают взаимодействию с пиперазином обшей формулы
/ к-м 3Н где R имеет указанные значения в среде растворителя, например воды, этанола аде тонитрила, диметилформамида с rtocaenyxaaaM. выделением целевого продукта в свободном виде или в виде соли.
2. Спосоо по п. 1, о т л и ч а ю ш и й» с я тем, что процесс осушествляют при нагревании, например, при температуре кипе578875
10 азота, R» -ацетнл; h 2 -всгде В - атом дород.
26. 10.73„ где А - атом азота, R - винил.
Составитель С Дашкевич
Редактор Р. Никольская Техред О. Луговая Корректор И. Гокснч
Заказ 3828/707 Тираж 557 Подписное
ЦНИИПИ Государственного комитета Совета Министров СССР по делам изобретений и открытий
113035, Москва, Ж35, Раушская наб., д, 4/5
Филиал ППП Патент, г. Ужгород, ул. Проектная, 4
9 о ния реакционной массы нли при 170 С, в замкнутом реакционном сосуде.
Приоритет по признакам:
18,12.72., где А и 8 группа=СН; Й» - водород
С» -С -алкил, бензил; Кй -С» -Сй. алкил, бензищ R> - водород, 21.12.72., где Ry С - алкил. 17.04.73., 5
Источники информации, принятые во внимание при экспертизе:
1. Вейганд-Хильгетаг. Методы эксперимента в органической химии, М„1969, »о с. 427..