Соединения фенилпиридазина и содержащие их лекарственные средства
Иллюстрации
Показать всеПредложены соединения фенилпиридазина, представленные следующей формулой (I):
где R1 представляет замещенный или незамещенный фенил, где заместители выбраны из группы, содержащей галоген, низший алкил, низший алкокси и фенилтио; или пиридил; R2 представляет низшую алкоксигруппу, низшую алкилтиогруппу, низший алкилсульфинил или низший алкилсульфонил; R3 представляет водород или низшую алкоксигруппу; или R2 и R3 вместе могут быть конденсированы, образуя низший алкилендиоксигруппу; R4 представляет циано; карбоксил; замещенный или незамещенный низший алкил, где заместители выбраны из группы, содержащей гидроксил, карбоксил и N-гидрокси-N-низший алкиламинокарбонил; низший алкенил; низший алкилтио; низший алкилсульфинил; низший алкилсульфонил; низший алкилсульфонилокси; замещенный или незамещенный фенокси, где заместители выбраны из группы, содержащей галоген, низший алкокси, нитро, циано; незамещенный фенилтио или фенилтио, замещенный галогеном; пиридилокси; морфолино; морфолинокарбонил; 1-пиперазинилкарбонил, замещенный низшим алкилом; замещенный или незамещенный амино, где заместители выбраны из группы, содержащей низший алкил, бензил, фенил, который может быть замещен атомами галогена или низшими алкоксигруппами и n=0; или их соли. Данные соединения обладают превосходной ингибирующей активностью против производства интерлейкина-1β и могут быть использованы при производстве лекарственного средства, ингибирующего производство интерлейкина-1β, при лечении и профилактике таких заболеваний, как заболевания иммунной системы, воспалительные заболевания и ишемические заболевания. Предложены также промежуточные соединения для получения соединений формулы (I). Кроме того, предложены лекарственное средство и фармацевтическая композиция, ингибирующие производство интерлейкина-1β и ингибитор производства интерлейкина-1β. 6 н. и 1 з.п. ф-лы, 1 табл.
Реферат
Область изобретения
Настоящее изобретение касается соединений фенилпиридазина, обладающих превосходной ингибирующей активностью против производства интерлейкина-1β, способов профилактики и лечения заболеваний иммунной системы, воспалительных заболеваний, ишемических заболеваний и им подобных с применением данных соединений и лекарств, содержащих данные соединения в качестве активных ингредиентов.
Известный уровень техники
При многих заболеваниях, таких как ревматизм, артрит, остеопороз, воспалительный колит, синдром иммунодефицита, пиемия, гепатит, нефрит, ишемическая болезнь, инсулинзависимый сахарный диабет, артериальный склероз, болезнь Паркинсона, болезнь Альцгеймера и лейкоз, наблюдается стимуляция производства воспалительного цитокина, известного как интерлейкин-1β. Интерлейкин-1β служит для индуцирования синтеза фермента, такого как коллагеназа и PLA2, который, как считают, принимает участие в воспалении и при внутрисуставном введении животным вызывает множественное суставное разрушение, в высокой степени похожее на ревматоидный артрит. С другой стороны, в нормальном живом организме активность интерлейкина-1β контролируют рецепторы интерлейкина-1 растворимый рецептор интерлейкина-1 и антагонисты рецепторов интерлейкина-1.
Из исследования, проведенного с применением рекомбинант данных ингибирующих биологическую активность веществ, анти-интерлейкин-1β антител, анти-рецепторных антител и мышей с ударными дозами на моделях различных заболеваний, обнаружено, что интерлейкин-1β играет центральную роль в организме, приводя к повышению эффективности веществ, обладающих анти-интерлейкин-1β-ингибирующей активностью, в качестве терапевтических средств для таких заболеваний.
Например, сообщается, что иммуносупрессоры и стероиды, применяемые для лечения ревматизма, ингибируют производство интерлейкина-1β. Сообщается, что даже среди лекарств, находящихся в настоящее время в разработке, КЕ298, производное бензоилпропионовой кислоты [The Japanese Society of Inflammation (11th), 1990], например, обладает ингибирующей активностью против производства интерлейкина-1β, хотя оно является иммунорегулятором. Ингибирующую активность против производства интерлейкина-1β наблюдают также в группе соединений, называемых "СОХ-2 селективными ингибиторами", включая, например, нимесулид, как производное феноксисульфонанилида (DE 2333643), Т-614, как производное феноксибензопирана (US 4954518), и тенидап (производное оксииндола), как двойных ингибиторов (COX-1/5-LO).
Однако для всех этих соединений активность ингибирования производства интерлейкина-1β не является первичным действием, поэтому их ингибирующее действие против производства интерлейкина-1β ниже их первичной активности.
В последние годы исследования продвигаются с возрастающей активностью и сфокусированы на ингибирующем действии против производства интерлейкина-1β. Ингибиторы производства можно классифицировать по группе соединений, которые ингибируют процесс передачи воспалительного сигнала ядру клетки и процесс транскрипции и трансляции, и другой группе соединений, которые ингибируют фермент ICE, который действует в превращении предшественника интерлейкина-1β. Известные примеры соединений, которые, как полагают, оказывают первичное действие, включают SB203580 [выложенная заявка (Kokai) на японском языке (PCT) №HEI 7-503017], FR167653 (Eur. J. Pharm., 327, 169-175, 1997), T-5090 (EP 376288), CGP47969A (Gastroenterology, 109, 812-828, 1995), производные гидроксииндола (Eur. J. Med. Chem., 31, 187-198, 1996) и производные триарилпиррола (WO 97/05878), тогда как известные примеры соединений, которые, как полагают, оказывают вторичное действие, включают VE-13045, который представляет собой пептидное соединение (Cytokine, 8(5), 377-386, 1996).
Однако ни одно из таких соединений не демонстрирует достаточную ингибирующую активность против производства интерлейкина-1β.
С другой стороны, известно, что разнообразные производные 5,6-дифенилпиридазина оказывают обезболивающее и противовоспалительное действие (Eur. J. Med. Chem., 14, 53060, 1979). Однако абсолютно ничего не известно в отношении ингибирующей активности данных производных 5,6-дифенилпиридазина против производства интерлейкина-1β.
В последние годы в JP 7-69894, WO 9841511, WO 9910331, WO 9910332, WO 9925697 и WO 9944995 раскрыты некоторые производные пиридазина, как обладающие ингибирующей активностью против производства интерлейкина-1β. Однако они отличаются по химической структуре от соединений настоящего изобретения.
Таким образом, одной целью настоящего изобретения является обеспечение соединения, обладающего превосходной ингибирующей активностью против производства интерлейкина-1β.
Краткое описание изобретения
Настоящее изобретение касается соединений пиридазина, представленных общей формулой (I), обладающих превосходной ингибирующей активностью против производства интерлейкина-1β и полезных в качестве лекарственных средств для профилактики и лечения заболеваний иммунной системы, воспалительных заболеваний и ишемических заболеваний.
А именно, настоящее изобретение относится к соединению фенилпиридазина, которое представлено следующей формулой (I):
где R1 представляет замещенную или незамещенную фенильную группу или замещенную или незамещенную пиридильную группу;
R2 представляет низшую алкоксигруппу, низшую алкилтиогруппу, низшую алкилсульфинильную группу или низшую алкилсульфонильную группу;
R3 представляет атом водорода или низшую алкоксигруппу;
или R2 и R3 вместе могут быть конденсированы, образуя алкилендиоксигруппу;
R4 представляет водород, галоген, циано, карбоксил, замещенный или незамещенный низший алкил, замещенный или незамещенный низший алкенил, замещенный или незамещенный низший алкилтио, замещенный или незамещенный низший алкилсульфинил, замещенный или незамещенный низший алкилсульфонил, замещенный или незамещенный низший алкилсульфонилокси, замещенный или незамещенный арил, замещенный или незамещенный ароматический гетероцикл, замещенный или незамещенный фенокси, замещенный или незамещенный фенилтио, замещенный или незамещенный фенилсульфинил, замещенный или незамещенный фенилсульфонил, замещенный или незамещенный пиридилокси, замещенный или незамещенный морфолино, замещенный или незамещенный морфолинокарбонил, замещенный или незамещенный пиперидинокарбонил, замещенный или незамещенный 1-пиперазинилкарбонил или замещенный или незамещенный амино, и
n равно 0 или 1,
при условии, что, если R1 представляет 4-метоксифенильную группу, R2 представляет метоксигруппу и R3 представляет атом водорода, то R4 не может быть водородом или галогеном, а также R1 не может быть 4-(метилсульфонил)фенилом или 4-(аминосульфонил)фенилом;
или его соль.
Настоящее изобретение относится также к лекарственному средству, включающему в качестве активного ингредиента соединение фенилпиридазина (I) или его соль.
Настоящее изобретение относится также к ингибитору производства интерлейкина-1β, включающему в качестве эффективного ингредиента соединение фенилпиридазина (I) или его соль.
Настоящее изобретение относится также к фармацевтической композиции, включающей соединение фенилпиридазина (I) или его соль в качестве эффективного ингредиента и фармакологически приемлемый носитель.
Настоящее изобретение относится также к способу лечения заболевания, вызванного стимуляцией производства интерлейкина-1β, который отличается введением соединения фенилпиридазина (I) или его соли нуждающемуся в этом пациенту.
Кроме того, настоящее изобретение относится также к применению соединения фенилпиридазина (I) или его соли для производства лекарственного средства.
Подробное описание предпочтительных вариантов
Примерами низших алкильных групп и низших алкильных фрагментов в низшей алкоксигруппе, низшей алкилтиогруппе, низшей алкилсульфинильной группе, низшей алкилсульфонильной группе и низшей алкилсульфонилоксигруппе, которые использованы в данном описании, являются линейные, разветвленные или циклические низшие алкильные группы, имеющие от 1 до 6 атомов углерода, такие как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, н-пентил, 2-метилбутил, 2,2-диметилпропил, циклопентил, циклогексил, н-гексил, 2-метилпентил, 3-метилпентил, 2,2-диметилбутил и 2,3-диметилбутил. Примеры атомов галогена могут включать атомы фтора, хлора, брома и йода.
Примеры одной или более групп заместителей в замещенной фенильной или пиридильной группе, обозначенной R1 в формуле (I), включают галоген, гидроксил, алкил, низшие алкокси- и фенилтиогруппы, причем особо предпочтительны галоген, низшие алкокси- и фенилтиогруппы. Среди галогенов предпочтительны фтор и хлор, а среди низших алкоксигрупп предпочтительна метоксигруппа. Данные группы заместителей предпочтительно находятся в положении 4 фенильной группы, хотя, если требуется, могут располагаться в любом другом положении. Предпочтительной группой R1 является фенильная группа, или пиридильная группа, или группа, замещенная одним или более галогенами, низшими алкоксигруппами или фенилтиогруппами. Более предпочтительными группами R1 являются 4-метоксифенил, 4-пиридил, фенил, 4-фторфенил, 4-хлорфенил или 4-(фенилтио)фенил.
В качестве низшего алкильного фрагмента в низших алкокси, низших алкилтио, низших алкилсульфинильных или низших алкилсульфонильных группах, обозначенных R2, особо предпочтительной является метильная группа. Наиболее предпочтительными R2 являются метокси, метилтио или метилсульфонильная группы.
В качестве низшей алкоксигруппы, обозначенной R3, особо предпочтительной является метоксигруппа.
Кроме того, если R2 и R3 объединены, образуя алкилендиоксигруппу, предпочтительной является этилендиоксигруппа.
Примеры одной или более групп заместителей в замещенных низших алкильных группах, обозначенных R4, включают галоген, гидрокси, циано, нитро, амино, карбоксильные и замещенные или незамещенные аминокарбонильные группы. Иллюстрацией одной или более групп заместителей в аминокарбонильной группе является гидроксил и низшие алкильные группы. Примеры одной или более групп заместителей в замещенной низшей алкенильной группе, обозначенной R4, включают галоген и арильные группы. Примеры низшей алкенильной группы включают линейные, разветвленные или циклические низшие алкенильные группы, имеющие 1-6 атомов углерода, причем особо предпочтительна аллильная группа. Примеры одной или более групп заместителей в замещенной низшей алкилтиогруппе, замещенной низшей алкилсульфинильной группе, замещенной низшей алкилсульфонильной группе или замещенной низшей алкилсульфонилоксигруппе, обозначенной R4, включают арильные группы. Иллюстрацией одной или более групп заместителей в замещенной арильной группе или замещенной ароматической гетероциклической группе, обозначенной R4, является галоген, низший алкил, низшие алкокси, циано, нитро и аминогруппы, причем особо предпочтительны галоген и низшие алкильные группы.
Примеры арильной группы включают фенил и группы с 6-10 атомами углерода, такие как нафтил, причем особо предпочтителен фенил. Примеры ароматических гетероциклических групп включают 5- или 6-членные кольца, содержащие азот, причем особо предпочтителен пиридил. Примеры одной или более групп заместителей в замещенной феноксигруппе, обозначенной R4, включают галоген, циано, нитро, амино, низшие алкильные и низшие алкоксигруппы, среди которых особо предпочтительны галоген, циано, нитро и низшие алкоксигруппы. Иллюстрацией одной или более групп заместителей в замещенных фенилтио, замещенных фенилсульфинильных или замещенных фенилсульфонильных группах, обозначенных R4, является галоген, низший алкил, низшие алкокси, циано, нитро и аминогруппы, причем особо предпочтителен галоген. Иллюстрацией одной или более групп заместителей в замещенной пиридилоксигруппе, обозначенной R4, является галоген, низший алкил, низшие алкокси, циано, нитро и аминогруппы. Иллюстрацией одной или более групп заместителей в замещенных морфолино, замещенных морфолинокарбонильных или замещенных пиперидинокарбонильных группах, обозначенных R4, является галоген, низший алкил, низшие алкоксигруппы, циано и нитрогруппы. Иллюстрацией одной или более групп заместителей в замещенной 1-пиперазинилкарбонильной группе, обозначенной R4, является галоген, низший алкил, низшие алкокси, циано, нитро и аминогруппы, причем особо предпочтительны низшие алкильные группы. Иллюстрацией одной или более групп заместителей в замещенной аминогруппе, обозначенной R4, является низший алкил, замещенный или незамещенный фенил, бензил или ацильные группы, среди которых предпочтительны низший алкил, замещенный или незамещенный фенил и бензил. Примеры групп заместителей в фенильной группе включают галоген, циано, нитро, амино и низшие алкоксигруппы, причем предпочтительны галоген и алкоксигруппы.
Предпочтительными группами R4 являются водород; галоген; циано; карбоксил; низший алкил, который может быть замещен одной или более группами, выбранными из гидроксила, карбоксила или замещенных или незамещенных аминокарбонильных групп; низший алкенил; низший алкилтио; низший алкилсульфонил; низший алкилсульфонилокси; фенил; фенокси, который может быть замещен одной или более группами, выбранными из галогенов, циано, нитро или низших алкоксигрупп; фенилтио, который может быть замещен одним или более атомами галогенов; пиридилокси; морфолино; морфолинокарбонил; 1-пиперазинилкарбонил, который может быть замещен одной или более низшими алкильными группами; или аминогруппа, которая может быть замещена одной или более группами, выбранными из низшего алкила, замещенной или незамещенной фенильной или бензильной групп.
В производных фенилпиридазина формулы (I) настоящего изобретения R1 представляет замещенную или незамещенную фенильную или пиридильную группу, R2 представляет низшую алкокси-, низшую алкилтио- или низшую алкилсульфонильную группу, R3 представляет водород или низшую алкоксигруппу, или R2 и R3 вместе могут быть конденсированы, образуя алкилендиоксигруппу. R4 представляет водород, галоген, циано, карбоксил, замещенный или незамещенный низший алкил, низший алкенил, низший алкилтио, низший алкилсульфонил, низший алкилсульфонилокси, замещенный или незамещенный арил, замещенный или незамещенный фенокси, замещенный или незамещенный низший фенилтио, пиридилокси, морфолино, морфолинокарбонил, 1-пиперазинилкарбонил или замещенную или незамещенную аминогруппу, и n равно 0 или 1, при условии, что исключено производное фенилпиридазина формулы (I), в которой R4 представляет атом водорода или галогена, R1 представляет 4-метоксифенил, R2 представляет метоксигруппу и R3 представляет водород; или, что исключено производное фенилпиридазина формулы (I), в которой R1 представляет 4-(метилсульфонил)фенил или 4-(аминосульфонил)фенил. Более предпочтительные конкретные примеры соединений фенилпиридазина (I) настоящего изобретения включают:
3,4-бис(4-метоксифенил)-6-(фенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(2,3-дифторфенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(2,5-дифторфенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(2,6-дифторфенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(3,4-дифторфенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(2,3,5,6-тетрафторфенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(2,3,4,5,6-пентафторфенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(3,4,5-трихлорфенилтио)пиридазин,
3,4-бис(4-метоксифенил)-6-(4-метоксифенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(4-нитрофенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(2-цианофенокси)пиридазин,
3,4-бис(4-метоксифенил)-6-(3-цианофенокси)пиридазин,
6-(2,4-дифторфенокси)-3-(4-метоксифенил)-4-(4-пиридил)пиридазин,
6-(2,3-дифторфенокси)-3-(4-метоксифенил)-4-фенилпиридазин,
6-(2,4-дифторфенокси)-3-(4-метоксифенил)-4-фенилпиридазин,
3-(4-метоксифенил)-6-(2,3,4,5,6-пентафторфенокси)-4-фенилпиридазин,
3-(4-метилтиофенил)-6-фенилтио-4-(4-фенилтиофенил)пиридазин,
4-(4-хлорфенил)-6-(2,4-дифторфенокси)-3-[4-(метилтио)фенил]пиридазин,
3,4-бис(4-метоксифенил)-6-цианопиридазин и
6-циано-3-(4-метоксифенил)-4-фенилпиридазин.
Способ получения
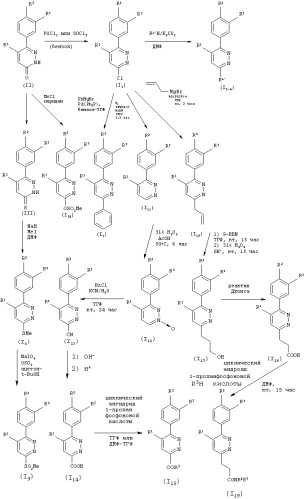
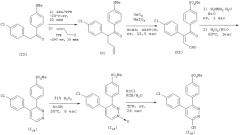
Способ получения соединения фенилпиридазина (I) настоящего изобретения или его соли не имеет никаких особых ограничений, и можно использовать различные способы, которые обычно используют для синтеза производных пиридазина, и их модификации. Например, соединение фенилпиридазина (I) настоящего изобретения или его соли можно получить по реакционным схемам любого из следующих способов получения 1-5.
(Способ получения 1)
где R1, R2 и R3 имеют такие же значения, как определены выше, R5 представляет замещенный или незамещенный морфолино, замещенный или незамещенный пиперидино, замещенный или незамещенный 1-пиперазинил или им подобные, R6 и R7 каждый независимо представляет водород, гидроксил, низший алкил или им подобные.
Описанные далее способы получения предполагают подходящие растворители, реагенты, катализаторы и условия для каждой реакции. Однако понятно, что они являются лишь иллюстративными по природе и не ограничивают настоящее изобретение.
В способе получения 1 исходные соединения (II) и (III) можно получить известными способами (WO 9925697).
(1) Получение соединения (I1), в котором R4 обозначает галоген:
Соединение (I1) можно получить взаимодействием агента галогенирования с соединением (II) в растворителе.
Подходящие растворители, применимые в данной реакции, включают бензол, толуол и N,N-диметилформамид (ДМФ). Подходящими агентами галогенирования являются оксихлорид фосфора и тионилхлорид. Предпочтительно проводить взаимодействие при температуре от 20 до 150°С в течение 0,5-10 час, более предпочтительно при температуре от 50 до 130°С в течение 1-5 час.
(2) Получение соединения (I2), в котором R4 обозначает замещенную или незамещенную феноксигруппу, соединения (I3), в котором R4 обозначает замещенную или незамещенную фенилтиогруппу, соединения (I4), в котором R4 обозначает замещенную или незамещенную пиридилоксигруппу, соединения (I5), в котором R4 обозначает замещенную или незамещенную морфолиногруппу, или соединения (I6), в котором R4 обозначает замещенную или незамещенную аминогруппу:
Соединения (I2-I6) каждое можно получить взаимодействием соответствующего соединения (I1) с R4'Н, в котором R4' обозначает замещенную или незамещенную феноксигруппу, замещенную или незамещенную фенилтиогруппу, замещенную или незамещенную пиридилоксигруппу, замещенную или незамещенную морфолиногруппу или замещенную или незамещенную аминогруппу, в присутствии основания в растворителе.
Подходящие основания включают неорганические основания, такие как карбонат калия, карбонат натрия и гидрид натрия; и органические основания, такие как алкоксиды металлов. Примеры подходящих растворителей включают ДМФ, диметилсульфоксид, ацетон и метилэтилкетон. Предпочтительно проводить взаимодействие при 20-150°С в течение 1-20 час, более предпочтительно при 50-130°С в течение 2-10 час.
(3) Получение соединения (I7), в котором R4 обозначает замещенный или незамещенный арил:
Соединение (I7) можно получить при растворении соответствующего соединения (I1) в растворителе, последовательном добавлении палладиевого катализатора и арилмагнийбромида и проведении их взаимодействие.
Подходящие для данной реакции растворители включают диэтиловый эфир, тетрагидрофуран (ТГФ), диметоксиэтан, бензол и толуол. Примеры палладиевого катализатора включают хлорид палладия и тетракис(трифенилфосфин)палладий. Предпочтительно проводить взаимодействие при 20-100°С в течение 0,5-2 час, более предпочтительно при 40-80°С в течение 1-1,5 час.
(4) Получение соединения (I8), в котором R4 обозначает алкилтиогруппу:
Соединение (I8) можно получить взаимодействием алкилгалогенида с соответствующим соединением (III) в присутствии гидрида натрия в растворителе.
Подходящие для данной реакции растворители включают ДМФ, диметилсульфоксид, ацетон, ТГФ, диоксан и метилэтилкетон. Предпочтительно проводить взаимодействие при перемешивании и температуре от 0 до 50°С в течение 0,5-2 час, более предпочтительно при 5-20°С в течение 1 час.
(5) Получение соединения (I9), в котором R4 обозначает алкилсульфонил:
Соединение (I9) можно получить окислением соответствующего соединения (I8) в растворителе.
Подходящие окислительные агенты включают смесь тетраоксид осмия-периодат натрия или метахлорпербензойную кислоту. В качестве растворителя можно использовать хлороформ, ацетон, бутанол или им подобные, или их смесь. Предпочтительно проводить взаимодействие при перемешивании и температуре от -40 до 50°С в течение 1-40 час, более предпочтительно при температуре от -10 до 20°С в течение 10-30 час.
(6) Получение соединения (I10), в котором R4 обозначает алкилсульфонилоксигруппу:
Соединение (I9) можно получить взаимодействием соответствующего соединения (II) с алкилсульфонилхлоридом в растворителе.
Подходящие растворители включают пиридин, пиколин и лутидин. Предпочтительно проводить взаимодействие при 10-40°С в течение 1-10 дней, более предпочтительно при 20-30°С в течение 3-5 дней.
(7) Получение соединения (I11), в котором R4 обозначает водород:
Соединение (I11) можно получить, подвергая соответствующее соединение (I1) каталитическому восстановлению в присутствии катализатора в растворителе.
Подходящие растворители включают метанол, этанол, ТГФ, этилацетат и уксусную кислоту. В качестве катализатора можно использовать 10% палладий на угле. Предпочтительно проводить реакцию в токе газообразного водорода при комнатной температуре и атмосферном давлении в течение 1-10 час, более предпочтительно в течение 4-5 час.
(8) Получение соединения (I12), в котором R4 обозначает водород, а именно, пиридазин-оксидного соединения:
Соединение (I12) можно получить взаимодействием соответствующего соединения (I11) с пероксидом водорода в растворителе.
Подходящим растворителем является уксусная кислота. Предпочтительно проводить взаимодействие при 20-80°С в течение 2-10 час, более предпочтительно при 40-60°С в течение 4-6 час.
(9) Получение соединения (I13), в котором R4 обозначает цианогруппу:
Соединение (I13) можно получить взаимодействием соответствующего соединения (I12) с ацилирующим агентом и цианидом щелочного металла в растворителе.
Подходящие цианиды щелочных металлов включают цианид натрия и цианид калия. В качестве ацилирующего агента можно использовать уксусный ангидрид, ацетилхлорид, бензоилхлорид или им подобные. Предпочтительно проводить взаимодействие при 10-40°С в течение 10-40 час, более предпочтительно при 20-30°С в течение 20-30 час.
(10) Получение соединения (I14), в котором R4 обозначает карбоксил:
Соединение (I14) можно получить гидролизом соответствующего соединения (I13) в присутствии неорганической кислоты или щелочи в растворителе.
Подходящие растворители включают воду, этанол, метанол и их смеси. В качестве неорганической кислоты можно использовать хлористоводородную, серную, азотную кислоты или им подобные. В качестве щелочи можно использовать гидроксид натрия, гидроксид калия или им подобные. Предпочтительно проводить реакцию при перемешивании и температуре 60-140°С в течение 0,5-2 час, более предпочтительно при 80-120оС.
(11) Получение соединения (I15), в котором R4 обозначает -COR5:
Соединение (I15) можно получить взаимодействием соединения, которое представлено формулой R5H, где R5 имеет такое же значение, как определено выше, с соответствующим соединением (I14) в присутствии агента конденсации.
Подходящие агенты конденсации включают 50% раствор циклического ангидрида 1-пропанфосфорной кислоты (n=3) в этилацетате. В качестве растворителя можно использовать ТГФ, ДМФ или их смеси. Предпочтительно проводить взаимодействие при перемешивании и температуре 10-40°С в течение 1-7 час, более предпочтительно при 20-30°С в течение 3-5 час.
(12) Получение соединения (I16), в котором R4 обозначает алкенил:
Соединение (I16) можно получить взаимодействием алкенилмагнийбромида с соответствующим соединением (I1) в присутствии палладиевого катализатора в растворителе и атмосфере инертного газа.
Подходящие растворители включают ТГФ, бензол и толуол. В качестве палладиевого катализатора предпочтителен тетракис(трифенилфосфин)палладий или ему подобные. Предпочтительно проводить взаимодействие при температуре -20-40°С в течение 0,5-4 час, более предпочтительно при температуре -10-10°С в течение 0,5-1,5 час, продолжая реакцию при 20-30°С в течение 1-3 час.
(13) Получение соединения (I17), в котором R4 обозначает гидроксиалкил:
Соединение (I17) можно получить, подвергая алкенильную группу соответствующего соединения (I16) реакции гидроборирования.
Реакцию гидроборирования можно проводить, например, добавляя раствор 9-борабицикло[3.3.1]нонана (9-BBN) или его соли к растворителю, в котором находится соединение (I16), в атмосфере инертного газа, такого как аргон или азот, перемешивая полученную смесь при 10-40°С в течение 5-30 час, предпочтительно при 20-30°С в течение 10-20 час, затем последовательно добавляя к реакционной смеси воду, водный раствор щелочи и раствор пероксида водорода при охлаждении ледяной водой и с последующим перемешиванием полученной таким образом смеси при 10-40°С в течение 1-4 час, предпочтительно при 20-30°С в течение 1,5-3 час.
(14) Получение соединения (I18), в котором R4 обозначает карбоксиалкил:
Соединение (I18) можно получить, подвергая соединение (I17) реакции окисления окислителем в растворителе.
Подходящие растворители включают ацетон и уксусную кислоту. В качестве окислителя предпочтителен реактив Джонса. Предпочтительно проводить взаимодействие при 10-40°С в течение 4-12 час, более предпочтительно при температуре 20-30°С в течение 6-10 час.
(15) Получение соединения (I19), в котором R4 обозначает алкил, замещенный замещенным или незамещенным аминокарбонилом:
Соединение (I19) можно получить взаимодействием соответствующего соединения (I18) и соединения, представленного формулой R6R7NH, в котором R6 и R7 имеют такие же значения, как определено выше, аналогично получению соединения (I15).
(Способ получения 2)
Получение соединения (I20), в котором R2 обозначает низший алкилсульфонил:
Соединение (I20) можно получить окислением соответствующего соединения (IV) в растворителе.
В данном случае можно применять реакцию, аналогичную реакции, применяемой при получении соединения (I9). Альтернативно, в качестве окислителя можно использовать пероксид водорода, а в качестве растворителя уксусную кислоту или тому подобное. В данном случае предпочтительно проводить взаимодействие при 40-100°С в течение 0,5-6 час, более предпочтительно при 60-80°С в течение 2-4 час.
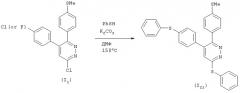
(Способ получения 3)
Получение соединения (I21), в котором R1 обозначает фенилтиофенил, и R4 обозначает фенилтиогруппу:
Соединение (I21) можно получить взаимодействием соответствующего соединения (I1), в котором R1 обозначает галогенфенильную группу, с тиофенолом в присутствии основания в растворителе.
Подходящие основания включают неорганические основания, такие как карбонат калия, карбонат натрия и гидрид натрия; и органические основания, такие как алкоксиды металлов. В качестве растворителя можно использовать ДМФ, диметилсульфоксид, ацетон, метилэтилкетон или им подобные. Предпочтительно проводить взаимодействие при 50-300°С в течение 5-40 час, более предпочтительно при 100-200°С в течение 10-30 час.
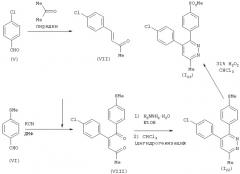
(Способ получения 4)
В способе получения 4 можно получить соединение (VII) взаимодействием ацетона с соединением (V) в присутствии основания в растворителе.
Подходящие растворители включают ацетон, этанол, метанол и их смеси. Примеры оснований включают пиперидин, морфолин и диизопропиламин. Предпочтительно проводить взаимодействие при перемешивании и температуре 10-40°С в течение 10 мин-1 час, более предпочтительно в течение 20-40 мин. Альтернативно, в качестве соединения (VII) можно использовать коммерческий продукт от Lancaster.
(1) Получение соединения (I22), в котором R4 обозначает алкил:
Соединение (I22) можно получить, проводя взаимодействие соединения (VI) и соединения (VII) в присутствии цианида щелочного металла в растворителе с получением соединения (VIII), взаимодействие гидразингидрата с соединением (VIII) в растворителе и последующую дегидрогенизацию.
Подходящие растворители для взаимодействия соединения (VI) и соединения (VII) включают ДМФ и диметилсульфоксид, а примеры цианида щелочного металла включают цианид калия и цианид натрия.
Подходящие растворители для взаимодействия с гидразингидратом включают этанол и изопропанол.
Предпочтительно проводить взаимодействие при перемешивании и температуре 50-100°С в течение 4-10 час, более предпочтительно при 70-90°С в течение 6-8 час. Реакцию дегидрогенизации можно осуществить окислением воздухом в таком растворителе, как хлороформ.
(2) Получение соединения (I23), в котором R2 обозначает алкилсульфонил, и R4 обозначает алкил:
Соединение (I23) можно получить взаимодействием соответствующего соединения (I22), в котором R2 обозначает алкилтиогруппу, по аналогичной методике получения соединения (I20).
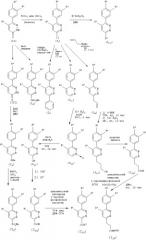
(Способ получения 5)
В способе получения 5 соединение (IX) можно получить по известной методике (WO 9925697). Соединение (Х) можно получить, добавлением литийдиизопропиламида (ЛДА) при -20°С к раствору соединения (IX) в ТГФ, проведением затем взаимодействия при комнатной температуре в течение 20 мин, добавлением аллилйодида и последующим проведением их взаимодействия при комнатной температуре в течение 30 мин. Соединение (XI) можно получить окислением соединения (Х) тетраоксидом осмия, аналогично описанному выше способу.
(1) Получение соединения (I24), в котором R1 обозначает галогенфенил и R4 обозначает водород:
Соединение (I24) можно получить взаимодействием соединения (XI) по аналогичной методике получения соединения (I22).
(2) Получение соединения (I25), пиридазин 1-оксида, в котором R1 обозначает галогенфенил и R4 обозначает водород:
Соединение (I25) можно получить взаимодействием соединения (I24) по аналогичной методике получения соединения (I12).
(3) Получение соединения (I26), в котором R1 обозначает галогенфенил и R4 обозначает цианогруппу:
Соединение (I26) можно получить взаимодействием соединения (I25) по аналогичной методике получения соединения (I13).
Промежуточные соединения и целевые соединения, полученные в описанных выше конкретных реакциях, можно выделить и очистить способами очистки, обычно применяемыми в синтетической органической химии, включая, но, не ограничиваясь ими, фильтрование, экстракцию, промывание, сушку, концентрирование, перекристаллизацию, различные хроматографические методы. Промежуточные продукты можно использовать в следующих реакциях без их очистки или можно очистить, если необходимо, применяя обычные способы очистки. Кроме того, их можно получать в виде сольватов растворителей, таких как реакционные растворители или растворители перекристаллизации, в особенности, гидратов.
Примерами солей фенилпиридазиновых соединений настоящего изобретения являются гидрохлорид, нитрат, гидробромид, ацетат, сульфат, пара-толуолсульфонат, метансульфонат, фумарат, сукцинат, лактат, соль натрия, соль калия, соль магния, соль кальция, соль аммония, соль метиламмония, соль диметиламмония и триметиламмония.
Фенилпиридазиновые соединения (I) и их соли, соответствующие настоящему изобретению, обладают превосходной ингибирующей активностью относительно производства интерлейкина-1β и полезны для профилактики и лечения заболеваний, вызванных стимуляцией производства интерлейкина-1β. Стимуляция производства интерлейкина-1β является причиной многих заболеваний, таких как заболевания иммунной системы, воспалительные заболевания, ишемические заболевания, остеопороз и пиемия. Настоящие соединения или их соли особо полезны в качестве лекарственных средств, таких как лекарства для профилактики и лечения ревматизма, синдрома иммунодефицита, артрита, воспалительного колита, ишемических заболеваний сердца, ишемической энцефалопатии, ишемического нефрита, ишемического гепатита, инсулинзависимого сахарного диабета, артериального склероза, болезни Паркинсона, болезни Альцгеймера и лейкоза, или ингибиторов производства интерлейкина-1β.
Фармацевтические композиции настоящего изобретения содержат в качестве активного ингредиента фенилпиридазиновые соединения (I) или их соли. Для данных композиций можно применять любые способы введения, включая, но, не ограничиваясь ими, пероральное введение в виде таблеток, капсул, гранул, порошков или сиропов, и парентеральное введение путем внутривенных инъекций, внутримышечных инъекций, в виде суппозиториев, ингаляций, трансдермальных препаратов, глазных капель или носовых капель. При получении фармацевтических композиций в виде различных стандартных дозированных форм активные ингредиенты можно использовать сами по себе или, если требуется, в комбинации с обычными фармацевтически приемлемыми эксципиентами, связующими, заменителями, разрыхлителями, поверхностно-активными веществами, смазывающими агентами, диспергирующими агентами, буферами, консервантами, модификаторами, ароматизаторами, покрывными агентами, растворителями, разбавителями и/или носителями.
Дозировку каждой фармацевтической композиции настоящего изобретения варьируют в зависимости от веса тела, возраста, пола и состояния пациента. Однако для взрослых обычно предпочтительно пероральное или парентеральное введение соединений, представленных формулой (I) в количестве примерно от 0,01 до 1000 мг, предпочтительно от 0,1 до 100 мг в день, одной или несколькими порциями.
Примеры
После описания данного изобретения в общих чертах можно получить дополнительное понимание при обращении к некоторым конкретным примерам, которые представлены здесь только для иллюстрации, а не с целью ограничения, если не указано иного.
Пример 1
Получение 3,4-бис(4-метоксифенил)-6-фенилпиридазина
3,4-Бис(4-метоксифенил)-6-хлорпиридазин [Eur. J. Med. Chem.-Chimica Therapeutica, 14, 53-60 (1979)] (309,3 мг, 0,95 ммоль) растворяют в бензоле (2 мл). Добавляют последовательно тетракис(трифенилфосфин)палладий [Pd(Ph3P)4] (90,6 мг, 0,08 ммоль) и фенилмагнийбромид (1,0 М тетрагидрофурановый раствор) (1,5 мл) и далее перемешивают при 60°С в течение 75 мин. После добавления к реакционной смеси воды-метиленхлорида смесь экстрагируют метиленхлоридом и органический слой сушат над безводным сульфатом натрия. Растворитель отгоняют, а остаток отделяют и очищают хроматографией на колонке с силикагелем [силикагель (10 г), гексан/этилацетат (2/1)], при этом получают указанное в заголовке соединение в виде светло-желтого аморфного твердого вещества (129 мг, 36,9%).
1Н-ЯМР (CDCl3) δ: 3,83 (3Н, с), 3,84 (3Н, с), 6,86 (2Н, д, J=9,04 Гц), 6,90 (2Н, д, J=9,04 Гц), 7,22 (2Н, д, J=9,04 Гц), 7,45-7,55 (5Н, м), 7,79 (1Н, с), 8,15-8,20 (2Н, м).
ИК (пленка) см-1: 1609, 1514, 1392, 1252, 1178.
Пример 2
Получение 3,4-бис(4-метокс