Производные 4-фенилпиридина и лекарственное средство на их основе
Иллюстрации
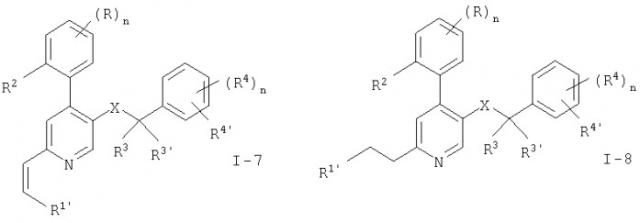
Показать всеДанное изобретение относится к новым производным 4-фенилпиридина общей формулы I
где R означает водород или галоид; R1 означает -(C≡C)mR1' или -(CR'=CR'')mR1', Х - означает -C(O)N(R8)-, -N(R8)C(O)- или -N(R8)-(CH2)p-, где m означает 0-4; а р означает 1-2; значения радикалов R1', R2', R3', R3, R4, R4', R8, R', R'' определены выше, к их фармацевтически приемлемыми кислотно-аддитивным солям и лекарственному средству на их основе. Новые соединения, являлась антагонистами нейрокинина-1, могут быть использованы в качестве лекарственных средств для лечения заболеваний, опосредованных действием рецептора нейрокинина-1. 2 н. и 11 з.п. ф-лы.
Реферат
Данное изобретение относится к соединениям общей формулы
где R означает водород или галоид;
R1 означает -(С≡С)mR1' или -(CR'=CR'')mR1',
где R1' означает
а) галоид,
б) циано или следующие группы:
в)
г) -C(O)NR'R'',
д) -C(O)O(CH2)mR5,
e) -C(O)R5,
ж) -N(OH)-(CH2)mR5,
з) -NR'C(O)-(CH2)mR5,
и) -N[C(O)-R']2,
к) -OR6,
л) -(CH2)m-SR6, -(CH2)m-S(O)R6 или -(CH2)m-S(O)2R6,
м) арил, необязательно замещенный одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'R'', нитро, -(CH2)nOR', -C(O)NR'R'', -C(O)OR' или -C(O)R',
н) пяти- или шестичленную гетероарильную группу, содержащую 1-4 гетероатома, выбранные из N, О или S, и может быть необязательно замещенной одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'R'', нитро, -(CH2)nOR', -C(O)OR', -C(O)NR'R'' или -C(O)R',
о) группировку пяти- или шестичленного насыщенного циклического третичного амина
которая может содержать один дополнительный гетероатом, выбранный из N, О или S,
R'/R'' означают независимо друг от друга водород, гидрокси, (низш.)алкил, циклоалкил или арил, где (низш.)алкил, циклоалкил или арильная группа могут быть необязательно замещены одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'''R'''', нитро, -(CH2)nOR''', -C(O)NR'''R'''', -C(O)OR''' или -C(O)R''',
R'''/R'''' означают независимо друг от друга водород, (низш.)алкил, циклоалкил или арил,
R5 означает водород, циано, гидрокси, галоид, трифторметил, -C(O)OR', -OC(O)R' или арил, необязательно замещенный одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'R'', нитро, -(CH2)nOR', -C(O)NR'R'', -C(O)OR' или -C(O)R', или означает пяти- или шестичленную гетероарильную группу, содержащую 1-4 гетероатома, выбранных из N, О или S, и может быть необязательно замещенной одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'R'', нитро, -(CH2)nOR', -C(O)NR'R'', -C(O)OR' или -C(O)R',
R6 означает водород, (низш.)алкил, трифторметил или арил, где (низш.)алкильная или арильная группа может быть необязательно замещенной одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'R'', нитро, -C(O)NR'R'', -(CH2)nOR', -C(O)OR' или -C(O)R', или означает пяти- или шестичленную гетероарильную группу, содержащую 1-4 гетероатома, выбранных из N, О или S, и может быть необязательно замещенной одним или несколькими заместителями, выбранными из галоида, трифторметила, (низш.)алкила, (низш.)алкокси, циано, гидрокси, -NR'R'', нитро, -(CH2)nOR', -C(O)NR'R'', -C(O)OR' или -C(O)R',
R7 означает -C(O)-(CH2)mOH или оксогруппу;
R2 означает водород, (низш.)алкил, (низш.)алкокси или CF3;
R3/R3' означают независимо друг от друга водород, (низш.)алкил или образуют вместе с атомом углерода, к которому они присоединены, циклоалкильную группу;
R4/R4' означают независимо друг от друга водород, галоид, CF3, (низш.)алкил или (низш.)алкокси;
R и R2 или R4 и R4' могут быть вместе группой -СН=СН-СН=СН-, необязательно замещенной одним или двумя заместителями, выбранными из (низш.)алкила, галоида или (низш.)алкокси;
Х означает -C(O)N(R8)-, (CH2)pО-, -(CH2)pN(R8)-, -N(R8)CO)- или -N(R8)-(СН2)p-;
где R8 означает водород или (низш.)алкил;
n означает 1 или 2;
m означает 0, 1, 2, 3 или 4;
о означает 1 или 2;
р означает 1 или 2;
и к их фармацевтически приемлемым кислотно-аддитивным солям.
Соединения формулы I и их соли отличаются тем, что имеют ценные терапевтические свойства. Неожиданно было обнаружено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина-1 (NK-1, вещества Р). Вещество Р представляет собой природный ундекапептид, принадлежащий к тахикининовому семейству пептидов, причем последние так названы благодаря их быстрому сократительному действию на ткань экстраваскулярной гладкой мышцы. Рецептором вещества Р является член огромного семейства рецепторов, сопряженных с G-белком.
Нейропептидный рецептор вещества Р (NK-1) широко распространен во всей нервной системе млекопитающих (особенно в головном мозгу и ганглиях позвоночника), в системе кровообращения и периферических тканях (особенно в двенадцатиперстной и в тощей кишке) и участвует в регуляции многих различных биологических процессов.
Центральное и периферическое действия тахикининового вещества Р млекопитающих ассоциированы с многочисленными воспалительными состояниями, включая мигрень, ревматоидный артрит, астму и воспалительные заболевания пищеварительного тракта, а также с опосредованием рвотного рефлекса и с нарушениями модуляции центральной нервной системы (ЦНС), такими как болезнь Паркинсона (Neurosci. Res., 1996, 7, 187-214), страх (Can. J. Phys., 1997, 75, 612-621) и депрессия (Science, 1998, 281, 1640-1645).
Доказательство полезности антагонистов тахикининовых рецепторов при боли, головной боли, особенно мигрени, болезни Альцгеймера, множественном склерозе, ослаблении синдрома отмены морфина, сердечно-сосудистых изменениях, отеке, таком как вызванный термическим повреждением, хронических воспалительных заболеваниях, таких как ревматоидный артрит, астме/бронхиальной гиперреактивности и других респираторных заболеваниях, включая аллергический ринит, воспалительных заболеваниях кишечника, включая язвенный колит и болезнь Крона, повреждении глаза и глазных воспалительных заболеваниях рассмотрено в публикации «Тахикининовый рецептор и антагонисты тахикининового рецептора», J. Auton. Pharmacol., 13, 23-93, 1993.
Кроме того, антагонисты рецептора нейрокинина-1 создавались для лечения множества физиологических нарушений, ассоциированных с избытком или дисбалансом тахикинина, особенно вещества Р. Примеры состояний, в которые вовлечено вещество Р, включают нарушения центральной нервной системы, такие как страх, депрессия и психоз (WO 95/16679, WO 95/18124 и WO 95/23798).
Помимо этого, антагонисты рецептора нейрокинина-1 применимы для лечения укачивания и индуцированной рвоты.
Кроме того, в публикации New England Journal of Medicine, 340 (3), 190-195 (1999) описано ослабление индуцированной цисплатином рвоты с помощью селективного антагониста рецептора нейрокинина-1.
Более того, в патенте US 5972938 описан способ лечения психоиммунологического или психосоматического нарушения путем введения тахикининового рецептора, такого как антагонист рецептора NK-1.
Затем применимость антагонистов рецептора нейрокинина-1 для лечения некоторых форм недержания мочи описана в Neuropeptides, 32 (1), 1-49 (1998) и в Eur. J. Pharmacol., 383 (3), 297-303 (1999),
Соединения формулы I могут также применяться в форме пролекарств. Примерами являются сложные эфиры, N-оксиды, фосфаты, гликоамидные сложные эфиры, глицеридные конъюгаты и тому подобное. Пролекарства могут увеличить преимущества данных соединений в адсорбции, фармакокинетике при распределении в мозге и транспорте в мозг.
Объектами настоящего изобретения являются соединения формулы I и их фармацевтически приемлемые соли, получение упомянутых выше соединений, содержащих их лекарственных средств и их изготовление, а также применение упомянутых выше соединений для контроля или предупреждения заболеваний, особенно заболеваний и нарушений упомянутого ранее типа, или в изготовлении соответствующих лекарственных средств.
Термин «(низш.)алкил», как он используется в контексте, означает насыщенную линейную или разветвленную алкильную группу, содержащую 1-7 атомов углерода, например метил, этил, пропил, изопропил, н-бутил, изобутил, 2-бутил, трет.-бутил и тому подобное. Предпочтительными (низш.)алкильными группами являются группы с 1-4 атомами углерода.
Термин «циклоалкил» означает насыщенную карбоциклическую группу, содержащую 3-6 атомов углерода.
Термин «галоид» означает хлор, йод, фтор или бром.
Термин «(низш.)алкокси» означает группу, в которой алкильная часть такая, как определено выше, и которая присоединена через атом кислорода.
Термин «пяти- или шестичленная гетероарильная группа, содержащая 1-4 гетероатома, выбранных из N, О или S» означает, например, следующие группы: пиррол-1-ил, имидазол-1 или -2-ил, пиразол-1-ил, пиридин-2, -3 или -4-ил, пиразинил, пиримидинил, пиридазинил, изотиазолил, изоксазолил, тиенил, 1,2,3-триазолил, 1,2,4-оксадиазолил, тетрагидропиридинил или фурил.
Термин «пяти- или шестичленный насыщенный циклический третичный амин» означает, например, пирролидинил, имидазолидинил, пиразолидинил, пиперидинил, пиперазинил, морфолинил, тиоморфолинил, тиоморфолин-1,1-диоксо или тиоорфолин-1-оксо.
Термин «арил» означает моноциклический ароматический углеводородный радикал или бициклическую либо трициклическую кольцевую систему, в которой, по меньшей мере, одно кольцо является ароматическим, предпочтительными являются фенильные, бензильные или нафтильные кольца.
Термин «фармацевтически приемлемые кислотно-аддитивные соли» охватывает соли с неорганическими и органическими кислотами, такими как хлористоводородная кислота, азотная кислота, серная кислота, фосфорная кислота, лимонная кислота, муравьиная кислота, фумаровая кислота, малеиновая кислота, уксусная кислота, янтарная кислота, винная кислота, метансульфоновая кислота, п-толуолсульфоновая кислота и тому подобное.
Наиболее предпочтительными показаниями по настоящему изобретению являются те, которые включают нарушения центральной нервной системы, например, лечение или предупреждение некоторых депрессивных нарушений или рвоты путем введения антагонистов рецептора NK-1. Основной депрессивный эпизод определен как период, по меньшей мере, в две недели, когда в течение большей части суток и почти каждый день наблюдается угнетенное настроение и потеря интереса или желания ко всем или почти всем видам деятельности.
Предпочтительными являются соединения формулы I, в которых Х означает -C(O)N(CH3)- и -(R4)n означает 3,5-ди-CF3. Примерами предпочтительных соединений данной группы являются те, в которых R3/R3' означают оба водород, и R2 означает метил, например, следующие соединения:
N-(3,5-бистрифторметилбензил)-6-(4-гидроксиацетилпиперазин-1-ил)-N-метил-4-о-толилникотинамид,
N-(3,5-бистрифторметилбензил)-6-хлор-N-метил-4-о-толилникотинамид,
N-(3,5-бистрифторметилбензил)-6-цианометил-N-метил-4-о-толилникотинамид,
N-(3,5-бистрифторметилбензил)-6-йод-N-метил-4-о-толилникотинамид,
(3,5-бистрифторметилбензил)метиламид 4-о-толил-[2,4']бипиридинил-5-карбоновой кислоты,
метиловый эфир 5-[(3,5-бистрифторметилбензил)метилкарбамоил]-4-о-толилпиридин-2-карбоновой кислоты,
N-(3,5-бистрифторметилбензил)-6-гидроксиметил-N-метил-4-о-толилникотинамид,
6-(5-ацетилтиофен-2-ил)-N-(3,5-бистрифторметилбензил)-N-метил-4-о-толилникотинамид,
(3,5-бистрифторметилбензил)метиламид 4-о-толил-1',2',3',6'-тетрагидро-[2,4']бипиридинил-5-карбоновой кислоты,
N-(3,5-бистрифторметилбензил)-6-(4-гидроксиметилфенил)-N-метил-4-о-толилникотинамид,
(3,5-бистрифторметилбензил)метиламид 2'-метил-4-о-толил-[2,4']бипиридинил-5-карбоновой кислоты,
N-(3,5-бистрифторметилбензил)-N-метил-6-(3-метил-[1,2,4]оксадиазол-5-ил)-4-о-толилникотинамид,
6-(3-аминопроп-1-инил)-N-(3,5-бистрифторметилбензил)-N-метил-4-о-толилникотинамид,
(RS)-N-(3,5-бистрифторметилбензил)-6-(2-гидроксиэтансульфинилметил)-N-метил-4-о-толилникотинамид,
N-(3,5-бистрифторметилбензил)-N-метил-6-(1-метил-1H-имидазол-2-илсульфанилметил)-4-о-толилникотинамид,
(RS)-N-(3,5-бистрифторметилбензил)-N-метил-6-(пиридин-2-сульфинил)-4-о-толилникотинамид,
N-(3,5-бистрифторметилбензил)-N-метил-6-(пиридин-2-сульфонил)-4-о-толилникотинамид или
N-(3,5-бистрифторметилбензил)-6-(3-гидроксипропокси)-N-метил-4-о-толилникотинамид.
Кроме того, предпочтительными являются соединения формулы I, где Х означает -N(СН3)С(O)- и -(R4)n означает 3,5-ди-CF3. Примерами предпочтительных соединений данной группы являются те, в которых R3/R3' означают оба метил, и R2 означает метил, например, следующие соединения:
2-(3,5-бистрифторметилфенил)-N-{6-[гидрокси-(2-гидроксиэтил)амино]-4-о-толилпиридин-3-ил}-N-метилизобутирамид,
2-(3,5-бистрифторметилфенил)-N-метил-N-[6-(3-оксоморфолин-4-ил)-4-о-толилпиридин-3-ил]изобутирамид,
(5-{[2-(3,5-бистрифторметилфенил)-2-метилпропионил]метиламино}-4-о-толилпиридин-2-илкарбамоил)метиловый эфир уксусной кислоты,
2-(3,5-бистрифторметилфенил)-N-[6-(2-гидроксиацетиламино)-4-о-толилпиридин-3-ил]-N-метилизобутирамид,
2-(3,5-бистрифторметилфенил)-N-[6-(гидроксиацетилметиламино)-4-о-толилпиридин-3-ил]-N-метилизобутирамид,
2-(3,5-бистрифторметилфенил)-N-[6-(2,5-диоксопирролидин-1-ил)-4-о-толилпиридин-3-ил]-N-метилизобутирамид,
(5-{[2-(3,5-бистрифторметилфенил)-2-метилпропионил]метиламино}-4-о-толилпиридин-2-ил)циклопропанкарбониламид циклопропанкарбоновой кислоты,
2-(3,5-бистрифторметилфенил)-N-(6-хлор-4-o-толилпиридин-3-ил)-N-метил-изобутирамид,
2-(3,5-бистрифторметилфенил)-N-[4-(2-хлорфенил)-2'-метил-[2,4']бипиридинил-5-ил]-N-метилизобутирамид,
2-(3,5-бистрифторметилфенил)-N-(6-этинил-4-о-толилпиридин-3-ил)-N-метил-изобутирамид,
2-(3,5-бистрифторметилфенил)-N-[6-(3-гидроксиметилизоксазол-5-ил)-4-о-толилпиридин-3-ил]-N-метилизобутирамид,
2-(3,5-бистрифторметилфенил)-N-[6-(3-гидроксипроп-1-инил)-4-о-толилпиридин-3-ил]-N-метилизобутирамид или
(RS)-2-(3,5-бистрифторметилфенил)-N-[6-(3-метоксибензолсульфинил)-4-о-толилпиридин-3-ил]-N-метилизобутирамид.
Кроме того, предпочтительными являются те соединения, в которых R3/R3' означают оба метил и R2 означает хлор, например, следующие соединения:
2-(3,5-бистрифторметилфенил)-N-{4-(2-хлорфенил)-6-[гидрокси-(2-гидроксиэтил)амино]пиридин-3-ил)-N-метилизобутир амид или
2-(3,5-бистрифторметилфенил)-N-[4-(2-хлорфенил)-6-(3-оксоморфолин-4-ил)пиридин-3-ил]-N-метилизобутирамид.
Данные соединения формулы I и их фармацевтически приемлемые соли могут быть получены способами, известными специалистам, например описанным ниже способом, который включает
(а) взаимодействие соединения формулы
с соединением формулы
с образованием соединения формулы
где R1-R4, R и n имеют приведенные выше значения, или
(б) взаимодействие соединения формулы
с соединением формулы
с образованием соединения формулы
где R1-R4, R и n имеют приведенные выше значения, или
(в) восстановление соединения формулы
в соединение формулы
где значения заместителей приведены выше, или
(г) взаимодействие соединения формулы
с соединением формулы
с образованием соединения формулы
где Z означает Cl, Br, I, -OS(O)2СН3 или -OS(O)2С6Н4СН3, и другие значения заместителей приведены выше, или
(д) взаимодействие соединения формулы
с соединением формулы
с образованием соединения формулы
где Z означает Cl, Br, I, -OS(O)2СН3 или -OS(O)2С6Н4СН3, и значения других заместителей приведены выше, или
(е) восстановление соединения формулы
в соединение формулы
где значения заместителей приведены выше, или
при необходимости превращение полученного соединения в фармацевтически приемлемую кислотно-аддитивную соль.
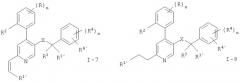
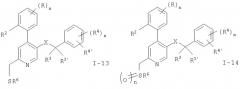
Кроме того, заместитель R1 может быть модифицирован в пределах приведенных выше значений, например, для следующих соединений формул I-2, I-4, I-5, I-7, I-8, I-10, I-11, I-12, I-13 или I-14:
взаимодействием соединения формулы
с соединением формулы R1' Н
с образованием соединения формулы
где заместители описаны выше, или
взаимодействием соединения формулы
с соединением формулы R6-Z
с образованием соединения формулы
где Z означает Cl, Br, I или -OS(O2)С6Н4СН3 или -OS(O2)СН3 и где остальные заместители описаны выше, или
взаимодействием соединения формулы
с R1'- Br или R1'- I с образованием соединения формулы
где заместители описаны выше, или
гидрированием соединения формулы
в соединения формул
или где заместители описаны выше, или
взаимодействием соединения формулы
с HNR'R'' с образованием соединения формулы
где заместители описаны выше, или
взаимодействием соединения формулы I-9 с LiBH4 с образованием соединения формулы
и при необходимости соединения
где заместители описаны выше, или
взаимодействием соединения формулы I-11 с R6SH с образованием соединений формул
или где заместители описаны выше.
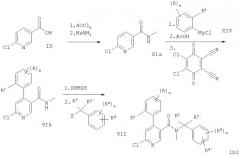
В соответствии с вариантом (а) способа получения прибавляют DIPEA (N-этилдиизопропиламин) к смеси соединения формулы II и соединения формулы III в дихлорметане, смесь перемешивают при температуре 25-40°С. Требуемое соединение формулы Ia после очистки выделяют с хорошим выходом.
Вариант (б) способа получения описывает реакцию соединения формулы IV с соединением формулы V с образованием соединения формулы Ib. Реакцию проводят общепринятым способом, например, в растворителе, таком как смесь толуола и триэтиламина. Смесь нагревают при кипении в течение примерно 1 ч.
В соответствии с вариантом (в) способа получения соединение формулы Ib восстанавливают в соединение формулы Ic. Данную реакцию проводят общепринятым способом с восстанавливающим агентом, таким как LiAlH4 или ВН3·ТГФ.
Вариант (г) способа получения описывает реакцию соединения формулы VI с соединением формулы VII, приводящую к образованию соединения формулы Ib. Данную реакцию проводят путем депротонирования соединения формулы VI с KHMDS (гексаметилдисилазидом калия) и последующего прибавления соединения формулы VII. Соответствующим растворителем является тетрагидрофуран. Реакцию проводят при комнатной температуре.
В соответствии с вариантом (д) получают соединение формулы Id. Данную реакцию проводят путем депротонирования соединения формулы VIII с NaH и последующего прибавления соединения формулы VII. Реакцию проводят общепринятым способом.
Другой способ получения соединения формулы I описан в варианте (е). Соединение формулы Ia восстанавливают в соединение формулы Ie общепринятым способом, например, с LiAlH4 или ВН3·ТГФ.
Солеобразование проводят при комнатной температуре известными по сути способами, которые знакомы любому специалисту в этой области. Рассматриваются не только соли с неорганическими кислотами, но также и соли с органическими кислотами. Примерами таких солей являются гидрохлориды, гидробромиды, сульфаты, нитраты, цитраты, ацетаты, малеаты, сукцинаты, метансульфонаты, п-толуолсульфонаты и тому подобное.
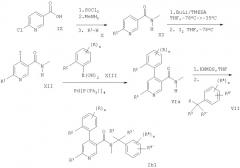
Следующие схемы 1-18 описывают способы получения соединений формулы Ia более подробно. Данные реакции проводят общепринятым способом в условиях, описанных на следующих схемах. Исходными веществами являются известные соединения или они могут быть получены способами, известными специалистам.
В схемах использованы следующие сокращения:
| PivCl | пивалоилхлорид |
| THF | тетрагидрофуран |
| TMEDA | N,N,N',N'-тетраметиленэтилендиамин |
| DIPEA | N-этилдиизопропиламин |
| KHMDS | гексаметилдисилазид калия |
| LDA | диизопропиламид лития |
| DPPA | дифенилфосфорилазид |
| EDC | гидрохлорид N-(3-диметиламинопропил)-N'-этилкарбодиимида |
| МСРВА | м-хлорнадбензойная кислота |
Схема 1
Z=Cl, Br, I или -OS(O2)С6Н4СН3 или -OS(O2)СН3
Заместители описаны выше.
Схема 2
Заместители имеют значения, описанные выше. R1' может быть тем же, что R1, за исключением хлора.
Схема 3
Заместители имеют значения, описанные выше. R1' может быть тем же, что R1, за исключением хлора.
Схема 4
Y=ОН, OR, вместе O(CR'R'')qO, R означает водород или (низш.)алкил, R1 и R6 описаны выше;
R',R''=H, CH3, q=2, 3,
или СО, НО(СН2)mR5 или H(C≡C)mR1'
и кат. (Pd, Ni, Cu), m, R5 и R1' описаны выше,
или
1) RMgCl, RMgBr, RMgl или R2Mg, где R означает (низш.)алкил;
2)
R5 описан выше;
Остальные заместители описаны выше.
Схема 5
Заместители описаны выше.
Схема 6
Заместители описаны выше.
Схема 7
Z=Cl, Br, I или OS(O)2C6H4CH3 или OS(O)2CH3
Заместители описаны выше.
Схема 8
Y может быть заместителем в пяти- или шестичленной гетероарильной группе, описанной по п. (н) для R1',
R1 является замещенным по п. (н) для R1,
R1' является незамещенным по п. (н) для R1.
Схема 9
R1' означает арильную или гетероарильную группу.
Схема 10
Заместители на схемах 8, 9 и 10 описаны выше.
Схема 11
Схема 13
Схема 14
Заместители имеют приведенные выше значения.
Схема 15
Заместители имеют приведенные выше значения.
Схема 16
Заместители имеют приведенные выше значения.
Схема 17
Заместители имеют приведенные выше значения.
Схема 18
Заместители имеют приведенные выше значения.
Как упоминалось ранее, соединения формулы I и их фармацевтически применимые аддитивные соли обладают ценными фармакологическими свойствами. Было найдено, что соединения по настоящему изобретению являются антагонистами рецептора нейрокинина-1 (NK-1, вещества Р).
Соединения исследовали в соответствии с тестами, приведенными в контексте.
Сродство исследуемых соединений к рецептору NK1 оценивали на человеческих рецепторах NK1 в клетках СНО (яичника китайского хомяка), инфицированных человеческим рецептором NK1 (используя экспрессионную систему вируса Semliki) и радиоактивно меченных с [3Н]-веществом Р (конечная концентрация 0.6 нМ). Анализы связывания проводили в буфере HEPES (50 мМ, рН 7,4), содержащем BSA (0.04%), лейпептин (8 мкг/мл), MnCl2 (3 мМ) и фосфоамидон (2 мкМ). Анализ связывания включал 250 мкл мембранной суспензии (1,25×10 клеток/пробирку для анализа), 0,125 мкл буфера замещающего агента и 125 мкл [3H]-вещества Р. Кривые замещения измеряли, по меньшей мере, с семью концентрациями соединения. Пробирки для анализа инкубировали в течение 60 мин при комнатной температуре, после чего содержимое пробирок быстро фильтровали в вакууме через фильтры GF/C, предварительно пропитанные в течение 60 мин PEI (полиэтиленимином) (0.3%) с промыванием (2×2 мл) буфером HEPES (50 мМ, рН 7,4). Радиоактивность, удержанную на фильтрах, измеряли с помощью сцинтилляционного счета. Все анализы проводили трижды, по меньшей мере, в 2 отдельных экспериментах.
Сродство предпочтительных соединений к рецептору NK-1, выраженное в виде pKI, для описываемых соединений находится в диапазоне 8,50-9,50.
| № примера | PKI |
| 8 | 9,29 |
| 13 | 8,79 |
| 16 | 8,5 |
| 26 | 8,65 |
| 38 | 8,67 |
| 42 | 9,08 |
| 62 | 8,52 |
| 66 | 8,57 |
| 99 | 8,58 |
| 113 | 8,78 |
Соединения формулы I, а также их фармацевтически приемлемые кислотно-аддитивные соли могут применяться в качестве лекарственных средств, например в виде фармацевтических препаратов. Фармацевтический препарат может вводиться перорально, например в виде таблеток, таблеток с покрытием, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий. Однако введение может осуществляться ректально, например в виде суппозиториев, или парентерально, например в виде инъекционных растворов.
Для получения таблеток, таблеток с покрытием, драже и твердых желатиновых капсул соединения формулы I и их фармацевтически приемлемые кислотно-аддитивные соли могут подвергаться обработке с фармацевтически инертными неорганическими или органическими наполнителями. Лактоза, кукурузный крахмал или их производные, тальк, стеариновая кислота или ее соли могут применяться в качестве таких наполнителей, например, для таблеток, драже и твердых желатиновых капсул.
Соответствующими наполнителями для мягких желатиновых капсул являются, например, растительные масла, воск, жиры, полутвердые и жидкие полиолы и т.д.
Соответствующими наполнителями для получения растворов и сиропов являются, например, вода, полиолы, сахароза, инвертный сахар, глюкоза и т.д.
Соответствующими наполнителями для инъекционных растворов, являются, например, вода, спирты, полиолы, глицерин, растительные масла и т.д.
Соответствующими наполнителями для суппозиториев являются, например, природные или затвердевшие масла, воск, жиры, полутвердые или жидкие полиолы и т.д.
Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие агенты, эмульгаторы, подсластители, красители, ароматизаторы, соли для изменения осмотического давления, буферы, маскирующие агенты или антиоксиданты. Они могут содержать и другие терапевтически ценные вещества.
Дозы могут меняться в широком диапазоне и, безусловно, будут соответствовать индивидуальным требованиям в каждом отдельном случае. В общем, в случае перорального введения должна быть принята суточная доза примерно 10-1000 мг на пациента соединения общей формулы I, хотя при необходимости приведенный верхний предел может быть также превышен.
Следующие примеры иллюстрируют настоящее изобретение без ограничений. Все температуры даны в °С. Соединения 39, 54, 65, 81, 83, 92, 108, 109, 117 и 118 выходят за пределы приведенной формулы I.
Пример 1
N-(3,5-Бистрифторметилбензил)-6-(4-гидроксиацетилпиперазин-1-ил)-N-метил-4-о-толилникотинамид
(а) 6-Хлор-N-метилникотинамид
К 50 г (317 ммолей) 2-хлорникотиновой кислоты прибавляли 230 мл (3,16 ммоля) тионилхлорида при 0°С. После нагревания смеси при кипении в течение 2 ч избыток тионилхлорида удаляли перегонкой. Маслянистый коричневый остаток растворяли в 250 мл дихлорметана, раствор обрабатывали газообразным метиламином при 0°С до прекращения экзотермической реакции. Полученную суспензию разбавляли 1000 мл смеси дихлорметан/вода. Слои разделяли, водный слой экстрагировали 3×300 мл дихлорметана. Высушивание органического слоя сульфатом натрия и упаривание дали 53,2 г (98%) заглавного соединения в виде светло-желтого твердого вещества.
МС (m/z, %): 171 [(М+Н)+ 15].
(б) 6-Хлор-N-метил-4-о-толилникотинамид
К раствору 3,41 г (20,0 ммолей) 6-хлор-N-метилникотинамида в 80 мл тетрагидрофурана прибавляли при 0°С 50 мл (50 ммолей) 1 М раствора о-толилмагнийхлорида в тетрагидрофуране. По окончании прибавления реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 1,5 ч. Смесь снова охлаждали до 0°С, затем прибавляли по каплям 5,7 мл (100 ммолей) уксусной кислоты и раствор 5,1 г (22 ммоля) 2,3-дихлор-5,6-циано-1,4-бензохинона в 18 мл тетрагидрофурана. По завершении прибавления реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение 15 мин. После прибавления 30 мл 2 н. водного раствора гидроксида натрия разбавляли 1 л этилацетата и 200 мл воды. Слои разделяли, органический слой промывали 4×250 мл 2 н. водного раствора гидроксида натрия. Объединенные водные слои экстрагировали 3×500 мл этилацетата. Объединенные органические экстракты промывали насыщенным водным раствором хлористого натрия и сушили сульфатом натрия. Концентрирование дало 5,44 г красно-коричневого масла. Колоночная флэш-хроматография дала 2,15 г (43%) заглавного соединения в виде светло-желтого твердого вещества.
МС (m/z, %): 260 (М+, 11); tпл 91-93°C.
(в) трет.-Бутиловый эфир 4-(5-метилкарбамоил-4-о-толилпиридин-2-ил)пиперазин-1-карбоновой кислоты
Смесь 8,31 г (31,9 ммоля) 6-хлор-N-метил-4-о-толилникотинамида, 6,53 г (35,0 ммолей) 1-трет.-бутоксикарбонилпиперазина, 16,7 мл (95,6 ммоля) N-этилдиизопропиламина и каталитического количества 4-(N,N-диметиламино)пиридина нагревали при кипении в течение ночи. После охлаждения до комнатной температуры смесь растворяли в дихлорметане и дважды промывали 0,1 М водным раствором хлористоводородной кислоты. Высушивание сульфатом натрия и концентрирование дали 10,7 г неочищенного продукта. Флэш-хроматография дала 6,28 г (48,0%) заглавного соединения в виде не совсем белого твердого вещества.
МС (m/z, %): 260 [(М+Н)+, 100].
(г) трет.-Бутиловый эфир 4-{5-[(3,5-бистрифторметилбензил)метилкарбамоил]-4-о-толилпиридин-2-ил}пиперазин-1-карбоновой кислоты
К раствору 6,28 г (15,3 ммоля) трет.-бутилового эфира 4-(5-метилкарбамоил-4-о-толилпиридин-2-ил)пиперазин-1-карбоновой кислоты в 250 мл тетрагидрофурана прибавляли 20 мл 1 М раствора (20 ммолей) гексаметилдисилазида калия в тетрагидрофуране при 0°С. Через 30 мин прибавляли по каплям 2,81 мл (15,3 ммоля) 3,5-бис(трифторметил)бензилбромида. Реакционной смеси давали нагреться до комнатной температуры в течение ночи. После добавления воды и 1 М водного раствора гидроксида натрия экстрагировали тремя порциями этилацетата. Объединенные органические экстракты сушили сульфатом натрия и концентрировали. Флэш-хроматография дала 6,89 г (70,8%) заглавного соединения в виде белого твердого вещества.
МС (m/z, %): 637 [(М+Н)+, 100].
(д) N-(3,5-Бистрифторметилбензил)-N-метил-6-пиперазин-1-ил-4-о-толилникотинамид
К раствору 6,60 г (104 ммоля) трет.-бутилового эфира 4-{5-[(3,5-бистрифторметилбензил)метилкарбамоил]-4-о-толилпиридин-2-ил}пиперазин-1-карбоновой кислоты и 8,40 мл (207 ммолей) метанола в 50 мл этилацетата прибавляли 14,7 мл (207 ммолей) ацетилхлорида при 0°С. Через 4 ч реакционную смесь разбавляли этилацетатом и обрабатывали 1 М раствором гидроксида натрия. Слои разделяли, водный слой экстрагировали дихлорметаном. Объединенные органические слои сушили сульфатом натрия и концентрировали, получая 5,36 г неочищенного продукта. Флэш-хроматография дала 4,86 г (87,4%) заглавного соединения в виде светло-коричневого твердого вещества.
МС (m/z, %): 537 [(М+Н)+, 100].
(е) N-(3,5-Бистрифторметилбензил)-6-(4-бромацетилпиперазин-1-ил)-N-метил-4-о-толилникотинамид
К раствору 0,30 г (0,56 ммоля) N-(3,5-бистрифторметилбензил)-N-метил-6-пиперазин-1-ил-4-о-толилникотинамида в 4 мл дихлорметана прибавляли по каплям последовательно 0,055 мл (0,62 ммоля) бромацетилбромида и 4 мл 2 М водного раствора карбоната натрия при 10°С. Через 2 ч реакционную смесь разбавляли водой и экстрагировали дихлорметаном. Органический экстракт сушили сульфатом натрия и концентрировали, получая 0,36 г неочищенного продукта. Флэш-хроматография дала 0,26 г (89%) заглавного соединения в виде белого твердого вещества.
МС (m/z, %): 657 [(М+Н)+ 100, 1 Br].
(ж) N-(3,5-Бистрифторметилбензил)-6-(4-гидроксиацетилпиперазин-1-ил)-N-метил-4-о-толилникотинамид
Смесь 0,12 г (0,18 ммоля) N-(3,5-бистрифторметилбензил)-6-(4-бромацетилпиперазин-1-ил)-N-метил-4-о-толилникотинамида, 1,2 мл 1-метил-2-пирролидона и 0,2 мл полунасыщенного водного раствора бикарбоната натрия перемешивали при 100° в течение ночи. После охлаждения до комнатной температуры и разбавления водой смесь экстрагировали пятью порциями трет.-бутилметилового эфира. Объединенные органические экстракты сушили сульфатом натрия, концентрировали и сушили в вакууме (0,5 мбар) при 70°С. Флэш-хроматография дала 71 мг (64%) заглавного соединения в виде белого твердого вещества.
МС (m/z, %): 595 [(М+Н)+, 100].
Пример 2
N-(3,5-Бистрифторметилбензил)-6-хлор-N-метил-4-о-толилникотинамид
К раствору 10,0 г (38,4 ммоля) 6-хлор-N-метил-4-о-толилникотинамида в 190 мл тетрагидрофурана прибавляли при 0°С 46 мл 1 М раствора (46 ммолей) гексаметилдисилазида калия в тетрагидрофуране. Через 30 мин к образующейся суспензии по каплям прибавляли 8,5 мл (46 ммолей) 3,5-би(трифторметил)-бензилбромида. По завершении прибавления охлаждающую баню со смесью льда и воды убирали, реакционной смеси давали нагреться до комнатной температуры. Через 2 ч реакцию прекращали добавлением воды. Доводили рН смеси до 3 с 1 М водным раствором хлористоводородной кислоты и перемешивали в течение 10 мин. Подщелачивание с 1 М водным раствором гидроксида натрия до рН 8 предшествовало концентрированию для удаления тетрагидрофурана. Водный остаток экстрагировали четырьмя порциями дихлорметана. Объединенные органические экстракты сушили сульфатом натрия и концентрировали, получая 21,4 г неочищенного продукта. Колоночная хроматография дала 18,4 г (98,5%) заглавного соединения в виде белого твердого вещества.
МС (m/z, %): 485 [(М-Н)+, 2].
Пример 3
N-(3,5-Бистрифторметилбензил)-6-цианометил-N-метил-4-о-толилникотинамид
(а) Этиловый эфир (RS)-{5-[(3,5-бистрифторметилбензил)метилкарбамоил]-4-о-толилпиридин-2-ил}циануксусной кислоты
Смесь 1,00 г (2,05 ммоля) N-(3,5-бистрифторметилбензил)-6-хлор-N-метил-4-о-толилникотинамида, 0,44 мл (4,1 ммоля) этилового эфира циануксусной кислоты и 0,46 г (4, 1 ммоля) трет.-бутилата калия в 2 мл диметилсульфоксида перемешивали при 100°С в течение ночи. После охлаждения до комнатной температуры прибавляли 10 мл полунасыщенного водного раствора хлористого аммония. Смесь экстрагировали 3 порциями этилацетата. Объединенные органические экстракты промывали двумя порциями воды, сушили сульфатом натрия и концентрировали, получая 1,2 г неочищенного продукта. Флэш-хроматография дала 0,681 г (58,8%) заглавного соединения в виде желтой пены.
МС (m/z, %): 563 (М+, 80).
(б) N-(3,5-Бистрифторметилбензил)-6-цианометил-N-метил-4-о-толилникотинамид
Смесь 650 мг (1,15 ммоля) этилового эфира (RS)-{5-[(3,5-бистрифторметилбензил)метилкарбамоил]-4-о-толилпиридин-2-ил}циануксусной кислоты и 0,20 г (4,6 ммоля) хлористого лития во влажном диметилсульфоксиде перемешивали при 120°С в течение ночи. Пос