Способ получения альфа-l-аспартил-l-фенилаланин-бета-эфира и способ получения альфа-l-аспартил-l-фенилаланин-альфа-метилового эфира
Иллюстрации
Показать всеИзобретение относится к области биотехнологии и может быть использовано в пищевой промышленности. Предложен способ ферментативного получения α-L-аспартил-L-фенилаланин-β-эфира (α-L-(β-о-замещенный аспартил)-L-фенилаланин) из α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина при 5-40°С и рН 7-10 в течение времени, достаточного для образования α-L-аспартил-L-фенилаланин-β-эфира из α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина. Указанный способ используют в способе получения α-L-аспартил-L-фенилаланин-α-метилового эфира, включающего стадию синтеза α-L-аспартил-L-фенилаланин-β-метилового эфира и стадию превращения указанного эфира в α-L-аспартил-L-фенилаланин-α-метиловый эфир. Применение изобретения обеспечивает получение α-L-аспартил-L-фенилаланин-β-эфира с последующим получением α-L-аспартил-L-фенилаланин-α-метилового эфира по упрощенной и дешевой схеме с повышенным выходом. 2 н. и 3 з.п. ф-лы, 1 ил., 4 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к способу получения α-L-аспартил-L-фенилаланин-β-эфира (также называемого "α-L-(β-o-замещенный аспартил)-L-фенилаланин" (сокращение: α-ARP)) и к способу получения α-L-аспартил-L-фенилаланин-α-метилового эфира (также называемого "α-L-аспартил-L-фенилаланин метилового эфира (сокращение: α-APM). Более конкретно, настоящее изобретение относится к способу получения α-L-аспартил-L-фенилаланин-β-эфира, который является важным промежуточным продуктом для получения α-L-аспартил-L-фенилаланин-α-метилового эфира (название продукта: аспартам), который пользуется большим спросом в качестве подсластителя, и к способу получения α-L-аспартил-L-фенилаланин-α-метилового эфира, используя способ получения α-L-аспартил-L-фенилаланин-β-эфира.
Предшествующий уровень техники
Общеизвестные способы получения α-L-аспартил-L-фенилаланин-α-метилового эфира (далее здесь "α-APM" для сокращения в некоторых случаях) включают способ химического синтеза и способ ферментативного синтеза. Что касается способа химического синтеза, то известен способ конденсации N-защищенного ангидрида L-аспарагиновой кислоты с метиловым эфиром L-фенилаланина с получением N-защищенного APM и удаления N-защитной группы с получением APM, а что касается способа ферментативного синтеза, то известен способ конденсации N-защищенной L-аспарагиновой кислоты с метиловым эфиром L-фенилаланина с получением N-защищенного APM и удаления N-защитной группы с получением APM. В обоих способах, однако, необходимы стадии введения и удаления защитной группы, и процессы являются очень затруднительными. С другой стороны, был разработан способ получения APM без использования N-защитной группы (смотри патентную публикацию Японии № H02-015196 Gazette). Однако этот способ не подходит для промышленного получения из-за очень низкого выхода продукта. Таким образом, в связи с этим желательно разработать недорогой способ промышленного получения аспартама.
Раскрытие изобретения
Целью настоящего изобретения является простой недорогой способ получения α-L-аспартил-L-фенилаланин-β-эфира, который является промежуточным продуктом α-L-аспартил-L-фенилаланин-α-метилового эфира, обеспечивающий высокий выход, не используя сложный способ синтеза. Кроме того, целью настоящего изобретения является разработка простого недорогого способа получения α-L-аспартил-L-фенилаланин-α-метилового эфира, обеспечивающего высокий выход.
В результате проведенных исследований в отношении вышеуказанных целей изобретателями настоящего изобретения было обнаружено, что недавно открытый фермент или вещество, содержащее фермент, способны к избирательному синтезу α-L-аспартил-L-фенилаланин-β-эфира из α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина, что и привело к осуществлению настоящего изобретения.
Конкретно, настоящее изобретение описано ниже.
[1] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенный аспартил)-L-фенилаланина), включающий получение α-L-аспартил-L-фенилаланин-β-эфира из α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина с помощью фермента или содержащего фермент вещества, которые способны избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[2] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [1] выше, где фермент или содержащее фермент вещество представляют собой один или два или несколько типов, выбранных из группы, включающей культуру микроорганизма, который обладает способностью избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь, клетку микроорганизма, выделенную из культуры, и обработанного продукта микроорганизмом клетки микроорганизма.
[3] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2] выше, в котором микроорганизм представляет собой микроорганизм, принадлежащий к роду, выбранному из группы, включающей Aeromonas, Azotobacter, Alcaligenes, Brevibacterium, Corynebacterium, Escherichia, Empedobacter, Flavobacterium, Microbacterium, Propionibacterium, Brevibacillus, Paenibacillus, Pseudomonas, Serratia, Stenotrophomonas, Sphingobacterium, Streptomyces, Xanthomonas, Williopsis, Candida, Geotrichum, Pichia, Saccharomyces, Torulaspora, Cellulophaga, Weeksell, Pedobacter, Persicobacter, Flexithrix, Chitinophaga, Cyclobacterium, Runella, Thermonema, Psychroserpens, Gelidibacter, Dyadobacter, Flammeovirga, Spirosoma, Flectobacillus, Tenacibaculum, Rhodotermus, Zobellia, Muricauda, Salegentibacter, Taxeobacter, Cytophaga, Marinilabilia, Lewinella, Saprospira, и Haliscomenobacter.
[4] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2] выше, где микрорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (A) или (B):
(A) белок с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 23 по 616 аминокислотной последовательности, представленной в SEQ ID NO: 6 перечня последовательностей,
(B) белок с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с 23 по 616 аминокислотной последовательности, представленной в SEQ ID NO: 6 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[5] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2], где микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (C) или (D):
(C) белок с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 21 по 619 аминокислотной последовательности, представленной в SEQ ID NO: 12 перечня последовательностей,
(D) белок с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с 21 по 619 аминокислотной последовательности, представленной в SEQ ID NO: 12 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[6] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (E) или (F), ниже:
(E) белок с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 23 по 625 аминокислотной последовательности, представленной в SEQ ID NO: 18 перечня последовательностей,
(F) белок с аминокислотной последовательностью, включающей замену, делецию, исерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с 23 по 625 аминокислотной последовательности, представленной в SEQ ID NO: 18 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[7] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2] выше, в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (G) или (H), ниже:
(G) белок с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 23 по 645 аминокислотной последовательности, представленной в SEQ ID NO: 23 перечня последовательностей,
(H) белок с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с 23 по 645 аминокислотной последовательности, представленной в SEQ ID NO: 23 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[8] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (I) или (J), ниже:
(I) белок с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 26 по 620 аминокислотной последовательности, представленной в SEQ ID NO: 25 перечня последовательностей,
(J) белок с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с 26 по 620 аминокислотной последовательности, представленной в SEQ ID NO: 25 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[9] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2] выше, в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (K) или (L), ниже:
(K) белок с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 18 по 644 аминокислотной последовательности, представленной в SEQ ID NO: 27 перечня последовательностей,
(L) белок с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с 18 по 644 аминокислотной последовательности, представленной в SEQ ID NO: 27 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[10] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (M) или (N), ниже:
(M) белок с аминокислотной последовательностью, представленной в SEQ ID NO: 6 перечня последовательностей,
(N) белок, содержащий область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 6 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[11] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (O) или (P), ниже:
(O) белок с аминокислотной последовательностью, представленной в SEQ ID NO: 12 перечня последовательностей,
(P) белок, содержащий область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 12 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[12] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно п.[2], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (Q) или (R), ниже:
(Q) белок, содержащий область зрелого белка с аминокислотной последовательностью, представленной в SEQ ID NO: 18 перечня последовательностей,
(R) белок с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 18 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[13] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [3], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (S) или (T), ниже:
(S) белок с аминокислотной последовательностью, представленной в SEQ ID NO: 23 перечня последовательностей,
(T) белок, содержащий область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 23 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[14] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2], в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (U) или (V), ниже:
(U) белок с аминокислотной последовательностью, представленной в SEQ ID NO: 25 перечня последовательностей,
(V) белок, содержащий область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 25 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[15] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [2] выше, в котором микроорганизм представляет собой трансформированный микроорганизм, который способен экспрессировать белок (W) или (X), ниже:
(W) белок с аминокислотной последовательностью, представленной в SEQ ID NO: 27 перечня последовательностей,
(X) белок, содержащий область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 27 перечня последовательностей, и способный избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[16] Способ получения α-L-аспартил-L-фенилаланин-β-эфира (т.е. α-L-(β-o-замещенного аспартил)-L-фенилаланина) согласно [1] выше, в котором фермент является, по меньшей мере, одним из белков, выбранных из группы, включающей (A)-(X), ниже:
(A) белка с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 23 по 616 аминокислотной последовательности, представленной в SEQ ID NO: 6 перечня последовательностей,
(B) белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с номерами от 23 по 616 аминокислотной последовательности, представленной в SEQ ID NO: 6 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(C) белка с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 21 по 619 аминокислотной последовательности, представленной в SEQ ID NO: 12 перечня последовательностей,
(D) белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с номерами от 21 по 619 аминокислотной последовательности, представленной в SEQ ID NO: 12 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(E) белка с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 23 по 625 аминокислотной последовательности, представленной в SEQ ID NO: 18 перечня последовательностей,
(F) белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с номерами от 23 по 625 аминокислотной последовательности, представленной в SEQ ID NO: 18 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(G) белка с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 23 по 645 аминокислотной последовательности, представленной в SEQ ID NO: 23 перечня последовательностей,
(H) белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с номерами от 23 по 645 аминокислотной последовательности, представленной в SEQ ID NO: 23 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(I) белка с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 26 по 620 аминокислотной последовательности, представленной в SEQ ID NO: 25 перечня последовательностей,
(J) белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с номерами от 26 по 620 аминокислотной последовательности, представленной в SEQ ID NO: 25 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(K) белка с аминокислотной последовательностью, состоящей из аминокислотных остатков с номерами от 18 по 644 аминокислотной последовательности, представленной в SEQ ID NO: 27 перечня последовательностей,
(L) белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, состоящей из аминокислотных остатков с номерами от 18 по 644 аминокислотной последовательности, представленной в SEQ ID NO: 27 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(M) белка с аминокислотной последовательностью, представленной в SEQ ID NO: 6 перечня последовательностей,
(N) белка, содержащего область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 6 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(O) белка с аминокислотной последовательностью, представленной в SEQ ID NO: 12 перечня последовательностей,
(P) белка, содержащего область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 12 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(Q) белка с аминокислотной последовательностью, представленной в SEQ ID NO: 18 перечня последовательностей,
(R) белка, содержащего область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 18 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(S) белка с аминокислотной последовательностью, представленной в SEQ ID NO: 23 перечня последовательностей,
(T) белка, содержащего область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 23 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(U) белка с аминокислотной последовательностью, представленной в SEQ ID NO: 25 перечня последовательностей,
(V) белка, содержащего область зрелого белка с аминокислотной последовательностью, включающей замену, делецию, инсерцию, добавление и/или инверсию одной или множества аминокислот в аминокислотной последовательности, представленной в SEQ ID NO: 25 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь,
(W) белка с аминокислотной последовательностью, представленной в SEQ ID NO: 27 перечня последовательностей, и
(X) белка, содержащего область зрелого белка, с аминокислотной последовательностью в аминокислотной последовательности, представленной в SEQ ID NO: 27 перечня последовательностей, и способного избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь.
[17] Способ получения α-L-аспартил-L-фенилаланин-α-метилового эфира (т.е. метилового эфира α-L-аспартил-L-фенилаланина), включающий: реакционную стадию синтеза α-L-аспартил-L-фенилаланин-β-метилового эфира (называемого также α-L-(β-о-метиласпартил)-L-фенилаланин (сокращение: α-AMP) c помощью способа получения α-L-аспартил-L-фенилаланин-β-эфира согласно любому из пунктов 1-16; и реакционную стадию преобразования α-L-аспартил-L-фенилаланин-β-метилового эфира (т.е. α-L-(β-о-метиласпартил)-L-фенилаланин) в α-L-аспартил-L-фенилаланин-α-метиловый эфир.
α-L-аспартил-L-фенилаланин-β-эфир может быть легко получен с помощью настоящего изобретения. α-L-аспартил-L-фенилаланин-β-эфир может быть легко получен и иметь высокий выход наряду со сниженным использованием сложных способов синтеза, таких как введение/удаление защитных групп с помощью способа настоящего изобретения.
Более того, с помощью настоящего изобретения α-L-аспартил-L-фенилаланин-α-метиловый эфир может быть легко получен и может иметь высокий выход при минимуме затрат.
Другие объекты, особенности и преимущества настоящего изобретения будут подробно описаны или станут очевидны из нижеследующего описания, сопровождающегося фигурами.
Краткое описание фигуры
На чертеже представлена диаграмма, отражающая количество ферментов, которое существует в цитоплазматической фракции (Cy) и фракции периплазмы (Pe).
Наилучший вариант осуществления изобретения
Далее настоящее изобретение будет описано в следующем порядке
<1> Способ получения α-L-аспартил-L-фенилаланин-β-эфира
1. Способ получения α-L-аспартил-L-фенилаланин-β-эфира
2. Микроорганизмы, используемые в настоящем изобретении
3. Ферменты, используемые в настоящем изобретении; и
<2> Способ получения α-L-аспартил-L-фенилаланин-α-метилового эфира.
<1> Способ получения α-L-аспартил-L-фенилаланин-β-эфира
1. Способ получения α-L-аспартил-L-фенилаланин-β-эфира
В способе получения α-L-аспартил-L-фенилаланин-β-эфира по настоящему изобретению (называемом здесь также «способом получения пептида по настоящему изобретению») L-фенилаланин и α,β-диэфир L-аспарагиновой кислоты взаимодействуют в присутствии фермента, обладающего известной пептид-образующей активностью. То есть способ получения пептида по настоящему изобретению заключается в том, что α-L-аспартил-L-фенилаланин-β-эфир образуется из α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина с помощью фермента или содержащего фермент вещества, способных избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты через пептидную связь. Фермент или содержащее фермент вещество, способные избирательно присоединять L-фенилаланин к α-эфирному участку α,β-диэфира L-аспарагиновой кислоты, относятся к ферменту или содержащему фермент веществу, обладающим способностью или активностью катализировать реакцию, в которой по существу L-фенилаланин не способен осуществлять нуклеофильное воздействие на β-эфирный участок α,β-диэфира L-аспарагиновой кислоты, но осуществляет нуклеофильное воздействие только на его α-эфирный участок. Как показано здесь ниже в ссылочном примере, однако, получены также фермент или содержащее фермент вещество, которые обладают способностью катализировать реакцию, в которой по существу L-фенилаланин не способен осуществлять воздействие на α-эфирный участок α,β-диэфира L-аспарагиновой кислоты, но осуществляет нуклеофильное воздействие только на его β-эфирный участок в отличие от указанной выше способности, и что дает β-L-аспартил-L-фенилаланин-α-эфир (называемый также β-L-(α-o-замещенный аспартил)-L-фенилаланин (сокращение: β-ARP) из α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина.
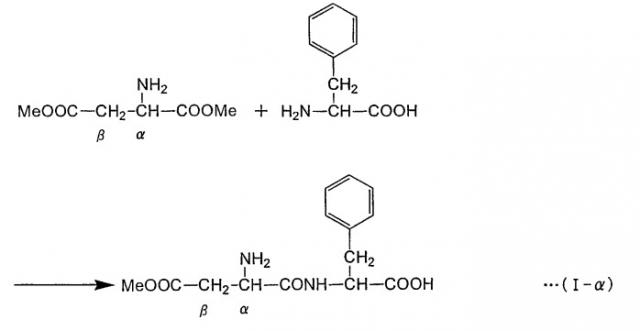
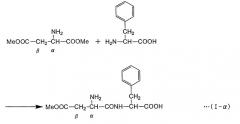
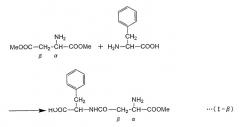
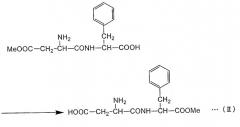
Формула реакции, в которой L-фенилаланин осуществляет нуклеофильное воздействие на α-эфирный участок α,β-диэфира L-аспарагиновой кислоты с получением α-L-аспартил-L-фенилаланин-β-эфира (сокращение: α-ARP), представлена в нижеследующей формуле (I-α) (где "Me" представляет собой метильную группу) путем цитирования случая, в котором в качестве α,β-диэфира L-аспарагиновой кислоты применяют α,β-диметиловый эфир L-аспарагиновой кислоты. Как показано в формуле (I-α), в способе получения пептида по настоящему изобретению аминогруппа L-фенилаланина взаимодействует с α-метиловым эфирным участком α,β-диметилового эфира L-аспарагиновой кислоты с образованием пептидной связи. С другой стороны, в нижепредставленной формуле (I-β) указана реакция, в которой β-метиловый эфирный участок α,β-диметилового эфира L-аспарагиновой кислоты подвергается нуклеофильному воздействию с образованием β-L-аспартил-L-фенилаланин-α-метилового эфира (называемого также β-L-(α-o-метил-аспартил)-L-фенилаланин (сокращение: β-AMP)). Пептидная связь в β-AMP образуется по β-метиловому эфирному участку α,β-диметилового эфира L-аспарагиновой кислоты. Фермент или содержащее фермент вещество, использующиеся в настоящем изобретении, ускоряют по существу только реакцию, как в формуле (I-α), но по существу не вызывают реакции как в формуле (I-β). α-APM может быть получен из α-AMP через простую стадию реакции (формула (II)), но α-APM не может быть получен непосредственно из β-AMP. Таким образом, способ по настоящему изобретению крайне эффективен в качестве способа получения промежуточного продукта α-APM и может использоваться для промышленного получения.
Формула реакции I-α
Формула реакции I-β
Формула реакции II
Способ, позволяющий ферменту или содержащему фермент веществу взаимодействовать с α,β-диэфиром L-аспарагиновой кислоты и L-фенилаланином, может быть осуществлен путем смешивания фермента или содержащего фермент вещества с α,β-диэфиром L-аспарагиновой кислоты и L-фенилаланином. Более конкретно, может быть использован способ, в котором фермент или содержащее фермент вещество добавляют к раствору, содержащему диэфир L-аспарагиновой кислоты и L-фенилаланин для воздействия на реакцию. Когда используют микроорганизм в качестве содержащего фермент вещества, который продуцирует фермент, реакция может быть осуществлена либо как описано выше, либо может быть использован способ, который включает культивирование микроорганизма, который продуцирует фермент для получения и аккумуляции фермента в микроорганизме или культуральной жидкости, в которой культивируется микроорганизм, и добавление к культуральной жидкости α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина, или сходный с ним способ. Полученный таким образом α-L-аспартил-L-фенилаланин-β-эфир выделяют общепринятым способом, и, при необходимости, он может быть очищен.
«Содержащее фермент вещество» может быть любым веществом, если оно содержит фермент, и конкретные его типы включают культуру микроорганизма, который продуцирует фермент, клетку микроорганизма, выделенную из культуры, и обработанный продукт клетки микроорганизма. Под культурой микроорганизма подразумевают вещество, полученное путем культивирования микроорганизма, и, конкретно, смесь клеток микроорганизма, среды, используемой для культивирования микроорганизма, и вещества, продуцируемого культивируемым микроорганизмом, и так далее. Кроме того, клетка микроорганизма может быть очищена для применения в качестве очищенной клетки микроорганизма. Более того, обработанный продукт клетки микроорганизма включает продукты, которые получают путем разрушения, лизиса или замораживания-оттаивания клетки микроорганизма и дальнейшего восстановления неочищенного фермента путем обработки клетки микроорганизма, и очистки фермента путем дальнейшей очистки. В качестве фермента, обработанного для очистки, может быть применен частично очищенный фермент, полученный с помощью различных способов очистки и так далее. Кроме того, могут быть использованы иммобилизованные ферменты, которые иммобилизованы с помощью метода образования ковалентных связей, метода адсорбции, метода улавливания и так далее. Кроме того, в случае некоторых используемых микроорганизмов часть клеток микроорганизма может подвергаться лизису в процессе культивирования и в таком случае в качестве содержащего фермент вещества также может быть использован супернатант культуральной жидкости.
Кроме того, в качестве микроорганизма, который содержит фермент, может быть использован штамм дикого типа или может быть использован рекомбинантный штамм, в котором экспрессируется фермент. Такой микроорганизм не ограничивается клеткой микроорганизма, продуцирующей фермент, а также могут использоваться обработанные продукты клетки микроорганизма, такие как обработанная ацетоном клетка микроорганизма и лиофилизованная клетка микроорганизма. Кроме того, могут быть использованы иммобилизованные клетки микроорганизма, полученные путем иммобилизации обработанного продукта клетки микроорганизма с применением метода образования ковалентных связей, метода адсорбции, метода улавливания или тому подобное, или иммобилизованный обработанный клеточный продукт микроорганизмов.
Применение штамма дикого типа, который может продуцировать фермент, образующий пептид и способный образовывать α-L-аспартил-L-фенилаланин-β-эфир, является предпочтительным, так как получение пептида может быть осуществлено более легко без прохождения стадии создания рекомбинантного штамма. С другой стороны, рекомбинантный штамм, который был трансформирован и экспрессирует фермент, образующий пептид и способный образовывать α-L-аспартил-L-фенилаланин-β-эфир, может быть модифицирован таким образом, чтобы фермент, образующий пептид, продуцировался в большем количестве. Таким образом, можно синтезировать α-L-аспартил-L-фенилаланин-β-эфир в большем количестве и с более высокой интенсивностью. Культивирование микроорганизма штамма дикого типа или рекомбинантного штамма в среде для аккумуляции в среде фермента, образующего пептид, и/или микроорганизма, и смешивание аккумулированного таким образом продукта с α,β-диэфиром L-аспарагиновой кислоты и L-фенилаланином может давать α-L-аспартил-L-фенилаланин-β-эфир.
Следует отметить, что, когда используют культивируемые продукты, культивируемые клетки микроорганизма, промытые клетки микроорганизма и обработанные продукты клетки микроорганизма, полученные путем разрушения или лизиса клеток микроорганизма, зачастую присутствует фермент, который разрушает образованный α-L-аспартил-L-фенилаланин-β-эфир, не будучи вовлеченным в образование α-L-аспартил-L-фенилаланин-β-эфира. В таком случае в некоторых случаях предпочтительно добавлять ингибитор металлопротеиназ, такой как этилендиаминтетрауксусная кислота (ЭДТА). Добавляемое количество находится в диапазоне от 0,1 миллимолярного (мМ) до 300 мМ, предпочтительно от 1 мМ до 100 мМ.
Используемое количество фермента или содержащего фермент вещества может быть достаточным, если это количество является количеством, при котором наблюдается требуемый эффект (эффективное количество). Несмотря на то что специалист в данной области техники может легко определить такое эффективное количество путем простого предварительного эксперимента, применяемое количество составляет, например, от приблизительно 0,01 до приблизительно 100 единиц ("Ед") в случае использования фермента и от приблизительно 0,1 до приблизительно 500 г/л в отмытых клеток микроорганизма. Следует отметить, что 1 Ед определяется как количество фермента, которое позволяет продуцировать 1 микромоль (мкмоль) α-L-аспартил-L-фенилаланин-β-метилового эфира из 100 мМ α,β-диметилового эфира L-аспарагиновой кислоты и 200 мМ L-фенилаланина при 25°С в одну минуту.
α,β-Диэфир L-аспарагиновой кислоты, используемый в реакции, может быть любым эфиром, конденсируемым с L-фенилаланином с получением α-L-аспартил-L-фенилаланин-β-эфира. Примеры α,β-диэфира L-аспарагиновой кислоты включают α,β-диметиловый эфир L-аспарагиновой кислоты и α,β-диэтиловый эфир L-аспарагиновой кислоты. Когда взаимодействуют α,β-диметиловый эфир L-аспарагиновой кислоты и L-фенилаланин, то образуется α-L-аспартил-L-фенилаланин-β-метиловый эфир (α-AMP), а когда взаимодействуют α,β-диэтиловый эфир L-аспарагиновой кислоты и L-фенилаланин, то образуется α-L-аспартил-L-фенилаланин-β-этиловый эфир (также называемый α-L-(β-o-этил аспартил)-L-фенилаланин (сокращение: α-AEP).
Тогда как концентрация α,β-диэфира L-аспарагиновой кислоты и L-фенилаланина, которые являются исходными продуктами, в каждом случае составляют от 1 мМ до 10 мМ, предпочтительно от 0,05 М до 2 М, могут быть случаи, когда предпочтительно добавлять один субстрат в эквимолярном или большем количестве по отношению к другому субстрату и по необходимости делать выбор. Кроме того, в тех случаях, когда высокие концентрации субстратов вызывают ингибирование реакции, тогда субстраты добавляют в процессе реакции в концентрации, которая не вызывает ингибирования.
Температура реакции, при которой возможно получение α-L-аспартил-L-