Пиримидинсульфамиды и их использование в качестве антагонистов эндотелиальных рецепторов
Иллюстрации
Показать всеНастоящее изобретение относится к новым сульфамидам общей формулы (I)
где R1 означает (низш.)алкил-O-(СН2)n-;
R2 означает Ra-Y-(CH2)m-;
R3 означает фенил, который может быть замещен такими заместителями, как галоген, (низш.)алкил или (низш.)алкилокси;
R4 означает водород;
R6 означает водород;
Х означает кислород или связь;
Y означает связь или -О-;
n означает целое число 2;
m означает целое число 2;
Ra означает гетероарил, представляющий собой 6-членное ароматическое кольцо, содержащее два атома азота, которое может быть замещено такими заместителями, как галоген, тио(низш.)алкил или (низш.)алкилокси;
и их фармацевтически приемлемым солям,
а также к их применению в качестве активных ингредиентов для получения фармацевтических композиций, обладающих ингибирующей активностью в отношении рецепторов эндотелина. Изобретение относится также к родственным объектам, включающим способы получения следующих соединений
где значения радикалов указаны выше или в описании, 2 н. и 11 з.п. ф-лы, 2 табл.
Реферат
Настоящее изобретение относится к новым пиримидинсульфамидам общей формулы I и к их использованию в качестве активных компонентов для получения фармацевтических композиций. Изобретение относится также к родственным объектам, включающим способы получения соединений, фармацевтических композиций, содержащих одно или более соединений общей формулы I, и, прежде всего, к их применению в качестве антагонистов рецепторов эндотелина.
Эндотелины (ЕТ-1, ЕТ-2 и ЕТ-3) представляют собой пептиды, содержащие 21 аминокислотный остаток и которые продуцируются и проявляют активность в большинстве тканей (Yanagisawa M. и др., Nature, 332, 411 (1988)). Эндотелины являются активными вазоконстрикторами и важными медиаторами сердечной, почечной, эндокринной и иммунной функций (McMillen M.A. и др., J.Am.Coll.Surg., 180, 621 (1995)). Эти пептиды принимают участие в бронхостенозе и регулируют высвобождение нейромедиаторов, активацию воспалительных клеток, фиброз, пролиферацию и дифференциацию клеток (Rubanyi G.M. и др., Pharmacol. Rev., 46, 328 (1994)).
Два рецептора эндотелина были клонированы и охарактеризованы в тканях млекопитающих (ЕТА, ЕТВ) (Arai Н. и др., Nature, 348, 730 (1990); Sakurai Т. и др., Nature, 348, 732 (1990)). Рецептор ЕТА характеризуется более высокой аффинностью в отношении к ЕТ-1 и ЕТ-2 по сравнению с ЕТ-3. Рецептор ЕТА в основном преобладает в клетках гладких мышц сосудов и опосредует ответные реакции в виде сужения сосудов и пролиферации клеток (Ohlstein E.H. и др., Drug Dev. Res., 29, 108 (1993)). В отличие от ЕТА рецептор ЕТВ характеризуется эквивалентной аффинностью в отношении трех изопептидов эндотелина и связывается с линейной формой эндотелина, тетра-Ala-эндотелином и сарафотоксином S6C (Ogawa Y. и др., BBRC, 178, 248 (1991)). Этот рецептор локализован в эндотелии сосудов и гладких мышцах сосудов и прежде всего преобладает в тканях легких и мозга. Рецептор ЕТВ из эндотелиальных клеток опосредует временную ответную реакцию на ЕТ-1 и ЕТ-2, т.е. расширение сосудов в ответ на высвобождение оксида азота и/или простациклина, а рецептор ЕТВ из клеток гладких мышц обладает сосудосуживающим действием (Sumner M.J. и др., Brit. J. Pharmacol., 107, 858 (1992)). Рецепторы ЕТА и ЕТВ характеризуются высокой структурной гомологией и относятся к подсемейству рецепторов, сопряженных с G-белком.
Предполагают, что патофизиологическая роль ЕТ-1 связана с его повышенным уровнем в плазме и тканях при некоторых заболеваниях, таких как гипертензия, легочная гипертензия, сепсис, атеросклероз, острый инфаркт миокарда, сердечная недостаточность, почечная недостаточность, мигрень и астма. В связи с этим антагонисты рецепторов эндотелина были тщательно изучены в качестве перспективных терапевтических агентов. При доклинических и/или клинических испытаниях установлено, что антагонисты рецепторов эндотелина проявляют эффективность при лечении различных заболеваний, таких как церебральный вазоспазм в результате субарахноидального кровоизлияния, сердечная недостаточность, легочная и системная гипертензия, нейрогенное воспаление, почечная недостаточность и инфаркт миокарда.
В настоящее время только один антагонист рецепторов эндотелина (Tracler™) выпускается в виде лекарственных препаратов, и некоторые из них проходят клинические испытания. Однако некоторые из этих молекул характеризуются рядом недостатков, таких как сложность синтеза, низкая растворимость, высокая молекулярная масса, неблагоприятный фармакокинетический профиль или побочные действия (например, повышение концентрации ферментов печени). Более того, до сих пор не изучено влияние различий в подавлении рецепторов ЕТA/ЕТВ на клинические симптомы. Таким образом, существует необходимость определить для каждого антагониста фармакохимические и фармакокинетические свойства, а также их селективность для данного клинического показания. Кроме того, в литературе не описано ни одного антагониста рецепторов эндотелина, содержащего пиримидиновый фрагмент с сульфамидной группой [2, 3, 5, 6, 8]. Неожиданно было установлено, что замещенные пиримидины, описанные ниже, относятся к новому классу пиримидинов и обладают указанным выше набором свойств, кроме того, соединения проявляют смешанную специфичность и селективность в отношении связывания ЕТА.
Ингибирующую активность соединений общей формулы I в отношении рецепторов эндотелина определяли с использованием следующих методов анализа.
Для определения активности и эффективности соединений общей формулы I использовали следующие методы.
1) Ингибирование связывания эндотелина с мембранами клеток СНО, содержащих рецепторы ЕТ человека.
Для определения конкурентного связывания использовали мембраны клеток СНО, экспрессирующих рекомбинантные рецепторы ЕТА или ЕТВ человека. Микросомальные мембраны получали из рекомбинантных клеток СНО и проводили анализ связывания, как описано ранее (Breu V. и др., FEBS Lett, 334, 210 (1993)).
Анализ проводили в 200 мкл 50 мМ буферного раствора Трис/HCl, рН 7,4, содержащего 25 мМ MnCl2, 1 мМ ЭДТУ и 0,5% (мас./об.) БСА с использованием полипропиленовых микропланшетов. Мембранную фракцию, содержащую 0,5 мкг белка, инкубировали в течение 2 ч при 20°С в присутствии 8 пМ [125I]ЕТ-1 (4000 имп./мин) и увеличивающейся концентрации немеченых антагонистов. Максимальное и минимальное связывание определяли в образцах, не содержащих и содержащих 100 нМ ЕТ-1 соответственно. Через 2 ч мембраны отфильтровывали на планшетах для фильтрования, содержащих фильтры GF/C (Unifilterplates фирмы Canberra Packard S.A. Цюрих, Швейцария). В каждую лунку добавляли по 50 мкл сцинтилляционной смеси (MicroScint 20 фирмы Canberra Packard S.A., Цюрих, Швейцария) и в планшетах для фильтрования определяли радиоактивность в счетчике радиоактивности для микропланшет (прибор TopCount, фирмы Canberra Packard S.A. Цюрих, Швейцария).
Все исследованные соединения растворяли, разбавляли и добавляли в реакционную смесь в виде раствора в ДМСО. Анализ проводили в присутствии 2,5% ДМСО, который, как было установлено, не оказывает значительного влияния на связывание. Величину IC50 рассчитывали как концентрацию антагониста, ингибирующую специфическое связывание с ЕТ-1 на 50%. Для контрольных соединений были получены следующие величины IC50: клетки ЕТА: 0,075 нМ (n=8) для ЕТ-1 и 118 нМ (n=8) для ЕТ-3; клетки ЕТВ: 0,067 нМ (n=8) для ЕТ-1 и 0,092 нМ (n=3) для ЕТ-3.
Величины IC50, определенные для соединений общей формулы I, приведены в таблице 1.
| Таблица 1 | ||
| Соединение, номер примера | IC50 [нМ] | |
| ЕТA | ЕТB | |
| Пример 1 | 0,28 | 174 |
| Пример 2 | 0,22 | 222 |
| Пример 3 | 0,20 | 120 |
| Пример 4 | 1,27 | 560 |
2) Ингибирование индуцированных эндотелином сокращений колец, полученных из аорты крысы (рецепторы ЕТA), и колец, полученных из трахеи крысы (рецепторы ЕТB).
Функциональную ингибирующую активность антагонистов эндотелина определяли по их ингибированию сокращения, индуцированного действием эндотелина-1 на кольца из аорты крысы (рецепторы ЕТА), и сокращения, индуцированного действием сарафотоксина S6C на кольца из трахеи крысы (рецепторы ЕТB). Взрослых крыс Wistar анестезировали и обескровливали, затем иссекали грудные аорту или трахею, препарировали их и разрезали на кольца толщиной 3-5 мм, осторожно соскребали эндотелий/эпителий с внутренней поверхности. Каждое кольцо суспендировали в отдельной ванне для органа объемом 10 мл, заполненной раствором Кребса-Хенселейта (состав буферного раствора: 115 мМ NaCl, 4,7 мМ KCl, 1,2 мМ MgSO4, 1,5 мМ КН2PO4, 25 мМ NaHCO3; 2,5 мМ CaCl2, 10 мМ глюкоза), при температуре 37°С и содержащем 95% О2 и 5% СО2. Кольца подсоединяли к динамометрическому датчику и измеряли изометрическое растяжение (прибор фирмы ЕМКА Technololgies SA, Париж, Франция). Кольца растягивали до натяжения покоя 3 г (аорта) или 2 г (трахея). Через 10 мин инкубирования с исследуемым соединением или с носителем добавляли кумулятивные дозы ЕТ-1 (аорта) или сарафотоксина S6C (трахея). Функциональную ингибирующую активность исследуемого соединения оценивали при расчете соотношения концентраций, например, по сдвигу вправо от величины ЕС50, индуцированной различными концентрациями исследуемого соединения. Величина ЕС50 означает концентрацию эндотелина, при которой наблюдается сокращение на половину от максимально возможной величины, величина рА2 означает отрицательный логарифм концентрации антагониста, при которой наблюдается сдвиг величины EC50 в 2 раза.
Величины рА2, полученные для соединений формулы I, приведены в таблице 2.
| Таблица 2 | ||
| Соединение, номер примера | Величина рА2 | |
| Аорта | Трахея | |
| Пример 1 | 6,90 | 5,29 |
| Пример 2 | 8,48 | <5,0 |
Поскольку описанные соединения обладают способностью ингибировать связывание эндотелина, то их используют для лечения заболеваний, которые связаны с возрастанием степени сужения сосудов, пролиферации или воспаления, вызванных эндотелином. Примеры таких заболеваний включают гипертензию, легочную гипертензию, сердечно-сосудистые заболевания, сердечную недостаточность, почечную ишемию и ишемию миокарда, почечную недостаточность, церебральную ишемию, деменцию, мигрень, субарахноидальное кровоизлияние, синдром Рейно, пальцевидную язву и портальную гипертензию. Их используют также при лечении или профилактике атеросклероза, рестеноза после пластической операции на сосудах с использованием баллона или стента, воспалительных процессов, язвы желудка и язвы двенадцатиперстной кишки, рака, меланомы, рака предстательной железы, гипертрофии предстательной железы, эректильной дисфункции, снижения слуха, слепоты, хронического бронхита, астмы, пневмосклероза, грамотрицательной септицемии, шока, серповидно-клеточной анемии, гломерулонефрита, почечных колик, глаукомы, заболеваний соединительных тканей, терапии и профилактике осложнений при диабете, осложнений после операций на сосудах или сердце, осложнений после трансплантации органов, после лечения циклоспорином, боли, гиперлипидемии, а также заболеваний, которые, как известно, связаны с эндотелином.
Соединения вводят пероральным, ректальным, парентеральным способами, например внутривенным, внутримышечным, подкожным, подоболочечным или чрезкожным способами, подъязычным способом, в виде офтальмологических или аэрозольных препаратов. Примеры включают капсулы, таблетки, суспензии или растворы для перорального введения, суппозитории, растворы для инъекций, глазные капли, мази или аэрозоли/распылители.
Предпочтительные варианты включают внутривенный, внутримышечный или пероральный способ введения, а также глазные капли. Доза зависит от типа активного компонента, возраста и состояния пациента, а также от формы введения. Обычно дозы составляют 0,1-50 мг/кг массы тела в сутки. Препарат, содержащий соединение, содержит инертный или фармакодинамически активный эксципиент. Таблетки или гранулы, например, содержат ряд связующих, наполнителей, носителей или разбавителей.
Настоящее изобретение относится к пиримидинсульфамидам общей формулы I
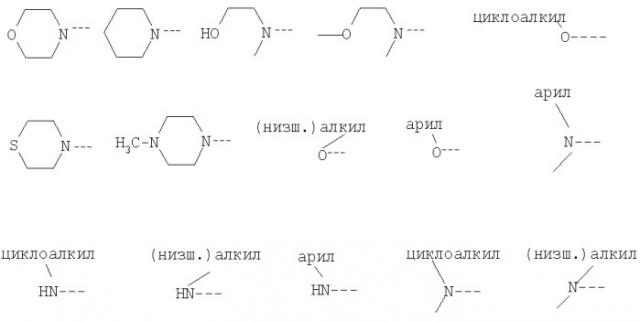
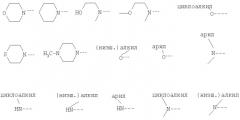
где R1 означает (низш.)алкил-O-(СН2)n-, циклоалкил-O-(СН2)n-, циклоалкил-СН2-O-(СН2)n-;
R2 означает -СН3, Ra-Y-(CH2)m-;
R3 означает арил, гетероарил;
R4 означает водород, трифторметил, (низш.)алкил, (низш.)алкиламино, (низш.)алкилокси, (низш.)алкилокси(низш.)алкилокси, гидрокси(низш.)алкилокси, (низш.)алкилсульфинил, (низш.)алкилтио, (низш.)алкилтио(низш.)алкил, гидрокси(низш.)алкил, (низш.)алкилокси(низш.)алкил, гидрокси(низш.)алкилокси(низш.)алкил, гидрокси(низш.)алкиламино, (низш.)алкиламино(низш.)алкил, амино, ди(низш.)алкиламино, [N-(гидрокси(низш.)алкил)-N-((низш.)алкил)]амино, арил, ариламино, арил(низш.)алкиламино, арилтио, арил(низш.)алкилтио, арилокси, арил(низш.)алкилокси, арил(низш.)алкил, арилсульфинил, гетероарил, гетероарилокси, гетероариламино, гетероарилтио, гетероарил(низш.)алкил, гетероарилсульфинил, гетероциклил, гетероциклил(низш.)алкилокси, гетероциклилокси, гетероциклиламино, гетероциклил(низш.)алкиламино, гетероциклилтио, гетероциклил (низш.)алкилтио, гетероциклил(низш.)алкил, гетероциклилсульфинил, циклоалкил, циклоалкилокси, циклоалкил(низш.)алкилокси, циклоалкиламино, циклоалкил(низш.)алкиламино, циклоалкилтио, циклоалкил(низш.)алкилтио, циклоалкил(низш.)алкил, циклоалкилсульфинил,
R6 означает водород или метил,
X означает кислород, серу, -СН2- или связь,
Y означает связь, -О-, -NH-, -SO2-NH-, -NH-SO2-NH-, -O-СО-, -СО-O-, -O-CO-NH-, -NH-CO-O-, -NH-CO-NH-,
n означает простые числа 2, 3 или 4,
m означает простые числа 2, 3 или 4,
Ra означает арил, гетероарил, (низш.)алкил, циклоалкил, водород;
и к оптически чистым энантиомерам, смесям энантиомеров, таким как, например, рацематы; к оптически чистым диастереомерам, смесям диастереомеров, рацематам диастереомеров, смесям рацематов диастереомеров и к мезоформам и их фармацевтически приемлемым солям.
При описании общей формулы I, если не указано иное, термин «(низш.)» означает прямые или разветвленные группы, содержащие от 1 до 7 атомов углерода, предпочтительно от 1 до 4 атомов углерода. Примеры (низш.)алкильных или (низш.)алкоксильных групп включают метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, гептил, метокси, этокси, пропокси, бутокси, изобутокси, фторбутокси, и трет-бутокси. (Низш.)алкенилдиоксигруппы предпочтительно означают метилендиокси и этилендиокси. Примеры (низш.)алканоильных групп включают ацетил, пропаноил и бутаноил. Термин (низш.)алкенилен означает, например, винилен, пропенилен и бутенилен. Термины (низш.)алкенил и (низш.)алкинил означают группы, такие как этенил, пропенил, бутенил, 2-метилпропенил и этинил, пропинил, бутинил, пентинил, 2-метилпентинил. Термин (низш.)алкенилокси означает аллилокси, винилокси и пропенилокси. Термин «циклоалкил» означает насыщенный циклический углеводород, содержащий от трех до семи атомов углерода, например циклопропил, циклобутил, циклопентил, циклогексил и циклогептил, которые могут содержать следующие заместители: (низш.)алкил, гидрокси(низш.)алкил, амино(низш.)алкил и (низш.)алкокси(низш.)алкил. Термин гетероциклил означает насыщенные или ненасыщенные (но не ароматические) четырех-, пяти-, шести- или семичленные кольца, содержащие один или два атома азота, кислорода или серы, которые являются одинаковыми или различными, причем упомянутые кольца могут содержать соответствующие заместители: (низш.)алкил, (низш.)алкокси, например, пиперидинил, морфолинил, тиоморфолинил, пиперазинил, тетрагидропиранил, дигидропиранил, 1,4-диоксанил, пирролидинил, тетерагидрофуранил, дигидропирролил, дигидроимидазолил, дигидропиразолил, пиразолидинил и замещенные производные таких колец, содержащие заместители, описанные выше. Термин гетероарил означает шестичленные ароматические кольца, содержащие от одного до четырех атомов азота, бензоконденсированные шестичленные ароматические кольца, содержащие от одного до трех атомов азота, пятичленные ароматические кольца, содержащие один атом кислорода или азота, или серы, бензоконденсированные пятичленные ароматические кольца, содержащие один атом кислорода, азота или серы, пятичленные ароматические кольца, содержащие атомы кислорода и азота и их бензоконденсированные производные, пятичленные ароматические кольца, содержащие атомы серы и азота и их бензоконденсированные производные, пятичленные ароматические кольца, содержащие два атома азота и их бензоконденсированные производные, пятичленнные ароматические кольца, содержащие три атома азота и их бензоконденсированные производные, или тетеразолильное кольцо, например фуранил, тиенил, пирролил, пиридинил, пиримидинил, индолил, хинолинил, изохинолинил, имидазолил, триазинил, тиазинил, тиазолил, изотиазолил, пиридазинил, оксазолил, изоксазолил, 5-оксо-1,2,4-оксадиазолил, 5-оксо-1,2,4-тиадиазолил, 5-тиоксо-1,2,4-оксадиазолил, 2-оксо-1,2,3,5-оксатиадиазолил, причем такие кольца могут быть замещены следующими группами: (низш.)алкил, (низш.)алкенил, амино, амино(низш.)алкил, галоген, гидрокси, (низш.)алкокси, трифторметокси, трифторметил, карбоксил, карбоксамидил, тиоамидил, амидинил, (низш.)алкоксикарбонил, циано, гидрокси(низш.)алкил, (низш.)алкилокси(низш.)алкил или другие гетероарильные или гетероциклильные кольца (например, см. [7]). Термин арил означает незамещенные и моно-, ди- или тризамещенные ароматические кольца, содержащие от шести до десяти атомов углерода, такие как фенил или нафтил, которые содержат следующие заместители: арил, галоген, гидрокси, (низш.)алкил, (низш.)алкенил, (низш.)алкинил, (низш.)алкокси, (низш.)алкенилокси, (низш.)алкинил(низш.)алкилокси, (низш.)алкенилен, (низш.)алкиленокси или (низш.)алкилендиокси, которые вместе с фенильным кольцом образуют пяти- или шестичленное кольцо, гидрокси(низш.)алкил, гидрокси(низш.)алкенил, гидрокси(низш.)алкил(низш.)алкинил, (низш.)алкилокси(низш.)алкил, (низш.)алкилокси(низш.)алкилокси, трифторметил, трифторметокси, циклоалкил, гидроксициклоалкил, гетероциклил и гетероарил.
Термин «фармацевтически приемлемые соли» означает соли неорганических или органических кислот, таких как галогенводородные кислоты, например хлористоводородная или бромистоводородная кислоты, серная кислота, фосфорная кислота, азотная кислота, лимонная кислота, муравьиная кислота, уксусная кислота, малеиновая кислота, винная кислота, метилсульфоновая кислота, пара-толуолсульфоновая кислота и т.п. или, если соединение формулы I присутствует в кислой форме, соли неорганических оснований, таких как основания щелочных или щелочноземельных металлов, таких как гидроксид натрия, гидроксид калия, гидроксид кальция и т.п.
Соединения общей формулы I содержат один или более асимметрических атомов углерода и их можно получить в форме оптически чистых энантиомеров или диастереомеров, смесей энантиомеров или диастереомеров, рацематов диастереомеров, смесей рацематов диастереомеров или в виде мезоформ. В настоящем изобретении описаны все эти формы. Смеси разделяют стандартными методами, например хроматографией на колонке, тонкослойной хроматографией, ЖХВР или перекристаллизацией.
Поскольку описанные соединения обладают способностью ингибировать связывание эндотелина, то их используют для лечения заболеваний, которые связаны с возрастанием степени сужения сосудов, пролиферации или воспаления, вызванных эндотелином. Примеры таких заболеваний включают гипертензию, легочную гипертензию, сердечно-сосудистые заболевания, сердечную недостаточность, почечную ишемию и ишемию миокарда, почечную недостаточность, церебральную ишемию, деменцию, мигрень, субарахноидальное кровоизлияние, синдром Рейно, пальцевидную язву и портальную гипертензию. Их используют также при лечении или профилактике атеросклероза, рестеноза после пластической операции на сосудах с использованием баллона или стента, воспалительных процессов, язвы желудка и язвы двенадцатиперстной кишки, онкологических заболеваний, меланомы, рака предстательной железы, гипертрофии предстательной железы, эректильной дисфункции, снижении слуха, слепоты, хронического бронхита, астмы, фиброза легких, грамотрицательной септицемии, шока, серповидно-клеточной анемии, гломерулонефрита, почечных колик, глаукомы, заболеваний соединительных тканей, терапии и профилактике осложнений при диабете, осложнений после операций на сосудах или сердце, осложнений после трансплантации органов, после лечения циклоспорином, боли, гиперлипидемии, а также заболеваний, которые, как известно, связаны с эндотелином.
Такие композиции вводят в энтеральной или пероральной форме, например, в виде таблеток, драже, желатиновых капсул, эмульсий, растворов или суспензий, в форме для введения в нос, такой как спрей, или в ректальной форме, такой как суппозиторий. Такие соединения вводят также внутримышечным, парентеральным или внутривенным способом, например, в форме растворов для инъекций.
Такие фармацевтические композиции содержат соединения формулы I, их фармацевтически приемлемые соли в комбинации с неорганическими и/или органическими эксципиентами, которые являются стандартными в фармацевтической промышленности, такими как лактоза, кукурузный крахмал, его производные, тальк, стеариновая кислота или их соли.
Для получения желатиновых капсул используют растительные масла, воски, жиры, жидкие или полужидкие полиолы. Для получения растворов и сиропов используют, например, воду, полиолы, сахарозу и глюкозу. Растворы для инъекций готовят с использованием, например, воды, полиолов, спиртов, глицерина, растительных масел, лицетина или липосом. Суппозитории получают с использованием природных или гидрированных масел, восков, жирных кислот (жиров), жидких или полужидких полиолов.
Композиции содержат дополнительные консерванты, стабилизаторы, вещества, повышающие или регулирующие вязкость, улучшающие свойства растворов, подсластители, красители, вкусовые добавки, соли для изменения осмотического давления, буферные вещества или антиоксиданты.
Соединения общей формулы I используют также в комбинации с одним или более других терапевтических агентов, например, α- и β-блокаторов, таких как фентоламин, феноксибензамин, атенолол, пропранолол, тимолол, метопролол, картеолол и т.п., сосудорасширяющие средства, такие как гидралазин, миноксидил, диазоксид или флозехинан, антагонисты кальция, такие как дилтиазем, никардипин, нимодипин, верапамил или нифедипин, ингибиторы АКФ, такие как силазаприл, каптоприл, эналаприл, лизиноприл и т.п., активаторы кальциевых каналов, такие как пинакидил, антагонисты рецептора ангиотензина II, такие как лосартан, валсартан, ирбесартан и т.п., диуретики, такие как гидрохлортиазид, хлортиазид, ацетоламид, буметанид, фуросемид, метолазон или хлорталидон, симпатолитики, такие как метилдопа, клонидин, гуанабенз или резерпин, производные простациклина, такие как флолан, антихолинергические агенты и другие терапевтические агенты, предназначенные для снижения повышенного кровяного давления и лечения других сердечно-сосудистых заболеваний.
Доза изменяется в широких пределах, но зависит от конкретного случая. В основном, дневная доза, вводимая пероральным способом, составляет от приблизительно 3 мг до приблизительно 3 г, предпочтительно от приблизительно 10 мг до приблизительно 1 г, наиболее предпочтительно от 5 до 300 мг, для взрослого человека с массой тела приблизительно 70 кг. Дозу вводят предпочтительно 1-3 раза в день равными дозами. Обычно дети должны получать уменьшенные дозы, адаптированные для их массы тела и возраста.
Предпочтительные соединения включают соединения общей формулы I, где R3 означает фенил, моно- или дизамещенный фенил, замещенный группами этокси, метокси или хлор, а X означает кислород, и их фармацевтически приемлемые соли.
Вторая группа предпочтительных соединений общей формулы I включает группы, где R3 означает фенил, моно- или дизамещенный фенил, замещенный группами этокси, метокси или хлор, X означает кислород, а R2 означает -(СН2)m-Y-Ra, и их фармацевтически приемлемые соли.
Третья группа предпочтительных соединений общей формулы I включает группы, где R3 означает фенил, моно- или дизамещенный фенил, замещенный группами этокси, метокси или хлор, X означает кислород, а R2 означает -(CH2)2-O-Ra, где Ra означает гетероарил, и их фармацевтически приемлемые соли.
Другая группа предпочтительных соединений включает соединения формулы II
где R1, R2, R3 и R4 имеют значения, определенные выше для общей формулы I,
и фармацевтически приемлемые соли соединений формулы II.
Предпочтительными являются также соединения формулы III
где R1, R2 и R4 имеют значения, определенные выше для общей формулы I, а А означает водород, метил, этил, хлор, бром, фтор, трифторметил или метокси,
и фармацевтически приемлемые соли соединений формулы III.
Предпочтительными являются также соединения формулы IV
где R1, R4 и m имеют значения, определенные выше для формулы I, A определено выше для формулы III, a R5 означает арил или гетероарил,
и фармацевтически приемлемые соли соединений формулы IV.
Другой наиболее предпочтительной группой соединений являются соединения формулы V
где R1 определен выше для общей формулы I, А определен выше для формулы III, a R5 означает арил или гетероарил,
и фармацевтически приемлемые соли соединений формулы V.
Наиболее предпочтительные соединения из группы соединений формулы V включают соединения, где R5 означает замещенный пиримидин, и их фармацевтически приемлемые соли.
Другая группа предпочтительных соединений включает соединения общей формулы I, где R1 означает СН3-О-СН2СН2-, R6 означает водород, а R2, R3 и R4 определены выше для общей формулы I, и их фармацевтически приемлемые соли.
Следующая группа предпочтительных соединений включает соединения общей формулы V, где R1 означает СН3-О-СН2СН2-, А определено выше для формулы III, a R5 означает арил или гетероарил, и фармацевтически приемлемые соли соединений формулы V.
Наиболее предпочтительные соединения включают
[6-[2-(5-бромпиримидин-2-илокси)этокси]-5-(2-хлор-5-метоксифенокси)пиримидин-4-ил]амид 2-метоксиэтансульфаминовой кислоты,
{5-(4-бромфенил)-6-[2-(5-бромпиримидин-2-илокси)этокси]пиримидин-4-ил}амид 2-метоксиэтансульфаминовой кислоты,
{5-(4-бромфенил)-6-[2-(5-метилсульфанилпиримидин-2-илокси)этокси]пиримидин-4-ил}амид 2-метоксиэтансульфаминовой кислоты,
{5-(4-бромфенил)-6-[2-(5-метоксипиримидин-2-илокси)этокси]пиримидин-4-ил}амид 2-метоксиэтансульфаминовой кислоты.
Соединения общей формулы I по настоящему изобретению получают согласно общей последовательности реакций, описанных ниже. Для упрощения и ясности изложения в некоторых случаях описывается только часть возможных методов синтеза соединений общей формулы I. Список публикаций приведен в конце данного раздела. В описании соответствующие ссылки заключены в квадратные скобки.
Способ А
Требуемые соединения общей формулы I получают при взаимодействии соединения формулы 1
где G1 означает реакционноспособный остаток, предпочтительно атом хлора, а другие символы определены выше для общей формулы I,
с соединением формулы 2
где R2 имеет значение, определенное выше для общей формулы I,
или его солью.
Способ Б
Соединения общей формулы I получают также при взаимодействии соединения формулы 3
где символы имеют значения, определенные выше для общей формулы I,
или его соли с соединением формулы 4
где G2 означает реакционноспособный остаток, предпочтительно атом галогена, а R5 имеет значение, определенное выше для формулы IV.
Способ В
Соединения общей формулы I получают также при взаимодействии соединения формулы 5
где G3 означает (низш.)алкилсульфонил или фенилсульфонил или атом галогена, а другие символы имеют значения, определенные выше для общей формулы I,
или его соли с соединением формулы 6
где R4′ означает
Способы А-В описаны также в работе [5].
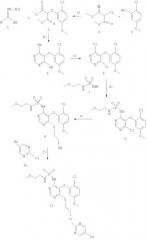
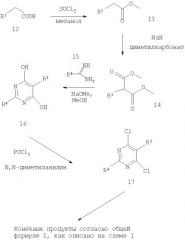
Синтез, представленный на схеме 1, предназначенный для получения соединений общей формулы I, проиллюстрирован при описании синтеза в примере 1. Соединения, описанные в других примерах, приведенных в настоящем описании, получают по аналогичным методикам, с использованием соответствующих заместителей и условий реакции. Ссылки на публикации заключены в квадратные скобки и приведены в конце данного раздела. Амидины 1 являются коммерческими препаратами или их синтезировали по стандартным методикам [1] при взаимодействии соответствующего нитрила с метилатом натрия в метаноле с последующим добавлением хлорида аммония. 2-Замещенные сложные эфиры малоновой кислоты 2 получали по опубликованным методикам [2] при взаимодействии диметилхлормалоната 4 с соответствующим спиртом 3 [9] в ацетоне и карбонате калия в качестве основания. Соединения 2 растворяли в метаноле, добавляли метилат натрия и перемешивали в течение приблизительно 30 мин, затем добавляли производное амидина 1. Перемешивание при температуре окружающей среды продолжали в течение 8 ч. После обработки кислотой выделяли 4,6-дигидроксипиримидины 5 (выход от 70 до 90%) [2]. Соединения 5 или их таутомерную форму превращали в дихлорпроизводное 6 при взаимодействии с оксихлоридом фосфора в присутствии N,N-диметиланилина при повышенной температуре (60-120°С) (выход от 40 до 75%) [3]. Дихлориды 6 вводили в реакцию с избытком соответствующей соли сульфамида калия 7 (полученной, как представлено на схеме 2) в ДМСО при КТ или при температуре от 40 до 60°С, при этом получали монохлорпиримидины 8 (выход от 70 до 90%) с использованием перекристаллизации или хроматографии. Производные пиримидина 8 вводили в реакцию с этиленгликолем (или другим 1-ω-диолом или моноспиртом) в присутствии основания, такого как трет-бутилат калия, гидрид натрия или натрий, при температуре от 80 до 110°С в течение от 4 до 16 ч, при этом получали соединения 9, которые относятся к первой группе соединений, заявленных в формуле изобретения (выход от 50 до 70%). Соединение 9 превращали в соединения 11 при взаимодействии с 2-хлор-5-бромпиридином 10 (или другим пригодным производным пиримидина или пиридина [16], [17]) в ТГФ/ДМФА, приблизительно 5:1, при КТ или при температуре от 50 до 70°С (выход от 50 до 80%).
Схема 1. Пример синтеза (пример 1).
а) К2СО3, ацетон, кипячение с обратным холодильником, b) NaOMe, MeOH, КТ, с) POCl3, N,N-диметиланилин, 70-130°С, d) 7, ДМСО, КТ, е) трет-бутилат калия, этиленгликоль, 75-100°С, f) NaH, ДМФА и/или ТГФ, 10, КТ-60°С.
Другие условия синтеза приведены в работах [1]-[3], [5], [6], [8], [10]-[15] и [20].
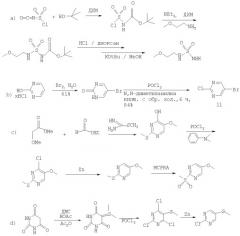
Схема 2. Синтез сульфамидных остатков, см. также [10]-[15], [19] и [20], и синтез замещенных пиримидинов в работах [16] и [17].
Схема 3. Получение предшественников для синтеза соединений общей формулы I, где X означает связь [5], [18].
На схеме 3 символы имеют значения, описанные выше для общей формулы I.
[1] W.Göhring, J.Schildknecht, M. Federspiel; Chimia, 50, 538-543 (1996).
[2] W.Neidhart, V.Breu, D.Bur, К.Burri, M.Clozel, G.Hirth, M.Müller, H.P.Wessel, H.Ramuz; Chimia, 50, 519-524 (1996), и цитируемые в ней работы.
[3] W.Neidhart, V.Breu, К.Burri, M.Clozel, G.Hirth, U.Klinkhammer, T.Giller, H.Ramuz; Bioorg. Med. Chem. Lett., 7, 2223-2228 (1997). R.A.Nugent, S.T.Schlachter, M.J.Murphy, G.J.Cleek, T.J.Poel, D.G.Whishka, D.R.Graber, Y.Yagi, B.J.Keiser, R.A.Olmsted, L.A.Kopta, S.M.Swaney, S.M.Poppe, J.Morris, W.G.Tarpley, R.C.Thomas; J. Med. Chem., 41, 3793-3803 (1998).
[4] J.March; Advanced Organic Chemistry, 4th Ed., p.499 (1994) и цитируемые в ней работы.
[5] ЕР 0743307 A1; EP 0658548 B1; EP 0959072 A1 (Tanabe Seiyaku).
[6] EP 0633259 B1; EP 0526708 A1; WO 96/19459 (F.Hoffmann-LaRoche).
[7] Описание синтеза пятичленных гетероциклов приведено в работе Y.Kohara и др.; J. Med. Chem., 39, 5228-5235 (1996), и цитируемых в ней работах.
[8] ЕР 0882719 A1 (Yamanouchi Pharmaceutical Co., Ltd).
[9] M.Julia, J.de Rosnay, Chim. Ther. 4, 334-343 (1965).
[10] E.Cohen, В.Klarberg; J. Am. Chem. Soc., 84, 1994 (1962).
[11] G.Weiss, G.Schulze, Liebigs Ann. Chem., 729, 40 (1969).
[12] R.Graf, Chem. Ber., 92, 509 (1959).
[13] J.A.Kloek, К.L.Leschinsky, J. Org. Chem., 41, 4028 (1976).
[14] R.E.Olson, Т.M.Sielecki и др.; J. Med. Chem., 42, 1178 (1999).
[15] R.P.Dickinson, К.N.Dack и др.; J. Med. Chem., 40, 3442 (1997).
[16] D.G.Crosby, R.V.Berthold; J. Org. Chem., 25; 1916 (1960); D.J.Brown, J.M.Lyall, Aust. J. Chem. 17, 794-802 (1964); Н.С.Koppel, R.H.Springer, R.К.Robins, С.С.Cheng, J.Org. Chem. 27, 3614-3617 (1962); S.A.Jacobsen, S.Rodbotten, T.Benneche, J. Chem. Soc. Perkin Trans 1, 3265-3268 (1999); С.Maggiali, G.Morini, F.Mossini, Farmaco, Ed. Sci. 43, 277-292 (1988); Patent France 1549494 (1968) (D.Razavi).
[17] US-4233294 (1980). (Bayer AG).
[18] E.D.Morgan; Tetrahedron, 23, 1735 (1967).
[19] M.J.Tozer, I.M.Buck и др.; Bioorg. Med. Chem. Lett., 9, 3103 (1999). G.Dewynter и др.; Tetrahedron, 49, 65 (1993).
[20] WO 0253557 (Actelion Pharmaceuticals Ltd.)
Примеры
В следующих примерах иллюстрируется настоящее изобретение.
Список сокращений:
| Ас2O | ангидрид уксусной кислоты |
| DBU | 1,8-диазабицикло[5.4.0]ундец-7-ен(1,5-5) |
| ДХМ | дихлорметан |
| DMAP | 4-диметиламинопиридин |
| ДМФА | диметилформамид |
| ДМСО | диметилсульфоксид |
| ЭА | этилацетат |
| Et3N | триэтиламин |
| KOtBu | трет-бутилат калия |
| МСРВА | мета-хлорпербензойная кислота |
| мин | минуты |
| кип. с обр. хол. | кипячение с обратным холодильником |
| КТ | комнатная температура |
| ТГФ | тетрагидрофуран |
| tR | время удерживания |
Следующие соединения получали согласно методикам, описанным выше и представленным на схемах 1-3. Все соединения охарактеризовывали с использованием 1H-ЯМР (300 МГц) и необязательно 13С-ЯМР (75 МГц) (прибор Varian Oxford, 300 МГц; величина химических сдвигов выражена в част./мин по отношению к используемому растворителю, s означает синглет, d означает дублет, t означает триплет; m означает мультиплет), с использованием ЖХ-МС1 (прибор Finnigan Navigator HP 1100 Binary Pump and DAD, колонка: 4,6×50 мм, сорбент Develosil RP Aqueous, 5 мкм, 120А, градиент (1 мин): 5-95% ацетонитрил в воде, содержащей 0,04% трифторуксусной кислоты, скорость потока: 4,5 мл/мин) или ЖХ-МС2 (прибор Waters Micromass; платформа ZMD с зондом ESI, Alliance 2790 НТ и DAD 996, колонка: 2×30 мм, сорбент Gromsil, 3 мкм, 120А; градиент 6 мин: 0-100% ацетонитрил в воде, содержащий 0,05% муравьиной кислоты, скорость потока: 0,45 мл/мин), tR в мин; с использованием ТСХ (пластины для ТСХ фирмы Merck, силикагель 60 F254) и необязательно с использованием температуры плавления.
Пример 1
а) К суспензии К2СО3 (49,3 г) в ацетоне (100 мл) по каплям при 40°С добавляли раствор 2-хлор-5-метоксифенола (37,7 г, tкип 83-86°С, 13 мбар, [9]). Затем по каплям добавляли диметиловый эфир хлормалоновой кислоты (43,6 г) в ацетоне (100 мл). Смесь кипятили с обратным холодильником в течение 16 ч, затем растворитель удаляли при пониженном давлении. Остаток переносили в воду (400 мл) и экстрагировали два раза ДХМ (400 мл). Органические экстракты сушили над MgSO4 и упаривали. После обработки маслообразного остатка диэтиловым эфиром продукт кристаллизовали. Кристаллы собирали, промывали смесью диэтилового эфира и гексана и сушили, при этом получали диметиловый эфир 2-(2-хлор-5-метоксифенокси)малоновой кислоты (53,73 г) в виде кристаллов белого цвета. 1H-ЯМР (CDCl3): 3,76 (s, 3H), 3,86 (s, 6H), 5,20 (s, 1H), 6,53-6,58 (m, 2H), 7,24-7,29 (m, 1H).
b) Раствор диметилового эфира 2-(2-хлор-5-метоксифенокси)малоновой кислоты (10 г) в метаноле (100 мл) по каплям при 0°С добавляли к раствору NaOMe (5,6 г) в метаноле (250 мл). Раствор перемешивали при КТ в течение 2 ч, затем добавляли гидрохлорид формамидина (3,347 г). Смесь перемешивали при КТ в течение 72 ч. Растворитель удаляли при пониженном давлении и полученный остаток обрабатывали 2 н. водным раствором HCl (150 мл). После перемешивания в течение 1 ч твердое вещество собирали, промывали водой и сушили, при этом получали 5-(2-хлор-5-метоксифенокси)пиримидин-4,6-диол (8,65 г) в виде порошка белого цвета. 1Н-ЯМР (D6-ДМСО): 3,65 (s, 3H), 6,23 (d, J=2,7, 1H), 6,58 (dd, J=2,7, 8,8, 1H), 7,33 (d, J=8,8, 1H), 8,07 (s, 1H), 12,3 (ушир. s, 2H).
c) К раствору N,N-диметиланилина (7,5 мл) в POCl3 (75 мл) порциями добавляли 5-(2-хлор-5-метоксифенокси)пиримидин-4,6-диол (8,65 г). Раствор от темно-красного до коричневого цвета нагревали до 120°С и перемешивали в течение 3 ч. Смесь охлаждали и избыток POCl3 упаривали. Остаток обрабатывали ледяной водой (400 мл) и экстрагировали два раза этилацетатом (200 мл). Органическую фазу промывали водой и упаривали. Неочищенный продукт очищали хроматографией на колонке с силикагелем (элюент:гептан/этилацетат, 7:3). Выделенный продукт суспендировали в метаноле, фильтровали, промывали метанолом, диэтиловым эфиром/гекса