Производное циннамида типа морфолина
Иллюстрации
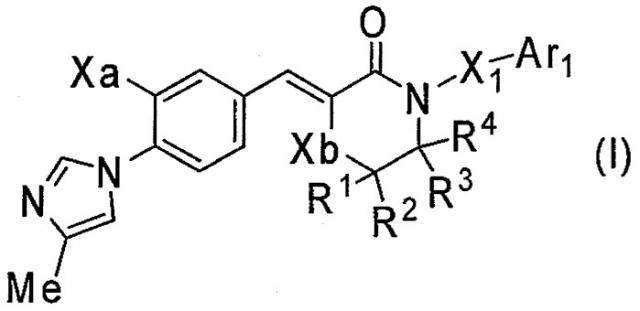
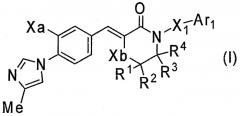
Показать всеНастоящее изобретение относится к производному циннамида типа морфолина общей формулы I или его фармакологически приемлемой соли, где (a) R1, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу; X1 представляет собой C1-6алкиленовую группу, где С1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, или С3-8циклоалкильной группой, образованной двумя С1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода С1-6алкиленовой группы; Ха представляет собой метоксигруппу или атом фтора; Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Ха представляет собой метоксигруппу; и Ar1 представляет собой арильную группу, пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы Al заместителей; (b) Ar1-X1-представляет собой С5-7циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в С5-7циклоалкильной группе может быть заменена атомом кислорода, С5-7циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами, и R1, R2, R3, R4, Ха и Xb являются такими, как определено в (a); (d) Ar1-X1- и R4, вместе с атомом азота, к которому группа Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен, образуют 5-7-членную азотсодержащую гетероциклическую группу, которая замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 5-7-членной азотсодержащей гетероциклической группе может быть заменена атомом кислорода, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы Al заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Ха являются такими, как определено в (а) и (b); группа Al заместителей: (1) атом галогена. Также настоящее изобретение относится к фармацевтической композиции, содержащей соединение формулы I, полезной при лечении болезни Альцгеймера, старческой деменции, синдрома Дауна или амилоидоза. Технический результат: получены новые производные циннамида типа морфолина, обладающие ингибирующей активностью в отношении продукции амилоида-β. 2 н. и 15 з.п. ф-лы, 9 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к производному циннамида типа морфолина и к фармацевтическому средству, содержащему данное соединение в качестве активного ингредиента. Более конкретно настоящее изобретение относится к непептидному двуядерному производному циннамида и ингибитору продукции амилоида-β (далее называемого как Aβ), который содержит данное соединение в качестве активного ингредиента и особенно эффективен при лечении нейродегенеративного заболевания, вызываемого Aβ, такого как болезнь Альцгеймера или синдром Дауна.
Предпосылки создания изобретения
Болезнь Альцгеймера является заболеванием, характеризующимся дегенерацией и потерей нейронов, а также образованием старческих бляшек и нейрофибриллярной дегенерацией. В настоящее время болезнь Альцгеймера лечат только методами симптоматической терапии с использованием средства для улучшения симптомов, типичным представителем которого является ингибитор ацетилхолинэстеразы, а фундаментальное лекарственное средство, ингибирующее прогрессирование заболевания, все еще не создано. Необходимо разработать способ контроля причины возникновения патологии, чтобы создать фундаментальное лекарственное средство для лечения болезни Альцгеймера.
Считается, что Aβ-белки в качестве метаболитов амилоидных белков-предшественников (далее называемых как APP) сильно вовлечены в процессы дегенерации и потери нейронов и возникновения симптомов деменции (см. непатентные документы 1 и 2). Aβ-белок содержит в качестве основных ингредиентов Aβ40, состоящий из 40 аминокислот, и Aβ42, в котором число аминокислот на две больше на С-конце. Известно, что Aβ40 и Aβ42 обладают высокой агрегационной способностью (см. непатентный документ 3) и являются основными составляющими старческих бляшек (см. непатентные документы 3, 4 и 5). Известно также, что Aβ40 и Aβ42 отличаются увеличенной мутацией в генах APP и пресенилина, которая наблюдается при болезни Альцгеймера семейного типа (см. непатентные документы 6, 7 и 8). Поэтому ожидается, что соединение, понижающее продукцию Aβ40 и Aβ42, будет ингибитором прогрессирования или профилактическим средством для болезни Альцгеймера.
Aβ продуцируется в результате расщепления APP β-секретазой и затем γ-секретазой. По этой причине были предприняты попытки создания ингибиторов β-секретазы и γ-секретазы, чтобы ингибировать продукцию Aβ. Многие из указанных ингибиторов секретаз уже известны, например пептиды и миметики пептидов, такие как L-685458 (см. непатентный документ 9) и LY-411575 (см. непатентные документы 10, 11 и 12).
[Непатентный документ 1] Klein WL, and seven others, Alzheimer,s disease-affected brain: Presence of oligomeric A(ligands (ADDLs) suggests a molecular basis for reversible memory loss, Proceding National Academy of Science USA 2003, Sep 2; 100(18), p.10417-10422;
[Непатентный документ 2] Nitsch RM, and sixteen others, Antibodies against β-amyloid slow cognitive decline in Alzheimer,s disease, Neuron, 2003, May 22; 38, p.547-554;
[Непатентный документ 3] Jarrett JT, and two others, The carboxy terminus of the (amyloid protein is critical for the seeding of amyloid formation: Implications for the pathogenesis of Alzheimer,s disease, Biochemistry, 1993, 32(18), p.4693-4697;
[Непатентный документ 4] Glenner GG, и one other, Alzheimer,s disease: initial report of the purification and characterization of a novel cerebrovascular amyloid protein, Biochemical and biophysical research communications, 1984, May 16, 120(3), p.885-890;
[Непатентный документ 5] Masters CL, and five others, Amyloid plaque core protein in Alzheimer disease and Down syndrome, Proceding National Academy of Science USA, 1985, Jun, 82(12), p.4245-4249;
[Непатентный документ 6] Gouras GK, and eleven others, Intraneuronal Aβ42 accumulation in human brain, American Journal of Pathology, 2000, Jan, 156(1), p.15-20;
[Непатентный документ 7] Scheuner D, and twenty others, Secreted amyloid β-protein similar to that in the senile plaques of Alzheimer,s disease is increased in vivo by the presenilin 1 and 2 and APP mutations linked to familial Alzheimer,s disease, Nature Medicine, 1996, Aug, 2(8), p.864-870;
[Непатентный документ 8] Forman MS, and four others, Differential effects of the swedish mutant amyloid precursor protein on β-amyloid accumulation and secretion in neurons and nonneuronal cells, The Journal of Biological Chemistry, 1997, Dec 19, 272(51), p.32247-32253;
[Непатентный документ 9] Shearman MS, and nine others, L-685,458, an Aspartyl Protease Transition State Mimic, Is a Potent Inhibitor of Amyloid β-Protein Precursor γ-Secretase Activity, Biochemistry, 2000, Aug 1, 39(30), p.8698-8704;
[Непатентный документ 10] Shearman MS, and six others, Catalytic Site-Directed γ-Secretase Complex Inhibitors Do Not Discriminate Pharmacologically between Notch S3 and β-APP Cleavages, Biochemistry, 2003, Jun 24, 42(24), p.7580-7586;
[Непатентный документ 11] Lanz TA, and three others, Studies of A(pharmacodynamics in the brain, cerebrospinal fluid, and plasma in young (plaque-free) Tg2576 mice using the γ-secretase inhibitor N2-[(2S)-2-(3,5-difluorophenyl)-2-hydroxyethanoyl]-N1-[(7S)-5-methyl-6-oxo-6,7-dihydro-5H-dibenzo[b,d]azepin-7-yl]-L-alaninamide (LY-411575), The journal of pharmacology and experimental therapeutics, 2004, Apr, 309(1), p.49-55;
[Непатентный документ 12] Wong GT, and twelve others, Chronic treatment with the γ-secretase inhibitor LY-411,575 inhibits β-amyloid peptide production and alters lymphopoiesis and intestinal cell differentiation, The journal of biological chemistry, 2004, Mar 26, 279(13), p.12876-12882.
Раскрытие сущности изобретения
Задачи, решаемые изобретением
Как описано выше, соединение, которое ингибирует продукцию Aβ40 и Aβ42 из APP, предполагается в качестве терапевтического или профилактического средства для заболевания, вызываемого Aβ, типичным представителем которого является болезнь Альцгеймера. Однако непептидное соединение, обладающее высокой эффективностью в отношении ингибирования продукции Aβ40 и Aβ42, все еще не известно. Следовательно, существует потребность в новом соединении с низкой молекулярной массой, которое будет ингибировать продукцию Aβ40 и Aβ42.
Средства решения указанных задач
В результате обширных исследований авторы настоящего изобретения обнаружили непептидное производное циннамида типа морфолина, которое ингибирует прежде всего продукцию Aβ40 и Aβ42 из APP, и, таким образом, разработали профилактическое или терапевтическое средство для заболевания, вызываемого Aβ, типичным представителем которого является болезнь Альцгеймера. Данная находка привела к созданию настоящего изобретения.
В частности, в соответствии с настоящим изобретением предлагаются:
1) Соединение, представленное формулой (I):
[Формула 1]
или его фармакологически приемлемая соль, где
(a) R1, R2, R3 и R4 являются одинаковыми или различными, и каждый представляет собой атом водорода или C1-6алкильную группу;
X1 представляет собой C1-6алкиленовую группу, где C1-6алкиленовая группа может быть замещена 1-3 гидроксильными группами или С1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 гидроксильными группами; или C3-13циклоалкильной группой, образованной двумя С1-6алкильными группами, вместе присоединенными к одному и тому же атому углерода C1-6алкиленовой группы;
Xa представляет собой метоксигруппу или атом фтора;
Xb представляет собой атом кислорода или метиленовую группу, при условии, что Xb представляет собой только атом кислорода, когда Xa представляет собой метоксигруппу; и
Ar1 представляет собой арильную группу, пиридинильную группу, арилоксигруппу или пиридинилоксигруппу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей;
(b) Ar1-X1- представляет собой C3-8циклоалкильную группу, конденсированную с бензольным кольцом, где одна метиленовая группа в C3-8циклоалкильной группе может быть замещена атомом кислорода, C3-8циклоалкильная группа может быть замещена 1-3 гидроксильными группами и/или C1-6алкильными группами, и бензольное кольцо может быть замещено 1-3 заместителями, выбранными из группы A1 заместителей, и R1, R2, R3, R4, Xa и Xb являются такими, как определено в (a);
(c) один из R1 и R2 и один из R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу; другой из R1 и R2 и другой из R3 и R4, вместе с атомами углерода, к которым они соответственно присоединены, образуют C3-8циклоалкильную группу, где C3-8циклоалкильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, и X1, Xa, Xb и Ar1 являются такими, как определено в (a) или (b);
(d) Ar1-X1- и R4, вместе с атомом азота, к которому группа Ar1-X1- присоединена, и атомом углерода, к которому R4 присоединен, образуют 4-8-членную азотсодержащую гетероциклическую группу, которая может быть замещена арильной группой или пиридинильной группой, где одна метиленовая группа в 4-8-членной азотсодержащей гетероциклической группе может быть замещена метиленовой группой, замещенной 1 или 2 заместителями, выбранными из группы A1 заместителей, виниленовой группой, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей, и арильная или пиридинильная группа может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, Xb представляет собой атом кислорода, и R1, R2, R3 и Xa являются такими, как определено в (a) и (b);
(e) R1 и R2, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R3, R4, X1, Xa, Xb и Ar1 являются такими, как определено в (a) и (b); или
(f) R3 и R4, вместе с атомом углерода, к которому они присоединены, образуют C3-8циклоалкильную группу, и R1, R2, X1, Xa, Xb и Ar1 являются такими, как определено в (a) и (b)
(группа А1 заместителей: (1) атом галогена, (2) гидроксильная группа, (3) цианогруппа, (4) C3-8циклоалкильная группа, (5) C3-8циклоалкоксигруппа, (6) C1-6алкильная группа, где C1-6алкильная группа может быть замещена 1-5 атомами галогена или одной-тремя C1-6алкоксигруппами, (7) аминогруппа, которая может быть замещена одной или двумя C1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-5 атомами галогена, (8) C1-6алкоксигруппа, где C1-6алкоксигруппа может быть замещена 1-5 атомами галогена, и (9) карбамоильная группа, которая может быть замещена одной или двумя C1-6алкильными группами, где C1-6алкильные группы могут быть замещены 1-3 атомами галогена);
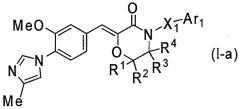
2) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (I-a):
[Формула 2]
где R1, R2, R3, R4, X1 и Ar1 являются такими, как определено выше в пункте 1);
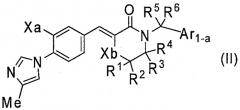
3) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (II):
[Формула 3]
где R1, R2, R3, R4, Xa и Xb являются такими, как определено выше в пункте 1), R5 и R6 являются одинаковыми или различными и каждый представляет собой атом водорода или C1-6алкильную группу, где C1-6алкильная группа может быть замещена 1-3 гидроксильными группами, и Ar1-a представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, выбранными из группы A1 заместителей, определенной выше в пункте 1);
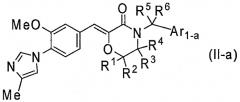
4) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-a):
[Формула 4]
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), и R5, R6 и Ar1-a являются такими, как определено выше в пункте 3);
5) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-b):
[Формула 5]
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), и R5, R6 и Ar1-a являются такими, как определено выше в пункте 3);
6) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-c):
[Формула 6]
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), R7 представляет собой атом водорода или C1-6алкильную группу и Ar1-a является таким, как определено выше в пункте 3);
7) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-d):
[Формула 7]
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), и R5, R6 и Ar1-a являются такими, как определено выше в пункте 3);
8) Соединение или его фармакологически приемлемая соль по пункту 3) выше, где соединение представлено формулой (II-e):
[Формула 8]
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), Ar1-a является таким, как определено выше в пункте 3), и R7 является таким, как определено выше в пункте 6);
9) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (I-b):
[Формула 9]
где R1, R2, R3 и R4 являются такими, как определено выше в пункте 1), R13 и R14 являются одинаковыми или различными и каждый представляет собой атом водорода или заместитель, выбранный из группы A1 заместителей, определенной выше в пункте 1), и Y представляет собой метиленовую группу или атом кислорода;
10) Соединение или его фармакологически приемлемая соль по пункту 9) выше, где R13 и R14 являются одинаковыми или различными и каждый представляет собой атом водорода, атом галогена или C1-6алкоксигруппу;
11) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение представлено формулой (I-c):
[Формула 10]
где R1 и R2 являются такими, как определено выше в пункте 1), Ar1-c представляет собой фенильную группу или пиридинильную группу, которая может быть замещена 1-3 заместителями, которые являются одинаковыми или различными и выбраны из группы A1 заместителей, Z1 представляет собой метиленовую группу или виниленовую группу, которая может быть замещена 1 или 2 заместителями, выбранными из группы A1 заместителей, определенной выше в пункте 1), атомом кислорода или иминогруппой, которая может быть замещена заместителем, выбранным из группы A1 заместителей,
и n и m являются одинаковыми или различными и каждый представляет собой целое число от 0 до 2;
12) Соединение или его фармакологически приемлемая соль по пункту 11) выше, где Z1 представляет собой метиленовую группу, где метиленовая группа может быть замещена 1 или 2 заместителями, которые являются одинаковыми или различными и выбраны из группы, состоящей из C1-6алкильной группы и гидроксильной группы, и n и m, каждый, равен 1;
13) Соединение или его фармакологически приемлемая соль по пункту 11) выше, где Z1 представляет собой атом кислорода, и n и m равно целому числу 1;
14) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где Ar1 представляет собой арильную группу или пиридинильную группу, или арильную группу или пиридинильную группу, замещенную 1-3 атомами галогена;
15) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где Ar1 представляет собой фенильную группу или пиридинильную группу, или фенильную группу или пиридинильную группу, замещенную 1-3 атомами галогена;
16) Соединение или его фармакологически приемлемая соль по пункту 1) выше, где соединение выбрано из следующей группы, включающей:
1) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(3,4,5-трифторбензил)морфолин-3-он,
2) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-(2,3,4-трифторбензил)морфолин-3-он,
3) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
4) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(3,4,5-трифторбензил)морфолин-3-он,
5) (Z)-(S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
6) (Z)-(R)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-(2,3,4-трифторбензил)морфолин-3-он,
7) (Z)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
8) (Z)-(R)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
9) (Z)-(S)-4-[(S)-1-(4-фторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
10) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
11) (Z)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(R)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
12) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
13) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
14) (Z)-(R)-4-[(S)-хроман-4-ил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
15) (Z)-(6S,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
16) (Z)-(6R,9aS)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
17) (Z)-(S)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
18) (Z)-(S)-4-[(R)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
19) (Z)-(S)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
20) (Z)-(S)-4-[(R)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
21) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
22) (Z)-(S)-4-[(R)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
23) (Z)-(S)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
24) (Z)-(S)-4-[(R)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
25) (Z)-(S)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
26) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
27) (Z)-4-[(R)-1-(4-фторфенил)-2-гидроксиэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
28) (Z)-(6R)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
29) (Z)-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
30) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]морфолин-3-он,
31) (Z)-(S)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
32) (Z)-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
33) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
34) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-метокси-4-(метилимидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
35) (Z)-(S)-4-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
36) (Z)-(6S)-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метил-4-[(S)-1-(3,4,5-трифторфенил)этил]морфолин-3-он,
37) (Z)-(6S)-4-[1-(4-фторфенил)-1-метилэтил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
38) (Z)-(6S)-4-[1-(4-фторфенил)циклопропил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
39) (Z)-(6S,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)гексагидропиридо[2,1-c][1,4]оксазин-4-он,
40) (Z)-(6S,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
41) (Z)-(6S,9aR)-6-(2,6-дифторпиридин-3-ил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]гексагидропиридо[2,1-c][1,4]оксазин-4-он,
42) (Z)-(S)-4-[(S)-1-(5-фторпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
43) (Z)-(S)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
44) (Z)-(S)-4-[(S)-1-(2-хлор-3-фторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
45) (Z)-(S)-4-[(S)-1-(2,6-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
46) (Z)-4-[(S)-1-(2-хлорпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
47) (Z)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
48) (Z)-4-[(S)-1-(6-фторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
49) (Z)-4-[(S)-1-(6-хлорпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
50) (Z)-4-[(S)-1-(2,3-дифторпиридин-4-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
51) (Z)-4-[(S)-1-(5-хлорпиридин-2-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
52) (Z)-(R)-4-[(S)-1-(2,6-дифторпиридин-3-ил)этил]-2-[1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
53) (Z)-(S)-4-(4-фторбензил)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
54) (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(S)-1-(4-трифторфенил)этил]-6,6-диметилморфолин-3-он,
55) (Z)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
56) (Z)-(S)-4-[(S)-хроман-4-ил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
57) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6-метилморфолин-3-он,
58) (Z)-(S)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6-метилморфолин-3-он,
59) (Z)-(S)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-1-(4-фторфенил)-2-гидроксипропил]-6-метилморфолин-3-он,
60) (Z)-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-4-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-6,6-диметилморфолин-3-он,
61) (Z)-4-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-2-[1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден]-6,6-диметилморфолин-3-он,
62) 1-[1-(2,4-дифторфенил)этил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]-(E)-метилиден}пиперидин-2-он,
63) (E)-(S)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
64) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]пиперидин-2-он,
65) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(2R,3R)-3-гидрокси-1,1-диметилиндан-2-ил]пиперидин-2-он,
66) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(S)-2-гидрокси-1-метил-1-(3,4,5-трифторфенил)этил]пиперидин-2-он,
67) (E)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[1-(4-фторфенил)-1-метилэтил]пиперидин-2-он,
68) (E)-(R)-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-1-[(1R,2R)-2-гидрокси-1-(3,4,5-трифторфенил)пропил]-5-метилпиперидин-2-он,
69) (E)-(S)-1-[(1R,2R)-1-(3,4-дифторфенил)-2-гидроксипропил]-3-{1-[3-фтор-4-(4-метил-1H-имидазол-1-ил)фенил]метилиден}-5-метилпиперидин-2-он,
70) (Z)-(6S,8aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)бензилиден]-6-(3,4,5-трифторфенил)тетрагидропирроло[2,1-c][1,4]оксазин-4-он,
71) (6S,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}гексагидропиридо[2,1-c][1,4]оксазин-4-он,
72) (6R,9aR)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}-6-(3,4,5-трифторфенил)-тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он,
73) (6R,9aR)-6-(3,4-дифторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он,
74) (6R,9aR)-6-(4-фторфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c][1,4]оксазин-4-он и
75) (6R,9aR)-6-(4-хлорфенил)-3-{1-[3-метокси-4-(4-метил-1H-имидазол-1-ил)фенил]-(Z)-метилиден}тетрагидро[1,4]оксазино[3,4-c]оксазин-4-он;
17) Фармацевтическое средство, содержащее соединение или его фармакологически приемлемую соль по любому из пунктов 1)-16) выше в качестве активного ингредиента;
18) Фармацевтическое средство по пункту 17) выше для предупреждения или лечения заболевания, вызываемого амилоидом-β, и
19) Фармацевтическое средство по пункту 18) выше, где заболеванием, вызываемым амилоидом-β, является болезнь Альцгеймера, старческая деменция, синдром Дауна или амилоидоз.
Соединение общей формулы (I) или его фармакологически приемлемая соль по настоящему изобретению и профилактическое или терапевтическое средство для заболевания, вызываемого Aβ, по настоящему изобретению являются новыми и не описаны в каких-либо публикациях.
Далее объяснено применение значений, терминов и тому подобное, используемых в данном описании, и настоящее изобретение описано более подробно.
В данном описании структурная формула соединения может для удобства представлять какой-либо изомер. Однако настоящее изобретение включает все изомеры и изомерные смеси, такие как геометрические изомеры, которые могут образовываться в связи со структурой соединения, оптические изомеры, образование которых основано на наличии асимметричного атома углерода, стереоизомеры и таутомеры. Настоящее изобретение не ограничивается описанием выбранной из соображений удобства химической формулы и может охватывать любой из изомеров или их смеси. Соответственно, соединение по настоящему изобретению может иметь в молекуле асимметричный углеродный атом и существовать в виде оптически активного соединения или рацемата, и настоящее изобретение включает, но без ограничений, как оптически активное соединение, так и рацемат. Хотя могут существовать кристаллические полиморфы соединения, данное соединение не ограничивается ими и может существовать в форме монокристалла или смеси монокристаллов. Соединение может быть негидратированным или гидратом.
“Заболевание, вызываемое Aβ” относится к широкому кругу заболеваний, таких как болезнь Альцгеймера (см., например, Klein WL, and seven others, Alzheimer's disease-affected brain: Presence of oligomeric A(ligands (ADDLs) suggests a molecular basis for reversible memory loss, Proceding National Academy of Science USA, 2003, Sep 2, 100(18), p.10417-10422; Nitsch RM, and sixteen others, Antibodies against β-amyloid slow cognitive decline in Alzheimer's disease, Neuron, 2003, May 22, 38(4), p.547-554; Jarrett JT, and two others, The carboxy terminus of the (amyloid protein is critical for the seeding of amyloid formation: Implications for the pathogenesis of Alzheimer's disease, Biochemistry, 1993, May 11, 32(18), p.4693-4697; Glenner GG, and one other, Alzheimer's disease а: initial report of the purification and characterization of a novel cerebrovascular amyloid protein, Biochemical and biophysical research communications, 1984, May 16, 120(3), p.885-890; Masters CL, and six others, Amyloid plaque core protein in Alzheimer disease and Down syndrome, Proceding National Academy of Science USA, 1985, June, 82(12), p.4245-4249; Gouras GK, and eleven others, Intraneuronal Aβ42 accumulation in human brain, American journal of pathology, 2000, Jan, 156(1), p.15-20; Scheuner D, and twenty others, Secreted amyloid β-protein similar to that in the senile plaques of Alzheimer's disease is increased in vivo by the presenilin 1 and 2 and APP mutations linked to familial Alzheimer's disease, Nature Medicine, 1996, Aug, 2(8), p.864-870; and Forman MS, and four others, Differential effects of the swedish mutant amyloid precursor protein on β-amyloid accumulation and secretion in neurons and nonneuronal cells, The journal of biological chemistry, 1997, Dec 19, 272(51), p.32247-32253), старческая деменция (см., например, Blass JP, Brain metabolism and brain disease: Is metabolic deficiency the proximate cause of Alzheimer dementia? Journal of Neuroscience Research, 2001, Dec 1, 66(5), p.851-856), лобно-височная деменция (см., например, Evin G, and eleven others, Alternative transcripts of presenilin-1 associated with frontotemporal dementia, Neuroreport, 2002, Apr 16, 13(5), p.719-723), болезнь Пика (см., например, Yasuhara O, and three others, Accumulation of amyloid precursor protein in brain lesions of patients with Pick disease, Neuroscience Letters, 1994, Apr 25, 171(1-2), p.63-66), синдром Дауна (см., например, Teller JK, and ten others, Presence of soluble amyloid β-peptide precedes amyloid plaque formation in Down's syndrome, Nature Medicine, 1996, Jan, 2(1), p.93-95; and Tokuda T, and six others, Plasma levels of amyloid (proteins Aβ1-40 and Aβ1-42(43) are elevated in Down's syndrome, Annals of Neurology, 1997, Feb, 41(2), p.271-273), церебральная ангиопатия (см., например, Hayashi Y, and nine others, Evidence for presenilin-1 involvement in amyloid angiopathy in the Alzheimer's disease-affected brain, Brain Research, 1998, Apr 13, 789(2), p.307-314; Barelli H, and fifteen others, Characterization of new polyclonal antibodies specific for 40 and 42 amino acid-long amyloid (peptides: their use to examine the cell biology of presenilins and the immunohistochemistry of sporadic Alzheimer's disease and cerebral amyloid angiopathy cases, Molecular Medicine, 1997, Oct, 3(10), p.695-707; Calhoun ME, and ten others, Neuronal overexpression of mutant amyloid precursor protein results in prominent deposition of cerebrovascular amyloid, Proceding National Academy of Science USA, 1999, Nov 23, 96(24), p.14088-14093; and Dermaut B, and ten others, Cerebral amyloid angiopathy is a pathogenic lesion in Alzheimer's Disease due to a novel presenilin-1 mutation, Brain, 2001, Dec, 124(12), p.2383-2392), наследственная церебральная геморрагия с амилоидозом (голландского типа) (см., например, Cras P, and nine others, Presenile Alzheimer dementia characterized by amyloid angiopathy and large amyloid core type senile plaques in the APP 692Ala -->Gly mutation, Acta Neuropathologica (Berl), 1998, Sep, 96(3), p.253-260; Herzig MC, and fourteen others, A(is targeted to the vasculature in a mouse model of hereditary cerebral hemorrhage with amyloidosis, Nature Neuroscience, 2004, Sep, 7(9), p.954-960; van Duinen SG, and five others, Hereditary cerebral hemorrhage with amyloidosis in patients of Dutch origin is related to Alzheimer disease, Proceding National Academy of Science USA, 1987, Aug, 84(16), p.5991-5994; and Levy E, and eight others, Mutation of the Alzheimer's disease amyloid gene in hereditary cerebral hemorrhage, Dutch type, Science, 1990, Jun 1, 248(4959), p.1124-1126), когнитивное нарушение (см., например, Laws SM, and seven others, Association between the presenilin-1 mutation Glu318Gly and complaints of memory impairment, Neurobiology of Aging, 2002, Jan-Feb, 23(1), p.55-58), нарушение памяти и неспособность к обучению (см., например, Vaucher E, and five others, Object recognition memory and cholinergic parameters in mice expressing human presenilin 1 transgenes, Experimental Neurology, 2002 Jun, 175(2), p.398-406; Morgan D, and fourteen others, A(peptide vaccination prevents memory loss in an animal model of Alzheimer's disease, Nature, 2000 Dec 21-28, 408(6815), p.982-985; and Moran PM, and three others, Age-related learning deficits in transgenic mice expressing the 751-amino acid isoform of human β-amyloid precursor protein, Proceding National Academy of Science USA, 1995, June 6, 92(12), p.5341-5345), амилоидоз, церебральная ишемия (см., например, Laws SM, and seven others, Association between the presenilin-1 mutation Glu318Gly and complaints of memory impairment, Neurobiology of Aging, 2002, Jan-Feb, 23(1), p.55-58; Koistinaho M, and ten others, β-amyloid precursor protein transgenic mice that harbor diffuse A(deposits but do not form plaques show increased ischemic vulnerability: Role of inflammation, Proceding National Academy of Science USA, 2002, Feb 5, 99(3), p.1610-1615; and Zhang F, and four others, Increased susceptibility to ischemic brain damage in transgenic mice overexpressing the amyloid precursor protein, The journal of neuroscience, 1997, Oct 15, 17(20), p.7655-7661), сосудистая деменция (см., например, Sadowski M, and six others, Links between the pathology of Alzheimer's disease and vascular dementia, Neurochemical Research, 2004, Jun, 29(6), p.1257-1266), офтальмоплегия (см., например, O'Riordan S, and seven others, Presenilin-1 mutation (E280G), spastic paraparesis, and cranial MRI white-matter abnormalities, Neurology, 2002, Oct 8, 59(7), p.1108-1110), рассеянный склероз (см., например, Gehrmann J, and four others, Amyloid precursor protein (APP) expression in multiple sclerosis lesions, Glia, 1995, Oct, 15(2), p.141-51; and Reynolds WF, and six others, Myeloperoxidase polymorphism is associated with gender specific risk for Alzheimer's disease, Experimental Neurology, 1999, Jan, 155(1), p.31-41), травма головы, краниальная травма (см., например, Smith DH, and four others, Protein accumulation in traumatic brain injury, NeuroMolecular Medicine, 2003, 4(1-2), p.59-72), апраксия (см., например, Matsubara-Tsutsui M, and seven others, Molecular evidence of presenilin 1 mutation in familial early onset dementia, American journal of Medical Genetics, 2002, Apr 8, 114(3), p.292-298), первичное заболевание, семейная амилоидная нейропатия, болезнь повтора триплетов (см., например, Kirkitadze MD, and two others, Paradigm shifts in Alzheimer's disease and other neurodegenerative disorders: the emerging role of oligomeric assemblies, Journal of Neuroscience Research, 2002, Sep 1, 69(5), p.567-577; Evert BO, and eight others, Inflammatory genes are upreglulated in expanded ataxin-3-expressing cell lines and spinocerebellar ataxia type 3 brains, The Journal of Neuroscience, 2001, Aug 1, 21(15), p.5389-5396; and Mann DM, and one other, Deposition of amyloid(A4) protein within the brains of persons with dementing disorders other than Alzheimer's disease and Down's syndrome, Neuroscience Letters, 1990, Feb 5, 109(1-2), p.68-75), болезнь Паркинсона (см., например, Primavera J, and four others, Brain accumulation of amyloid-(in Non-Alzheimer Neurodegeneration, Journal of Alzheimer's Disease, 1999, Oct, 1(3), p.183-193), деменция с тельцами Леви (см., например, Giasson BI, and two others, Interactions of amyloidogenic proteins. NeuroMolecular Medicine, 2003, 4(1-2), p.49-58; Masliah E, and six others, β-amyloid peptides enhance α-synuclein accumulation and neuronal deficits in a trancgenic mouse model linking Alzheimer's disease and Parkinson's disease, Proceding National Academy of Science USA, 2001, Oct 9, 98(21), p.12245-12250; Barrachina M, and six others, Amyloid-(deposition in the cerebral cortex in Dementia with Lewy bodies is accompanied by a relative increase in AβPP mRNA isoforms containing the Kunitz protease inhibitor, Neurochemistry International, 2005, Feb, 46(3), p.253-260; and Primavera J, and four others, Brain accumulation of amyloid-(in Non-Alzheimer Neurodegeneration, Journal of Alzheimer's Disease, 1999, Oct, 1(3), p.183-193), комплекс паркинсонизм-деменция (см., например, Schmidt ML, and six others, Amyloid plaques in Guam amyotrophic lateral sclerosis/ parkinsonism-dementia complex contain species of A(similar to those found in the amyloid plaques of Alzheimer's disease and pathological aging, Acta Neuropathologica (Berl), 1998, Feb, 95(2), p.117-122; and Ito H, and three others, Demonstration of (amyloid protein-containing neurofibrillary tangles in parkinsonism-dementia complex on Guam, Neuropathology and applied neurobiology, 1991, Oct, 17(5), p.365-373), лобно-височная деменция и паркинсонизм, связанный с хромосомой 17 (см., например, Rosso SM, and three others, Coexistent tau and amyloid pathology in hereditary frontotemporal dementia with tau mutations, Annals of the New York academy of sciences, 2000, 920, p.115-119), деменция с аргирофильными зернами (см., например, Tolnay M, and four others, Low amyloid (Aβ) plaque load and relative predominance of diffuse plaques distinguish argyrophilic grain disease from Alzheimer's disease, Neuropathology and applied neurobiology, 1999, Aug, 25(4), p.295-305), болезнь Ниманна-Пика (см., например, Jin LW, and three others, Intracellular accumulation of amyloidogenic fragments of amyloid-(precursor protein in neurons with Niemann-Pick type C defects is associated with endosomal abnormalities, American Journal of Pathology, 2004, Mar, 164(3), p.975-985), боковой амиотрофический склероз (см., например, Sasaki S, and one other, Immunoreactivity of β-amyloid precursor protein in amyotrophic lateral sclerosis, Acta Neuropathologica(Berl), 1999, May, 97(5), p.463-468; Tamaoka A, and four others, Increased amyloid (protein in the skin of patients with amyotrophic lateral sclerosis, Journal of neurology, 2000, Aug, 247(8), p.633-635; Hamilton RL, and one other, Alzheimer disease pathology in amyotrophic lateral sclerosis, Acta Neuropathologica, 2004, Jun, 107(6), p.515-522; and Turner BJ, and six others, Brain β-amyloid accumulation in transgenic mice expressing mutant superoxide dismutase 1, Neurochemical Research, 2004, Dec, 29(12), p.2281-2286), гидроцефалия (см., например, Weller RO, Pathology of cerebrospinal fluid and interstitial fluid of the CNS: Significance for Alzheimer disease, prior disorders and multiple sclerosis, Journal of Neuropathology and Experimental Neurology, 1998, Oct, 57(10), p.885-894; Silverberg GD, and four others, Alzheimer's disease, normal-pressure hydrocephalus, and senescent changes in CSF circulatory physiology: a hypothesis, Lancet neurology, 2003, Aug, 2(8), p.506-511; Weller RO, and three others, Cerebral amyloid angiopathy: Accumulation of A(in interstitial fluid drainage pathways in Alzheimer's disease, Annals of the New York academy of sciences, 2000, Apr, 903, p.110-117; Yow HY, and one other, A role for cerebrovascular disease in determining the pattern of β-amyloid deposition in Alzheimer's disease, Neurology and applied neurobiology, 2002, 28, p.149; and Weller RO, and four others, Cerebrovasculardisease is a major factor in the failure of elimination of A(from the aging human brain, Annals of the New York academy of sciences, 2002, Nov, 977, p.162-168), парапарез (см., например, O'Riordan S, and seven others, Presenilin-1 mutation (E280G), spastic paraparesis, and cranial MRI white-matter abnormalities, Neurology, 2002, Oct 8, 59(7), p.1108-1110; Matsubara-Tsutsui M, and seven others, Molecular evidence of presenilin 1 mutation in familial early onset dementia, American journal of Medical Genetics, 2002, Apr 8, 114(3), p.292-298; Smith MJ, and eleven others, Variable phenotype of Alzheimer's disease with spastic paraparesis, Annals of Neurology, 2001, 49(1), p.125-129; and Crook R, and seventeen others, A variant of Alzheimer's disease with spastic pararesis and unusual plaques due to deletion of exon 9 of presenilin 1, Nature Medicine, 1998, Apr; 4(4), p.452-455), прогрессивный супрануклеарный паралич (см., например, Barrachina M, and six others, Amyloid-(deposition in the cerebral cortex in Dementia with Lewy bodies is accompanied by a relative increase in AβPP mRNA isoforms containing the Kunitz protease inhibitor, Neurochemistry International, 2005, Feb, 46(3), p.253-260; and Primavera J, and four others, Brain accumulation of amyloid-(in Non-Alzheimer Neurodegeneration, Jornal of Alzheimer's Disease, 1999, Oct, 1(3), p.183-193), внутримозговое кровоизлияние (см., например, Atwood CS, and three others, Cerebrovascular requirement for sealant, anti-coagulant and remodeling molecules that allow for the maintenance of vascular integrity and blood supply, Brain Research Reviews, 2003, Sep, 43(1), p.164-78; and Lowenson JD, and two others, Protein aging: Extracellular amyloid formation and intracellular repair, Trends in cardiovascular medicine, 1994, 4(1), p.3-8), конвульсия (см., например, Singleton AB, and thirteen others, Pathology of early-onset Alzheimer's disease cases bearing the Thr113-114ins presenilin-1 mutation, Brain, 2000, Dec, 123(Pt12), p.2467-2474), легкое когнитивное нарушение (см., например, Gattaz WF, and four others, Platelet phospholipase A2 activity in Alzheimer's disease and mild cognitive impairment, Journal of Neural Transmission, 2004, May, 111(5), p.591-601; and Assini A, and fourteen others, Plasma levels of amyloid β-protein 42 are increased in women with mild cognitive impariment, Neurology, 2004, Sep 14, 63(5), p.828-831) и артериосклероз (см., например, De Meyer GR, and eight others, Platelet phagocytosis and processing of β-amyloid precursor protein as a mechanism of macrophage activation in atherosclerosis, Circulation Reserach, 2002, Jun 14, 90(11), p.1197-1204).
"C1-6алкиленовая группа" относится к алкиленовой группе, содержащей 1-6 углеродных атомов. Предпочтительные примеры группы включают метиленовую группу, этиленовую группу, пропиленовую группу, бутиленовую группу и пентиленовую группу.
“C1-6алкильная группа" относится к алкильной группе, содержащей 1-6 углеродных атомов. Предпочтительные примеры группы включают неразветвленные или разветвленные алкильные группы, такие как метильная группа, этильная группа, н-пропильная группа, изопропильная группа, н-бутильная группа, изобутильная группа, трет-бутильная группа, н-пентильная группа, изопентильная группа, неопентильная группа, н-гексильная группа, 1-метилпропильная группа, 1,2-диметилпропильная группа, 1-этилпропильная группа, 1-метил-2-этилпропильная группа, 1-этил-2-метилпропильная группа, 1,1,2-триметилпропильная группа, 1-метилбутильная группа, 2-метилбутильная группа, 1,1-диметилбутильная группа, 2,2-диметилбутильная группа, 2-этилбутильная группа, 1,3-диметилбутильная группа, 2-метилпентильная группа и 3-метилпентильная группа.
“C3-13циклоалкильная группа” относится к циклической алкильной группе, содержащей 3-13 углеродных атомов. Предпочтительные примеры группы включают циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, циклогептильную группу, циклооктильную группу, циклононанильную группу, циклодеканильную группу, циклоундеканильную группу, циклододеканильную группу и циклотридеканильную группу.
“Арильная группа” относится к "6-14-членной ци