Новые цис-имидазолины
Иллюстрации
Показать всеНастоящее изобретение относится к соединениям формулы (I) и их фармацевтически приемлемым солям. Соединения настоящего изобретения обладают ингибирующей активностью в отношении взаимодействия MDM2 - р-53. В формуле (I)
R означает насыщенное 6-членное кольцо, содержащее один или два гетероатома азота и замещенное группой, выбранной из следующих групп: (низш.)алкил, -C(O)-R1, (низш.)алкил, замещенный группой -SO2-(низш.)алкил, (низш.)алкил, замещенный группой -C(O)-R1, -SO2-(низш.)алкил, или 5-членное насыщенное кольцо, содержащее один гетероатом азота, R1 выбирают из группы, включающей (низш.)алкил, -N((низш.)алкил)2, или R1 означает 6-членное насыщенное кольцо, содержащее два гетероатома, выбранных из N и О, X1 и Х2 независимо выбирают из группы, включающей водород, (низш.)алкокси, каждый Y1 и Y2 независимо выбирают из группы, включающей -Сl и -Вr, и абсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию соответственно. Изобретение также относится к фармацевтической композиции, обладающей ингибирующей активностью в отношении взаимодействия MDM2 - р-53, содержащей эффективное количество соединения изобретения. 3 н. и 9 з.п. ф-лы, 1 табл.
Реферат
Настоящее изобретение относится к хиральным цис-имидазолинам, которые являются низкомолекулярными ингибиторами взаимодействия MDM2-р53. Фактор р53 является подавляющим опухоль белком, который играет ключевую роль в защите от развития рака. Указанный белок способствует сохранению целостности клетки и предотвращает распространение необратимо поврежденных клеточных клонов за счет индукции остановки роста клеток или апоптоза. На молекулярном уровне белок р53 является фактором транскрипции, который активирует ряд генов, включенных в регуляцию клеточного цикла и апоптоза. Белок р53 является активным ингибитором клеточного цикла, который на клеточном уровне строго регулируется MDM2. MDM2 и р53 образуют петлю регуляции обратной связи. MDM2 связывается с белком р53 и ингибирует его способность трансактивировать гены, регулируемые р53. Кроме того, MDM2 опосредует убиквитин-зависимую деградацию р53. Белок р53 активирует экспрессию гена MDM2, таким образом повышая концентрацию белка MDM2 в клетках. Указанная петля регуляции обратной связи обеспечивает низкие концентрации MDM2 и р53 в нормальных пролиферирующих клетках. MDM2 является также кофактором для E2F, который играет ключевую роль в регуляции клеточного цикла.
Нарушение соотношения MDM2 и р53 (E2F) наблюдается во многих случаях рака. Установлено, что в большинстве случаев наблюдаемые молекулярные дефекты в локусе p16INK4/p19ARF действуют, например, на деградацию белка MDM2. Ингибирование взаимодействия MDM2-p53 в опухолевых клетках (содержащих белок р53 дикого типа) приводит к накоплению р53, остановке клеточного роста и/или апоптозу. В связи с этим, антагонисты MDM2 представляют новый подход для лечения рака, и их можно использовать в качестве отдельных агентов или в комбинации с широким спектром других противоопухолевых терапевтических средств. Перспективность указанной стратегии установлена при использовании различных макромолекулярных средств ингибирования взаимодействия MDM2-p53 (например, антител, антисмысловых олигонуклеотидов, пептидов). MDM2 связывается также с E2F в консервативном участке связывания, аналогично р53, и активирует Е2F-зависимую транскрипцию циклина А, что позволяет предположить о воздействии антагонистов MDM2 на клетки, содержащие мутант белка р53.
В статье Wells и др., J. Org. Chem., т.37, с.2158-2161 (1972) описан синтез имидазолинов. В статье Hunter и др., Can. J. Chem., т.50, с.669-77 (1972) описано получение амариновых и изоамариновых соединений, хемилюминесцентные свойства которых изучены ранее (МсСарrа и др., Photochem. and Photobiol., т.4, c.1111-1121 (1965)). В статье Zupanc и др., Bull. Soc. Chem. & Tech. (Yugoslavia), 27/28, c. 71-80 (1980-81) описано применение триарилимидазолинов в качестве исходных соединений для получения производных ЭДТУ.
В европейском патенте ЕР 363061 (Matsumoto) описаны производные имидазолина, которые можно использовать в качестве иммуномодуляторов. Установлено, что указанные соединения характеризуются низкой токсичностью. В связи с этим указана возможность лечения и/или профилактики ревматоидного артрита, рассеянного склероза, системной красной волчанки, эритематоза и ревматизма. В заявке WO 00/78725 (Choueiry и др.) описан способ получения замещенных амидиновых соединений и указано, что соединения имидазолинового типа можно использовать для лечения диабета или связанных с ним заболеваний, включая нарушение утилизации глюкозы.
В патенте США №6617346 В1, опубликованном 9 сентября 2003, и в патенте США №6734302 В2, опубликованном 11 мая 2004, описаны родственные рацемические цис-имидазолины. В патенте США №6734302 В2 прежде всего описан родственный широкий класс рацемических соединений, который в основном включает соединения, заявленные в настоящем изобретении, за исключением хиральности и узкого класса соединений по настоящему изобретению.
В настоящем изобретении предлагается по крайней мере одно соединение формулы I
где X1, Х2, Y1, Y2 и R имеют значения, как определено в данном контексте, а также его фармацевтически приемлемые соли и сложные эфиры.
В настоящем изобретении предлагаются хиральные цис-имидазолины, которые являются низкомолекулярными ингибиторами взаимодействия MDM2-р53. По данным бесклеточного анализа и анализа с использованием клеток установлено, что соединения по настоящему изобретению ингибируют взаимодействие белка MDM2 с р53-подобным пептидом, причем указанная ингибирующая активность приблизительно в 100 раз выше по сравнению с ингибирующей активностью пептидного фрагмента р53. Данные анализа с использованием клеток свидетельствуют о том, что указанные соединения проявляют механистическую активность. Инкубирование раковых клеток, содержащих белок р53 дикого типа, приводит к накоплению белка р53, индукции гена р21, регулируемого р53, и к остановке клеточного цикла в фазах G1 и G2, что указывает на высокую антипролиферативную активность in vitro в отношении клеток, содержащих р53 дикого типа. И, наоборот, указанный тип активности не наблюдается в раковых клетках, содержащих мутант р53 при сравнительно низких концентрациях соединения. Следовательно, можно предположить, что активность антагонистов MDM2 обусловлена их механизмом действия. Указанные соединения являются активными и селективными противоопухолевыми агентами.
В настоящем изобретении предлагается по крайней мере одно соединение формулы I и его фармацевтически приемлемые соли и сложные эфиры,
где:
R означает насыщенное или ненасыщенное 5-6-членное кольцо, содержащее по крайней мере один гетероатом, выбранный из S, N и О, и
необязательно замещенное группой, выбранной из следующих групп: (низш.)алкил, циклоалкил, -C(O)-R1, гидрокси, (низш.)алкил, замещенный группой гидрокси, (низш.)алкил, замещенный группой (низш.)алкокси, (низш.)алкил, замещенный группой -NH2, (низш.)алкил, замещенный группой -SO2-(низш.)алкил, (низш.)алкил, замещенный группой -C(O)-R1, -NH-(низш.)алкил, -N((низш.)алкил)2, -SO2-(низш.)алкил, =O, -СН2С(O)СН3, или 5-6-членное насыщенное кольцо, содержащее один, два или три гетероатома, выбранных из S, N и О,
R1 выбирают из группы, включающей водород, (низш.)алкил, -NH2, -NH-(низш.)алкил, -N((низш.)алкил)2, (низш.)алкил, замещенный группой гидрокси, (низш.)алкил, замещенный группой -NH2, или R1 означает 5-6-членное насыщенное кольцо, содержащее один, два или три гетероатома, выбранных из S, N и O,
X1 и Х2 независимо выбирают из группы, включающей водород, (низш.)алкокси,
-СН2ОСН3, -СH2ОСН2СН3, -ОСН2СF3, -OCH2CH2F,
каждый Y1 и Y2 независимо выбирают из группы, включающей -Сl, -Вr, -NO2, -C≡N и -С≡СН, и
абсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию соответственно (как показано в формуле I).
В одном предпочтительном варианте осуществления настоящего изобретения предлагается по крайней мере одно соединение, выбранное из соединения формулы I
и его фармацевтически приемлемых солей и сложных эфиров, где
R выбирают из насыщенного и ненасыщенного 5- и 6-членного кольца, содержащего по крайней мере один гетероатом, причем гетероатом выбирают из S, N и О, и необязательно замещенного группой, выбранной из следующих групп: (низш.)алкил, циклоалкил, (низш.)алкил, замещенный группой гидрокси, (низш.)алкил, замещенный группой -NH2, N-(низш.)алкил, -SО2СН3, =O, -СН2С(O)СН3, а также из 5- и 6-членных насыщенных колец, содержащих по крайней мере один гетероатом, выбранный из S, N и О,
X1 и X2 независимо выбирают из группы, включающей водород, (низш.)алкокси,
-СН2ОСН3, -СН2ОСH2СН3, -ОСН2СF3, -OCH2CH2F,
каждый Y1 и Y2 независимо выбирают из группы, включающей -Сl, -Вr, -NO2, -C≡N и -С≡СН, и
абсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию соответственно (как показано в формуле I).
Другими предпочтительными соединениями являются соединения формулы I, где каждый Y1 и Y2 независимо выбирают из -Сl и -Вr.
Кроме того, предпочтительными соединениями являются соединения формулы I, где R означает пиперазинил, замещенный по крайней мере одной группой, выбранной из следующих групп: (низш.)алкил, циклоалкил, C(O)-R1, (низш.)алкил, замещенный группой гидрокси, (низш.)алкил, замещенный группой -NH2, (низш.)алкил, замещенный группой -C(O)-R1, N-(низш.)алкил, -SO2СН3, =O, -СН2С(O)СН3, или пиперидинил, замещенный по крайней мере одной группой, выбранной из следующих групп: С1-С3алкил, -С1-С2алкокси, -С(O)СН3, -SO2СН3, -С(O), -ОН, -CH2NH2,
-C(O)CH2NH2, -С(O)СН2OН, -С(O)С(ОН)СН2OН, -СН2С(ОН)СН2OН,
-C(O)N(CH2)2, -C(O)NH2 и -C(O)N(CH3)CH3, -N(СН3)СН3, пирролидинил и пиперидинил.
Предпочтительны также соединения формулы I, где группу X1, расположенную в орто-положении, выбирают из следующих групп: (низш.)алкокси, -ОСH2СF3 и
-OCH2CH2F, а группа Х2, расположенная в пара-положении, означает (низш.)алкокси.
В других предпочтительных соединениях группу X1, расположенную в орто-положении, выбирают из следующих групп: этокси, изопропокси, -ОСН2СF3 и
-OCH2CH2F, а группу Х2, расположенную в пара-положении, выбирают из метокси и этокси.
В еще одном предпочтительном варианте осуществления настоящего изобретения предлагаются соединения формулы I-A и их фармацевтически приемлемые соли
где:
R означает пиперазинил или пиперидинил, замещенный следующими группами:
С1-С4алкил, -С(O)-(С1-С4алкил), пирролидин-1-ил, =O, -CH2-C(O)-морфолино,
-СН2-С(O)-N(С1-С4алкил)2, -(СH2)n-SО2-(С1-C4алкил),
X1 означает -O-(С1-С4алкил),
Х2 означает водород или -O-(С1-С4алкил),
n равно 0, 1 или 2, и
абсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию соответственно.
Кроме того, предпочтительны соединения формулы I, где R выбирают из пиперазинила и замещенного пиперазинила.
Указанные соединения включают, например:
1-{4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанон,
4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-2-он,
[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-ил]-(4-пирролидин-1-илпиперидин-1-ил)метанон,
4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-2-он,
1-{4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанон,
2-{4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}-1-морфолин-4-илэтанон,
[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-ил][4-(2-метансульфонилэтил)пиперазин-1-ил]метанон и
[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-ил](4-метилпиперазин-1-ил)метанон.
Термин «эффективное количество» означает количество, которое является эффективным для предотвращения, снижения интенсивности или облегчения симптомов заболевания или увеличения продолжительности жизни субъекта, нуждающегося в лечении.
Термин «галоген» означает фтор, хлор, бром или иод.
Термин «гетероатом» означает атом, выбранный из N, О и S.
Термин «IC50» означает концентрацию конкретного соединения, которая требуется для 50% ингибирования оцениваемой специфической активности. Кроме того, величину IC50 определяют, как описано ниже.
Термин «алкил» означает насыщенный алифатический углеводород с прямой или разветвленной цепью.
Термин «(низш.)алкил» означает C1-С6алкильные группы и включает метил, этил, пропил, изопропил, бутил, трет-бутил, 2-бутил, пентил, гексил и т.п. Обычно, (низш.)алкил предпочтительно означает С1-С4алкил и более предпочтительно C1-С3алкил.
Термин «циклоалкил» означает неароматический, частично или полностью насыщенный одновалентный циклический углеводородный радикал, содержащий от 3 до 8 атомов. Примеры циклоалкильных групп включают циклопропил, циклобутил, циклопентил и циклогексил.
Термин «алкокси» означает -O-алкил. Термин «(низш.)алкокси» означает -O-(низш.)алкил.
Определение «содержащий по крайней мере один гетероатом» в сочетании с определенными выше 5-6-членными кольцами означает, что указанные кольца содержат один или более, предпочтительно один, два или три гетероатома.
Термин «фармацевтически приемлемый сложный эфир» означает стандартное этерифицированное соединение формулы I, содержащее карбоксильную группу, причем указанные сложные эфиры сохраняют биологическую эффективность и свойства соединений формулы I, а также расщепляются in vivo (в организме) с образованием соответствующей активной карбоновой кислоты.
Информация, касающаяся сложных эфиров и применения сложных эфиров для доставки фармацевтических соединений, приведена в сборнике Design of Prodrugs, Bundgaard H eds., Elsevier (1985). См. также Ansel H. и др., Pharmaceutical Dosage Forms and Drug Delivery Systems, 6th eds., c.108-109 (1995), Krogsgaard-Larsen и др., Textbook of Drug Design and Development, 2nd eds., c.152-191 (1996).
Термин «фармацевтически приемлемые соли» означает стандартные кислотно-аддитивные соли или основно-аддитивные соли, которые сохраняют биологическую эффективность и свойства соединений по настоящему изобретению и образуются из пригодных нетоксичных органических или неорганических кислот или органических или неорганических оснований. Примеры кислотно-аддитивных солей включают соли неорганических кислот, таких как соляная кислота, бромистоводородная кислота, иодистоводородная кислота, серная кислота, сульфаминовая кислота, фосфорная кислота и азотная кислота, а также соли органических кислот, таких как пара-толуолсульфоновая, салициловая кислота, метансульфоновая кислота, щавелевая кислота, янтарная кислота, лимонная кислота, яблочная кислота, молочная кислота, фумаровая кислота и т.п. Примеры основно-аддитивных солей включают соли аммония, калия, натрия и четвертичных гидроксидов аммония, таких как, например, гидроксид тетраметиламмония. Химическое превращение фармацевтического соединения (т.е. лекарственного средства) в солевую форму для улучшения физической и химической стабильности, гигроскопичности, текучести и растворимости соединений проводят по методике, известной в фармацевтической химии. См., например, сборник Ansel H. и др., Pharmaceutical Dosage Forms and Drug Delivery Systems, 6th eds., c.196 и с.1456-1457 (1995).
Термин «фармацевтически приемлемый», такой как фармацевтически приемлемый носитель, эксципиент и т.д., означает фармакологически приемлемое и в значительной степени нетоксичное в отношении субъекта конкретное соединение, которое вводят указанному субъекту.
Термин «замещенный» означает, что заместители находятся в одном или более положений и, если не указано иное, что заместители при каждом атоме независимо выбирают из указанных вариантов.
Термин «терапевтически эффективное количество» означает количество по крайней мере одного указанного соединения, которое ингибирует в значительной степени пролиферацию и/или предотвращает дифференциацию опухолевых клеток человека, включая линии опухолевых клеток человека.
Соединения по настоящему изобретению, примеры которых описаны ниже, характеризуются значениями IC50 от приблизительно 0,020 мкМ до приблизительно 20 мкМ.
Соединения по настоящему изобретению можно использовать для лечения или контроля нарушений клеточной пролиферации, прежде всего онкологических нарушений. Указанные соединения и составы, содержащие указанные соединения, можно использовать для лечения или контроля солидных опухолей, таких как, например, опухоли молочной железы, ободочной кишки, легких и предстательной железы.
Терапевтически эффективное количество соединения по настоящему изобретению означает количество соединения, которое проявляет эффективное действие и предотвращает, облегчает или снижает интенсивность симптомов заболевания или продлевает продолжительность жизни субъекта, нуждающегося в лечении. Терапевтически эффективное количество определяется специалистами в данной области.
Терапевтически эффективное количество или дозировку соединения по настоящему изобретению варьируют в широких пределах и определяют известным способом. Указанная дозировка подбирается в соответствии с индивидуальными требованиями в каждом конкретном случае, включая специфическое вводимое соединение(я), способ введения, заболевание, подлежащее лечению, а также пациента, нуждающегося в лечении. В основном, при пероральном или парентеральном введении взрослому человеку с массой тела приблизительно 70 кг соответствующая суточная дозировка составляет от приблизительно 10 мг до приблизительно 10000 мг, предпочтительно от приблизительно 200 мг до приблизительно 1000 мг, хотя верхний предел можно превысить в зависимости от показания. Суточную дозу вводят в виде однократной дозы или раздельными дозами или, при парентеральном введении, дозу вводят непрерывным вливанием.
В настоящем изобретении предлагаются также фармацевтические композиции, содержащие по крайней мере одно соединение формулы I или его фармацевтически приемлемую соль или сложный эфир и фармацевтически приемлемый носитель или эксципиент.
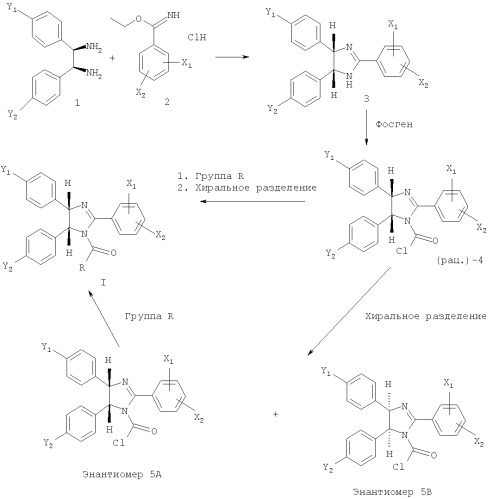
Соединения по настоящему изобретению получают согласно следующей схеме 1.
Схема I
На первой стадии синтеза проводят реакцию конденсации бензимидата 2 (полученного из соответствующих бензонитрилов с использованием газообразного хлористого водорода в этаноле, патент США №6617346 В1) с диамином 1, например мезо-1,2-бис-(4-хлорфенил)этан-1,2-диамином (полученным по методике, описанной в статье Jennerwein M. и др., Cancer Res. Clin. Oncol., т.114, с.347-58 (1988), Vogtle F., Goldschmitt E., Chem. Ber., т.109, с.1-40 (1976)), в растворителе, таком как этанол. После обработки имидазолина 3 фосгеном в присутствии основания, такого как триэтиламин, получают рацемический карбамоилхлорид 4. Энантиомеры (рац.)-4-карбамоилхлорида разделяют хиральной хроматографией. В качестве неподвижной фазы используют хиральный носитель R,R-Whelk-O1, поставляемый фирмой Regis Technologies. При конденсации требуемого энантиомера 5А с соответствующими аминогруппами (показанными как группа R) получают соединения формулы I.
При необходимости рацемические соединения формулы I получают из (рац.)-6-производных с использованием соответствующих аминогрупп (указанных как группа R). Энантиомеры I затем разделяют хиральной хроматографией. В качестве неподвижной фазы используют хиральный носитель фирмы Diacel ChiralPak OD или AD.
Абсолютную стереохимическую конфигурацию активного энантиомера I определяют по кристаллической структуре его комплекса с MDM2 человека (Vassilev и др., Science, т.303, с.844-848 (2004)).
Следующие примеры и ссылки приведены для более полного понимания сущности настоящего изобретения, полный объем которого определен в прилагаемой формуле изобретения.
Пример 1
цис-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидро-1Н-имидазол получали по методике, описанной в патенте США №6617346 В1.
Пример 2
дис-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидро-1H-имидазол получали по методике, описанной в патенте США №6617346 В1.
Пример 3
1-{4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанон
В раствор цис-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидро-1Н-имидазола (5,48 г, 12,03 ммоля, пример 2) в хлористом метилене (100 мл), охлажденном до 0°С, последовательно добавляли триэтиламин (11,8 мл, 84,21 ммоля) и фосген (30,53 мл, 60,15 ммоля, 21% раствор в толуоле). Реакционную смесь перемешивали при 0°С в течение 0,5 ч в атмосфере аргона, при этом результаты тонкослойной хроматографии (силикагель, 100% этилацетат) свидетельствовали о полном потреблении исходного соединения. Растворитель и избыток реагентов упаривали при пониженном давлении, а остаток сушили в вакууме в течение 1 ч. Остаток растворяли в хлористом метилене (100 мл), затем добавляли раствор 1-ацетилпиперазина (1,619 г, 12,63 ммоля) в хлористом метилене (10 мл). Реакционную смесь перемешивали при комнатной температуре в течение 1 ч (или до тех пор, пока результаты тонкослойной хроматографии свидетельствовали о полном потреблении исходного соединения). Затем добавляли насыщенный раствор бикарбоната натрия (10 мл), продукт экстрагировали хлористым метиленом (2 раза по 50 мл). Органические слои промывали солевым раствором (1 раз 20 мл), сушили над безводным сульфатом натрия и упаривали в вакууме. После очистки неочищенного остатка экспресс-хроматографией (система Biotage, KP-Sil™ 32-63 мкм, силикагель 60 Å, элюент: 100% этилацетат, затем 5% метанол в этилацетате) получали (рац.)-1-{4-[4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанон в виде пены оранжевого цвета (~7,2 г). Полученное соединение перекристаллизовывали из хлористого метилена и этилового эфира (6,721 г, твердое вещество белого цвета). Дополнительное количество (рац.)-1-{4-[4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанона (201 мг, желто-коричневого цвета) получали из маточного раствора после очистки экспресс-хроматографией (система Biotage, KP-Sil™ 32-63 мкм, силикагель 60 Å, элюент: 100% этилацетат и затем 5% метанол в этилацетате). Общий выход: 6,922 г (94%). МС-ВР (ES, m/z): рассч. для C32H35N4O4Cl2 609,2030 [(М+Н)+], найд. 609,2045.
Энантиомеры (рац.)-1-{4-[4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1 -карбонил]пиперазин-1-ил} этанона разделяли хиральной хроматографией (неподвижная фаза Daicel ChiralPak OD, элюент: этанол/гексан 1:1). Первая фракция, полученная при элюции, содержит требуемый энантиомер, 1-{4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанон. МС-НР (APCI): 609,12 [(М+Н)+].
Пример 4
4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-2-он получали из цис-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидро-1Н-имидазола (пример 2) и 2-пиперазинона аналогично тому, как описано в примере 3. МС-ВР (ES, m/z): рассч. для С30Н31N4O4Сl2 581,1717 [(М+Н)+], найд. 581,1709.
Пример 5
[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-ил1(4-пирролидин-1-илпиперидин-1-ил)метанон получали из цис-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидро-1Н-имидазола (пример 2) и 4-(1-пирролидинил)пиперидина аналогично тому, как описано в примере 3. МС-ВР (ES, m/z): рассч. для С35Н41N4O3Сl2 635,2550 [(М+Н)+], найд. 635,2558.
Пример 6
(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорид
В раствор цис-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазола (5 г, 10,98 ммоля, пример 2) в хлористом метилене (50 мл), охлажденном до 0°С, добавляли триэтиламин (3 мл, 21,96 ммоля) и фосген (8,7 мл, 16,47 ммоля, ~20% раствор в толуоле) соответственно. Реакционную смесь перемешивали при 0°С в течение 30 мин, затем избыток реагентов и растворитель упаривали при пониженном давлении. Остаток переносили в хлористый метилен (~100 мл) и раствор отфильтровывали через слой силикагеля (~50 г). Силикагель промывали 20% этилацетатом в гексане. Фильтрат упаривали в вакууме и остаток очищали экспресс-хроматографией (система Biotage, KP-Sil™ 32-63 мкм, силикагель 60 Å, элюент: 5%, 10%, 20% этилацетат в гексане), при этом получали (рац.)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метилфенил)-4,5-дигидроимидазол-1-карбонилхлорид в виде твердого вещества белого цвета (4,31 г, 76%).
Энантиомеры (рац.)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида разделяли хиральной хроматографией в системе Waters Delta Prep 4000 на колонке Modcol spring (50 мм × 70 см), заполненной сферическим силикагелем R,R-Whelk-O1 Kromasil (поставляемым фирмой Regis Technologies, элюент: 30% хлористый метилен в гексане), скорость потока: 85 мл/мин, нанесение образца: ~2 г. Первая фракция, полученная при элюции, содержит требуемый энантиомер, (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорид.
Пример 7
(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонилхлорид получали из 4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазола (пример 1) и фосгена аналогично тому, как описано в примере 6.
Пример 8
4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-2-он
В раствор (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (100 мг, 0,211 ммоля, пример 7) в хлористом метилене (3 мл), охлажденном до 0°С, добавляли триэтиламин (30 мкл, 0,211 ммоль) и 2-пиперазинон (23 мг, 0,232 ммоля) соответственно. Через 15 мин результаты тонкослойной хроматографии (силикагель, 20% этилацетат в гексане) свидетельствовали о полном потреблении исходного соединения. Реакционную смесь наносили на колонку для экспресс-хроматографии с силикагелем (12 г). После очистки колоночной экспресс-хроматографией (элюент: 5% метанол и 0,1% триэтиламин в этилацетате, система Intelliflash 280) получали 4-[(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-2-он в виде пены белого цвета (69 мг). МС-ВР (ES, m/z): рассч. для С30Н31N4O5Сl2 581,1717 [(М+Н)+], найд. 581,1717.
Пример 9
1-{4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}этанон получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 7) и 1-ацетилпиперазина аналогично тому, как писано в примере 8. МС-ВР (ES, m/z): рассч. для С30Н31N4О3Сl2 565,1768 [(М+Н)+], найд. 565,1772.
Пример 10
2-{4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}-1-морфолин-4-илэтанон получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 7) и гидрохлорида 1-морфолин-4-ил-2-пиперазин-1-илэтанона (фирмы Oakwood Chemicals) аналогично тому, как описано в примере 8. МС-ВР (ES, m/z): рассч. для C34H38N5O4Cl2 650,2296 [(М+Н)+], найд. 650,2299.
Пример 11
[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-ил][4-(2-метансульфонилэтил)пиперазин-1-ил]метанон
Метилвинилсульфон (1,8 мл, 20,1 ммоля) добавляли в раствор 1-(трет-бутилоксикарбонил)пиперазина (1,50 г, 8 ммоля) в метаноле (84 мл). Реакционную смесь перемешивали при комнатной температуре в течение 4 ч и упаривали досуха, получали твердое вещество белого цвета. После очистки твердого вещества колоночной экспресс-хроматографией (силикагель, элюент: 1-5% метанол в хлористом метилене) получали 1-трет-бутилоксикарбонил-4-(2-метансульфонилэтил)пиперазин в виде твердого вещества белого цвета (2,29 г, 95%).
В охлажденный раствор 1-трет-бутилоксикарбонил-4-(2-метансульфонилэтил)пиперазина (2,29 г, 7,8 ммоля) в 1,4-диоксане (42 мл) добавляли хлористоводородную кислоту (42 мл, 168 ммоля, 4М раствор в 1,4-диоксане). Смесь перемешивали при комнатной температуре в течение ночи, затем упаривали, при этом получали бисгидрохлорид 1-(2-метансульфонилэтил)пиперазина в виде твердого вещества белого цвета (2,05 г).
(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-карбонилхлорид (пример 7) вводили в реакцию с бисгидрохлоридом 1-(2-метансульфонилэтил)пиперазина в хлористом метилене аналогично тому, как описано в примере 8, при этом получали [(4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-этоксифенил)-4,5-дигидроимидазол-1-ил][4-(2-метансульфонилэтил)пиперазин-1-ил]метанон. МС-ВР (ES, m/z): рассч. для С32Н35Н4O4SСl2 629,1751 [(М+Н)+], найд. 629,1757.
Пример 12
[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-ил](4-метилпиперазин-1-ил)метанон получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 6) и 1-метилпиперазина аналогично тому, как описано в примере 8. МС-ВР (ES, m/z): рассч. для C31H35N4O4SCl2 629,1751 [(М+Н)+], найд. 629,1757.
Пример 13
[(45,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-ил][4-(2-метансульфонилэтил)пиперазин-1-ил]метанон получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 6) и 1-(2-метансульфонилэтил)пиперазина (пример 11) аналогично тому, как описано в примере 8. МС-НР: 673,3 [(М+Н)+].
Пример 14
2-{4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}-N,N-диметилацетамид получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 6) и N,N-диметил-2-пиперазин-1-илацетамида (фирмы Oakwood Chemicals) аналогично тому, как описано в примере 8. МС-НР: 652,3 [(М+Н)+].
Пример 15
2-{4-[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонил]пиперазин-1-ил}-1-морфолин-4-илэтанон получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 6) и гидрохлорида 1-морфолин-4-ил-2-пиперазин-1-илэтанона (фирмы Oakwood Chemicals) аналогично тому, как описано в примере 8. МС-НР: 694,3 [(М+Н)+].
Пример 16
[(4S,5R)-4,5-Бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-ил](4-этансульфонилпиперазин-1-ил)метанон получали из (4S,5R)-4,5-бис-(4-хлорфенил)-2-(2-изопропокси-4-метоксифенил)-4,5-дигидроимидазол-1-карбонилхлорида (пример 6) и 1-этансульфонилпиперазина (полученного из 1-трет-бутилоксикарбонилпиперазина и этансульфонилхлорида) аналогично тому, как описано в примере 8. МС-НР: 659,2 [(М+Н)+].
Пример 17
Определение активности in vitro
Способность соединений ингибировать взаимодействие между белками р53 и MDM2 оценивали методом ИФА (твердофазный иммуноферментный анализ), т.е. по связыванию рекомбинантного MDM2, содержащего GST, с пептидом, включающим участки связывания белка р53 с MDM2 (Böttger и др., J. Mol. Bio., т.269, с.744-756 (1997)). Указанный пептид иммобилизовали на поверхности 96-луночного планшета за счет связывания N-концевого биотина, который связывается с лунками, покрытыми стрептавидином. В каждую лунку добавляли MDM2 в присутствии мышиных моноклональных антител против MDM2 (SMP-14, Santa Cruz Biotech). После удаления несвязанного белка MDM2 добавляли конъюгат пероксидазы с вторичными антителами (мышиные антитела анти-IgG, Roche Molecular Biochemicals) и количество связанного с пептидом MDM2 определяли калориметрически после добавления субстрата пероксидазы (МТВ Microwell Peroxydase Substrate System, Kirkegaard & Perry Labs).
Анализируемые планшеты готовили нанесением на их поверхность стрептавидина (раствор в ФСБ, 5 мг/мл) в течение 2 ч с последующей промывкой ФСБ (фосфатно-солевой буферный раствор) и блокированием при 4°С в течение ночи блокирующим буфером (150 мкл), содержащим 2 мг/мл бычьего сывороточного альбумина (Sigma) и 0,05% раствор твин 20 (Sigma) в ФСБ. В каждую лунку добавляли биотинилированный пептид (1 мкМ) в 50 мкл блокирующего буфера и после инкубирования в течение 1 ч тщательно промывали. Анализируемые соединения разбавляли в отдельном 96-луночном планшете и добавляли в трех повторах в планшет для инкубации соединения, содержащий смесь белка MDM2 и антител против MDM2. Через 20 мин инкубации содержимое планшета переносили в анализируемый планшет и инкубировали в течение еще 1 ч. В анализируемый планшет добавляли вторичные мышиные антитела анти-IgG и промывали три раза 0,05% раствором твин 20 в ФСБ. Затем в каждую лунку добавляли субстрат пероксидазы и регистрировали величину поглощения на ридере для считывания планшетов (MR7000, Dynatech) при длине волны 450 нм. Ингибирующую активность анализируемых соединений выражали в виде % связывания MDM2 в лунках, обработанных соединением, по сравнению с лунками в отсутствие соединения и рассчитывали величину IC50.
Полученные данные свидетельствуют о том, что соединения по настоящему изобретению проявляют биологическую активность, причем значения IC50 находятся в диапазоне от приблизительно 0,020 мкМ до приблизительно 20 мкМ. Полученные результаты для некоторых соединений приведены ниже:
| Пример | IC50 (мкМ) |
| 4 | 0,604 |
| 5 | 0,071 |
1. Соединение формулы I и его фармацевтически приемлемые соли, где R означает насыщенное 6-членное кольцо, содержащее один или два гетероатома азота, и замещенное группой, выбранной из следующих групп: (низш.)алкил, -C(O)-R1, (низш.)алкил, замещенный группой -SO2-(низш.)алкил, (низш.)алкил, замещенный группой -C(O)-R1, -SO2-(низш.)алкил, или 5-членное насыщенное кольцо, содержащее один гетероатом азота,R1 выбирают из группы, включающей (низш.)алкил, -N((низш.)алкил)2, или R1 означает 6-членное насыщенное кольцо, содержащее два гетероатома, выбранных из N и О,X1 и Х2 независимо выбирают из группы, включающей водород, (низш.)алкокси,каждый Y1 и Y2 независимо выбирают из группы, включающей -Сl и -Вr, иабсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию, соответственно.
2. Соединение формулы I по п.1, гдеR означает насыщенное 6-членное кольцо, содержащее один или два гетероатома азота, и замещенное группой, выбранной из следующих групп: (низш.)алкил, -SО2СН3, а также 5-членное насыщенное кольцо, содержащее один гетероатом N,X1 и Х2 независимо выбирают из группы, включающей водород и (низш.)алкокси,каждый Y1 и Y2 независимо выбирают из группы, включающей -Сl и -Вr, иабсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию, соответственно.
3. Соединение по п.1, гдеR означает пиперазинил, замещенный группой, выбранной из следующих групп: (низш.)алкил, C(O)-R1, (низш.)алкил, замещенный группой -C(O)-R1, -SО2СН3, -СН2С(O)СН3, и гдеR1 выбирают из группы, включающей (низш.)алкил, -N-((низш.)алкил)2.
4. Соединение по п.3, где группа X1, расположенная в орто-положении, представляет собой (низш.)алкокси, а группа X2, расположенная в пара-положении, означает также (низш.)алкокси.
5. Соединение по п.4, где группу X1, расположенную в орто-положении, выбирают из следующих групп: этокси, изопропокси, а группу X2, расположенную в пара-положении, выбирают из метокси и этокси.
6. Соединение по п.5, где R означает пиперазинил, замещенный группой, выбранной из следующих групп: (низш.)алкил, C(O)-R1, (низш.)алкил, замещенный группой -C(O)-R1, -SO2CH3, -CH2C(O)CH3, гдеR1 выбирают из группы, включающей (низш.)алкил и -N-((низш.)алкил)2.
7. Соединение по п.1 формулы I-A и его фармацевтически приемлемые соли где R означает пиперазинил или пиперидинил, замещенный следующими группами: C1-С4алкил, -С(O)-(С1-С4алкил), пирролидин-1-ил,X1 означает -O-(С1-С4алкил),Х2 означает водород или -O-(С1-С4алкил), иабсолютная стереохимическая конфигурация в положении 4 и 5 имидазолинового кольца включает S и R конфигурацию, соответственно.
8. Соедине