Замещенные производные норборниламина, способ их получения и лекарственное средство
Иллюстрации
Показать всеИзобретение относится к новым замещенным производным норборниламина с экзоконфигурацией азота и эндоаннелированными пяти-шестичленными циклами формулы (I) и с экэо-конфигурацией азота и экзоаннелированными пяти-шестичленными циклами формулы (Ia), а также их фармацевтически приемлемым солям или трифторацетатам, которые могут быть использованы для получения лекарственных средств, пригодных для лечения или профилактики нарушений дыхательного импульса, в частности обусловленных сном нарушений дыхания, таких как временная остановка дыхания во время сна, храпа, для лечения или профилактики острых и хронических почечных заболеваний, в частности острой почечной недостаточности и хронической почечной недостаточности, нарушений функции кишечника, желчного пузыря, ишемических состояний периферической и центральной нервной системы и острых приступов и др. Соединения изобретения являются ингибиторами натрийпротонного обмена, влияют на сывороточный липопротеин и поэтому могут быть использованы для профилактики и для регрессии атеросклеротических изменений.
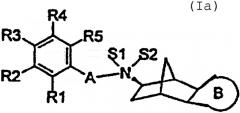
В соединениях формулы (I) или (Ia) А обозначает (С1-С4)-алкилен; S1 обозначает отсутствует или обозначает (С1-С4)-алкил; S2 обозначает (С1-С4)-алкил или Н; причем, если S1 и S2 обозначают алкил, X- в образующейся группировке [-N+(S1S2)-X-] соответствует фармакологически приемлемому аниону или трифторацетату; В обозначает насыщенный или ненасыщенный углеродный пяти- или шестичленный цикл, и R1, R2, R3, R4 и R5 имеют значения, указанные в описании. Изобретение также относится к способу получения соединений и к лекарственному средству. 3 н. и 18 з.п. ф-лы, 4 табл.
Реферат
Изобретение относится к замещенным производным норборниламина с экзоконфигурацией азота и эндоаннелированными пяти-, шести- или семичленными циклами формулы I и с экзоконфигурацией азота и экзоаннелированными пяти-, шести- или семичленными циклами формулы Ia,
где обозначают
А - (С1-С4) - алкилен;
S1 - свободную пару электронов или (С1-С4)-алкил;
S2 - (С1-С4)-алкил или Н;
причем, если S1 и S2 обозначают алкил, Х- в образующейся группировке [-N+(S1S2)-X-] соответствует фармакологически приемлемому аниону или трифторацетату;
В - насыщенное или ненасыщенное углеродное пяти-, шести- или семичленное кольцо, которое независимо друг от друга может быть одно- или многократно оксо-, гидрокси-, (C1-C4)-алкоксигруппой и (C1-C4)-алкилом;
и R1, R2, R3, R4 и R5 - независимо друг от друга Н, ОН, F, Cl, Br, I, CN, NO2, амидиногруппу, -CO2R(11), -CONR(11)R(12), -SOrR(11), -SOsNR (11) R (12), (C1-C4) -алкил, (C1-C4) -алкоксигруппу, (C1-C4) -алкокси(C1-C4) -алкил, (C1-C4) -алкокси(C1-C4) -алкилоксигруппу, гидрокси-(C1-C4)-алкил, (С3-С7)-циклоалкокси или фенилоксигруппу,
причем фенил не замещен или замещен вплоть до трех заместителями, независимо друг от друга выбранными из группы, состоящей из F, Cl, Br и метоксигруппы;
амино-, (C1-C4) -алкиламино-, ди(C1-C4) -алкиламиногруппу, амино(C1-C4) -алкил, ди(C1-C4) -алкиламино(C1-C4) -алкил, (C1-C4)-алкиламино-(C1-C4)-алкил, причем атомы водорода в алкильных остатках полностью или частично могут быть замещены фтором;
R11 и R12- независимо друг от друга Н или (C1-C4)-алкил,
причем атомы водорода в алкильных остатках полностью или частично могут быть замещены фтором;
r - 0, 1 или 2;
s - 1 или 2;
или каждые из R1 и R2, R2 и R3, R3 и R4 или R4 и R5 - вместе группу -O-(СН2)n-O-;
n - 1 или 2;
и каждый из остальных остатков R1, R2, R3, R4 или R5 независимо друг от друга Н, ОН, F, Cl, Br, I, CN, NO2, амидиногруппу, -CO2R(11), -CONR(11)R(12); -SOrR(11), -SOsNR(11)R(12), (С1-С4)-алкил, (C1-C4)-алкоксигруппу, (C1-C4)-алкокси(C1-C4)-алкил, (С3-С7) -циклоалкоксигруппу, гидрокси-(C1-C4) -алкил, амино-, (C1-C4) -алкиламино-, ди(C1-C4) -алкил-аминогруппу, амино(C1-C4) -алкил, ди(C1-C4) -алкиламино-(C1-C4)-алкил, (C1-C4)-алкиламино-(C1-C4)-алкил,
причем атомы водорода в алкильных остатках полностью или частично могут быть замещены фтором;
R11 и R12 - независимо друг от друга Н или (C1-C4)-алкил,
причем атомы водорода в алкильных остатках полностью или частично могут быть замещены фтором;
r - 0, 1 или 2;
s - 1 или 2;
при этом бензил-(октагидро-4,7-метано-инден-5-ил)-амин исключается, а также их фармацевтически приемлемые соли или трифторацетаты.
Предпочтительны соединения с экзоконфигурацией азота и эндоаннелированным пяти- или шестичленным кольцом формулы I и с экзоконфигурацией азота и экзоаннелированным пяти- или шестичленным кольцом формулы Ia, в которых обозначают
А - (С1-С2)-алкилен;
S1 - свободную пару электронов или метил;
S2 - Н;
В - насыщенное или ненасыщенное углеродное пяти- или шестичленное кольцо;
R1, R2, R3, R4 и R5 - независимо друг от друга Н, аминогруппу, гидроксиметил, ОН, метоксигруппу, F, Cl, Br или иод;
или R2 и R3 - вместе -O-СН2-O-;
и остающиеся остатки R1, R4 и R5 независимо друг от друга Н, ОН, F, Cl, Br, I, CN, NO2, (С1-С2)-алкокси-, амино-, (С1-С2)-алкиламино- или ди- (C1-C2)-алкиламиногруппу,
причем атомы водорода в алкильных остатках полностью или частично могут быть замещены фтором;
при этом исключается бензил-(октагидро-4,7-метано-инден-5-ил)-амин, а также их фармацевтически приемлемые соли и трифторацетаты.
Особенно предпочтительны соединения с экзоконфигурацией азота и эндоаннелированным пяти- или шестичленным кольцом формулы I и с экзоконфигурацией азота и экзоаннелированным пяти- или шестичленным кольцом формулы Ia, в которых обозначают:
А - (С1-С2)-алкилен;
S1 - свободную пару электронов;
S2 - Н;
В - насыщенное или ненасыщенное углеродное пяти- или шестичленное кольцо;
R1, R3 и R5 - водород;
и R2 и R4 - независимо друг от друга Н, метоксигруппу, F или Cl;
или R2 и R3 - вместе -О-СН2-О-;
и R1, R4 и R5 - водород;
при этом исключается бензил-(октагидро-4,7-метано-инден-5-ил)-амин, а также их фармацевтически приемлемые соли или трифторацетаты.
Наиболее предпочтительны следующие соединения с экзоконфигурацией азота и эндоаннелированным пяти- или шестичленным кольцом формулы I и с экзоконфигурацией азота и экзоаннелированным пятичленным кольцом формулы Ia:
экзо/эндо-(3-хлорбензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3-фторбензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-бензо[1,3]диоксол-5-илметил-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(рац)-(3-метоксибензил)-(октагидро-4,7-метано- инден-5-ил)амин,
экзо/эндо-(+)-(3-метоксибензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(-)-(3-метоксибензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-[1-(3-метоксифенил)-этил]-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3-фторбензил)-(3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3-фторбензил)-(3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)-(3-метоксибензил)амин,
экзо/эндо-(3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-ил)-(3-метоксибензил)амин,
экзо/эндо-(декагидро-1,4-метано-нафталин-2-ил)-(3-метоксибензил)амин,
экзо/ендо-(3,5-дифторбензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3-фторбензил)-(октагидро-4,7-метано-инден-5-ил)амин
и
экзо/эндо-(3-метоксибензил)-(октагидро-4,7-метано-инден-5-ил)амин,
а также их фармацевтически приемлемые соли или трифторацетаты.
Особенно предпочтительны следующие соединения с экзоконфигурацией азота и эндоаннелированными пяти- или шестичленными циклами формулы I:
экзо/эндо-(3-хлорбензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3-фторбензил)-(октагидро-4,7-метано-инден-5-ил)амин
экзо/эндо-(3-фторбензил)-(3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)амин,
экзо/эндо-(3-фторбензил)-(3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-ил)амин,
экзо/эндо-бензо[1,3]диоксол-5-илметил-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(рац)-(3-метоксибензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(+)-(3-метоксибензил)-(октагидро-4,7-метано-инден-5-ил)амин,
экзо/эндо-(декагидро-1,4-метано-нафталин-2-ил)-(3-метоксибензил)амин,
экзо/эндо-(-)-(3-метоксибензил)-(октагидро-4,7-метано-инден-5-ил)амин и
экзо/эндо-(3,5-дифторбензил)-(октагидро-4,7-метано-инден-5-ил)-амин,
а также их фармацевтически приемлемые соли или трифторацетаты.
В качестве аддитивных солей кислот принимают во внимание все фармакологически приемлемые соли, например галогениды, в частности хлориды, лактаты, сульфаты, цитраты, тартраты, ацетаты, фосфаты, метилсульфонаты, пара-толуолсульфонаты, адипинаты, фумараты, глюконаты, глутаматы, глицерофосфаты, малеаты и памоаты. Указанная группа соответствует также фармакологически приемлемым анионам. Но речь идет также о трифторацетатах.
Если соединение формулы I или Ia содержит один или более центров асимметрии, то они могут иметь как S-, так и R-конфигурацию. Соединения могут быть представлены в виде оптических изомеров, диастереомеров, рацематов или их смесей. Конечно, аминозаместитель должен находиться в экзоположении и кольцо быть эндо- или экэоаннелированным.
Названные алкильные или алкиленовые остатки могут быть как линейными, так и разветвленными.
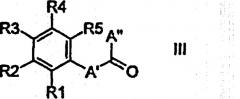
Дополнительно изобретение относится к способу получения соединений формулы I или Ia, отличающемуся тем, что а) соединение формулы II или IIa
подвергают взаимодействию с соединением формулы III в присутствии подходящего восстановителя и, возможно, также кислоты Льюиса непосредственно с образованием соединений формулы I или Ia,
где S1, S2, В, R1, R2, R3, R4 и R5 имеют приведенные выше значения, в то время как независимо друг от друга А' соответствует связи или (С1-С3)-алкилу и А'' соответствует Н или (С1-С3)-алкилу и А' и А'' вместе с атомом углерода карбонильной группы содержат столько атомов углерода, как указано выше для А;
или
b) образованный из соединений формул II или IIa и III промежуточное соединение формулы IV или IVa,
где если S1 обозначает (С1-С4)-алкил, образуется ониевый азот, которому соответствует противоион, такой как, например, хлорид или тозилат,
выделяют и затем подходящим восстановителем переводят в соединения формулы I или Ia,
или
с) соединение формулы II или IIa превращают с алкилирующим агентом формулы V,
где U обозначает нуклеофильно замещаемую группу, такую как хлор, бром и иод, а также мезилат, тозилат, трифлат или другую хорошо удаляемую группу, а другие остатки определены, как описано выше, но здесь атому углерода карбонильной группы соответствует атом углерода, связанный с U,
предпочтительно в присутствии ненуклеофильного основания, такого как диизопропилэтиламин,
или
а) амиды карбоновых кислот формулы VI или VIa
где А обозначает связь или (С1-С3)-алкил и другие
остатки определены, как описано выше, восстанавливают до соответствующих аминов;
или
e) соединения формулы I или Ia, в которых S1 обозначает свободную пару электронов и S2 обозначает водород, одно- или диалкилируют алкилирующим средством формулы VII,
где S* обозначает (С1-С4)-алкил и U имеет описанное выше значение, так что в результате этого взаимодействия образуется третичный амин или четвертичная соль аммония;
или
f) дициклопентадиенилплатиновый комплекс формулы VIII
подвергают взаимодействию с аминами типа формулы IX,
где S1, S2, R1, R2, R3, R4 и R5 имеют вышеприведенные значения, в то время как независимо друг от друга А' обозначает связь или (С1-С3)-алкил и А'' обозначает Н или (С1-С3)-алкил и А' и А'' вместе с атомом углерода, с которым связан атом азота, содержат столько атомов углерода, как описано выше для А,
и затем образовавшееся промежуточное соединение восстанавливают до получения соединения формулы I (J.K. Stille, D.B. Fox JACS 1970 (92), 1974),
и в случае необходимости переводят в фармацевтически приемлемую соль или трифторацетат.
В описании патента US 4024274 (Ное 74/F018) описан норборниламин подобной структуры, но с неизвестной пространственной структурой, с хорошей диуретической и салуретической активностью.
При анализе множества описанных в патенте примеров следует выделить некоторые соединения указанного типа в качестве сильных ингибиторов натрий-водородного обмена, подтип 3 (NHE3). Соединения были на основании этого испытаны на их салидиуретическое действие и неожиданно не было подтвержено никакого салидиуретического действия, так что взаимосвязь между NНЕ3-активностью и салидиурезом не могла быть показана.
Поскольку пространственная структура трицикла была неизвестна, существовал выбор между четырьмя возможными парами энантиомеров, то есть всего восемью пространственно различными структурами. Для указанных пар энантиомеров показано, что только две пары проявляют сильное NHE3-ингибирующее действие, тогда как две другие пары энантиомеров едва проявляют NНЕ3-блокирующие свойства. Поиск наиболее активных структур путем рентгеноструктурного анализа показал, что в случае наиболее сильных NНЕ3-активных пар энантиомеров речь идет о соединениях с определенной экзоконфигурацией для азота, а также с определенным эндоаннелированным пятичленным кольцом. Несколько менее активная пара энантиомеров обладает определенной экзоконфигурацией азота, а также определенно экзоаннелированным пятичленным кольцом. Обе оставшиеся пары энантиомеров с определенными эндо/экзо- или эндо/эндоконфигурациями едва проявляют NНЕ3-ингибируюшее действие.
Далее неожиданно было показано, что определенные разделенные энантиомеры - соединения из примера, которые имели определенную экзоконфигурацию атома азота, а также определенно эндоаннелированное пятичленное кольцо, оба были одинаково активными по отношению к NHE3. Из-за их зеркального пространственного расположения ожидали четкого различия активностей.
В противоположность известным ингибиторам натрий-водородного обмена, подтипа 3 по патенту EP-OS 825178 {НОЕ 96/F226), которые представлены относительно полярными структурами и соответствуют ацилгуанидинному типу (J.-R. Schwark и др. Eur. J. Physiol (1998) 436:797), в случае предложенных соединений речь идет о неожиданно липофильных веществах, которые не относятся к ацилгунидиновому типу и представляют собой совершенно новые структуры для ингибирования NHE3. Вслед за только что названными ацилгуанидинами и затрудненно действующим скваламином (M.Donowitz и др. Am. J. Physiol. 276 (Cell Physiol. 45): C136-C144) активность наблюдалась через один час, речь идет о третьем классе веществ NНЕ3-ингибиторов, которые были известны ранее. В противоположность вышеназванным NHE3-ингибиторам они проявляют повышенную проницаемость через мембраны и незамедлительное наступление действия.
NHE3 был обнаружен в различных частях тела, предпочтительно в желчном пузыре, кишечнике и почках (Larry Fliegel и др., Biochem. Cell. Biol. 76: 735-741, 1998), а также в головном мозге (Е. Ма и др. Neuroscience 79:591-603).
Предлагаемые согласно; изобретению соединения формулы I или Ia пригодны для применения в качестве антигипертензивных средств для лечения первичной и вторичной гипертонии.
Кроме того, соединения индивидуально или в сочетании с NHE-ингибиторами других подтипов могут защищать от острой или хронической кислородной недостаточности органа путем уменьшения или затруднения индуцированных ишемией нарушений. Они применимы таким образом в качестве лекарственных средств, например, при оперативных вмешательствах (например, при трансплантации органов, почки и печени, причем эти соединения могут быть использованы для зашиты органа у донора перед или во время отделения, для защиты отделенного органа, например, при обработке или хранении в физиологической жидкости, а также при его пересадке в организм реципиента) или острой и хронической почечной недостаточности. С особенной пользой удается снизить индуцированные ишемией нарушения в кишечнике.
В соответствии с их защитным действием против индуцированных ишемией нарушений соединения потенциально применимы также в качестве лекарственных средств для лечения ишемии нервной системы, в частности ЦНС, причем они, например, применимы для лечения острых приступов или отека мозга. Кроме того, предложенные соединения формулы I или Ia равным образом применимы для лечения форм шоков, таких как, например, аллергический, кардиогенный, гиповолемический и бактериальный шоки.
Далее соединения индуцируют улучшение дыхательного импульса и поэтому привлекаются к лечению затруднения дыхания при следующих клинических состояниях и заболеваниях: затрудненный центральный дыхательный импульс (например, центральный синдром временной остановки дыхания во время сна, внезапная детская смерть, постоперационная гипоксия), обусловленные мускулатурой нарушения дыхания, нарушения дыхания после длительной искусственной вентиляции легких, нарушения дыхания при адаптации к высокогорью, обструктивные и смешанные формы временной остановки дыхания во время сна, острые и хронические заболевания легких с гипоксией и гиперкапнией.
Дополнительно соединения повышают мускульный тонус верхних дыхательных путей, так что подавляется храп.
Комбинация NHE-ингибитора с ингибитором карбоангидразы (например, ацетазоламидом), причем последний приводит к метаболическому ацидозу и таким образом повышает устойчивость дыхания, оказывается полезной благодаря усиленному действию и уменьшенному введению активного вещества.
Показано, что соединения согласно изобретению обладают мягким послабляющим действием и поэтому с пользой могут быть использованы в качестве слабительных средств или при угрожающих запорах, причем уменьшение застойных явлений в кишечнике особенно полезно при ишемических нарушениях.
Дополнительно существует возможность ингибирования образования желчных камней.
Кроме того, предлагаемые согласно изобретению соединения формулы I или Ia могут оказывать ингибирующее действие на пролиферацию клеток, например пролиферацию фибробластных клеток и пролиферацию клеток гладких мускулов сосудов. Поэтому в случае соединений формулы I или Ia речь идет о ценных терапевтических средствах при заболеваниях, при которых пролиферация клеток является первичной или вторичной причиной, и поэтому могут быть использованы в качестве антиатеросклеротических средств, средств против поздних диабетических осложнений, раковых заболеваний, фибротических заболеваний, таких как фиброз легких, фиброз печени или фиброз почки, эндотелиальной дисфункции, гипертрофии и гиперплазии органов, в частности при гиперплазии простаты или гипертрофии простаты.
Предлагаемые согласно изобретению соединения являются активными ингибиторами клеточного натрий-протонного обмена, который при многочисленных заболеваниях (эссенциальной гипертонии, атеросклерозе, диабете и т.д.) повышен в таких клетках, которые легко доступны для измерений, как, например, в эритроцитах, тромбоцитах или лейкоцитах. Соединения согласно изобретению поэтому пригодны в качестве простых научных средств, например при их применении в качестве диагностических средств для определения и распознавания определенных форм гипертонии, а также атеросклероза, диабета, пролиферативных заболеваний и т.д. Сверх того, соединения формулы I или Ia применимы для профилактической терапии для предотвращения генеза кровяного давления, например эссенциальной гипертонии.
Кроме того, обнаружено, что NHE-ингибиторы оказывают благоприятное влияние на сывороточные липопротеины. Вообще признано, что для возникновения артериосклеротических изменений сосудов, в частности коронарных сердечных заболеваний, слишком высокое содержание жира в крови, так называемая гиперлипопротеинемия, представляет собой существенный фактор риска. Поэтому для профилактики и регрессии атеросклеротических изменений снижение повышенного сывороточного липопротеина имеет исключительное значение. Предлагаемые соединения поэтому могут привлекаться для профилактики и для регрессии атеросклеротических изменений, в то время как они исключают причинный фактор риска. Благодаря такой защите сосудов в отношении синдрома эндотелиальной дисфункции соединения формулы I или Ia являются ценными лекарственными средствами для предупреждения и лечения спазм коронарных сосудов, атерогенеза и атеросклероза, левовентрикулярной гипертонии и дилатационной кардиомиопатии, и тромботических заболеваний.
Названные соединения поэтому находят применение для получения лекарственного средства для предупреждения и лечения временной остановки дыхания во время сна и мускульно обусловленных нарушений дыхания; для получения лекарственного средства для предупреждения и лечения храпа; для получения лекарственного средства для снижения кровяного давления; для получения лекарственного средства с послабляющим действием для предупреждения и лечения кишечных запоров; для получения лекарственного средства для предупреждения и лечения заболеваний, вызываемых ишемией и реперфузией центральных и периферических органов, таких как острая почечная недостаточность, острый приступ, состояние эндогенного шока, кишечные заболевания и т.д.; для получения лекарственного средства для лечения гиперхолестеринемии; для получения лекарственного средства для предупреждения атерогенеза и атеросклероза; для получения лекарственного средства для предупреждения и лечения заболеваний, вызванных повышенным уровнем холестарина; для получения лекарственного средства для предупреждения и лечения заболеваний, вызванных эндотелиальной дисфункцией; для получения лекарственного средства для лечения поражения эктопаразитами; для получения лекарственного средства для лечения названных болезней в сочетании с понижающими кровяное давление веществами, предпочтительно с ингибиторами ангиотензинпревращающего фермента (АСЕ) и антагонистами рецепторов ангиотензина. Комбинация NHE-ингибитора формулы I или Ia с понижающим уровень жира в крови активным веществом, предпочтительно с ингибитором HMG-CoA-редуктаэы (например, ловастатином или правастатином), причем последний приводит к гиполипидемическому действию и таким образом повышает гиполипидемические свойства NHE-ингибитора формулы I или Ia, представляет собой благоприятную комбинацию с усиленным действием и уменьшенным введением активного вещества.
В качестве лекарственного средства нового типа для понижения повышенного уровня кровяного давления предлагается введение ингибиторов натрий-протонного обмена формулы I или Ia, а также комбинации ингибиторов натрий-протонного обмена с понижающими кровяное давление и/или гиполипидемически действующими лекарственными средствами.
Лекарственное средство, которое содержит соединение I или Ia, можно при этом вводить перорально, парентерально, внутривенно, ректально или путем ингаляций, причем предпочтительное введение зависит от соответствующей картины заболевания. Соединения I или Ia при этом могут применяться индивидуально или вместе с галеновыми вспомогательными веществами как в ветеринарии, так и в медицине.
Какие вспомогательные вещества применимы для желательной готовой препаративной формы лекарственного средства известно специалисту на основании его специальных знаний. Наряду с растворителями, гелеобразователями, основами суппозиториев, вспомогательными средствами для таблетирования и другими носителями активного вещества могут быть использованы, например, антиоксиданты, диспергаторы, эмульгаторы, вспениватели, вкусовые добавки, консерванты, солюбилизаторы или красители.
Для пероральной формы применения активные соединения смешивают с подходящими добавками, такими как носители, стабилизаторы или инертные разбавители, и переводят обычными способами в подходящие формы применения, такие как таблетки, драже, капсулы, водные, спиртовые или масляные растворы. В качестве инертного носителя могут быть использованы, например, гуммиарабик, магнезия, карбонат магния, фосфат калия, молочный сахар, глюкоза или крахмал, в частности кукурузный крахмал. При этом препаративная форма может быть получена как в виде сухих, так и в виде влажных гранулятов. В качестве масляного носителя или в качестве растворителя могут быть использованы, например, растительные или животные масла, такие как подсолнечное мало или рыбий жир.
Для подкожного или внутривенного применения активные соединения, при желании, с обычными веществами, такими как солюбилизаторы, эмульгаторы или другие вспомогательные вещества, вносят в раствор, суспензию или эмульсию. В качестве растворителя речь идет, например, о воде, физиологическом растворе поваренной соли или спирте, например этаноле, пропаноле, глицерине, кроме того, растворах сахаров, таких как растворы глюкозы или маннита, или также смеси различных названных растворителей.
В качестве фармацевтической готовой формы для применения в виде аэрозолей или спреев пригодны, например, растворы, суспензии или эмульсии активного соединения формулы I или Ia в фармацевтически приемлемом растворителе, в особенности в таком, как этанол или вода, или в смеси таких растворителей.
Готовая препаративная форма может содержать также еще другие фармацевтические вспомогательные вещества, такие как поверхностно-активные вещества, эмульгаторы и стабилизаторы, и газ-носитель. Такая готовая препаративная форма содержит активное вещество обычно в концентрации примерно от 0,1 до 10, в частности примерно от 0,3 до 3 мас.%.
Дозировка вводимого активного вещества формулы I или Ia и частота введения зависят от силы действия и продолжительности действия используемых соединений; кроме того, от вида и тяжести излечиваемого заболевания, также и от пола, возраста, веса и индивидуальных особенностей излечиваемого млекопитающего.
В среднем дневная доза соединения формулы I или Ia при весе пациента примерно 75 кг составляет по меньшей мере 0,001 мг/кг, предпочтительно 1-10 мг/кг, самое большее 100 мг/кг веса тела. При острых приступах болезни могут также быть необходимы еще большие и прежде всего более частые дозировки, например до 4 отдельных доз в день. В частности, при внутривенном введении, например, в случае инфарктного пацента в отделении интенсивной терапии может оказаться необходимым до 200 мг в день.
Экспериментальная часть:
Использованные сокращения:
СН2Cl2 - дихлорметан
CI - химическая ионизация
DIP - диизопропиловый эфир
ЭА - этилацетат
ES - электрораспыление
НОАс - уксусная кислота
Н2O - вода
H2O2 - пероксид водорода
т.кип. - температура кипения
МеОН - метанол
MgSO4 - сульфат магния
т.пл. - температура плавления
MS - масс-спектр
МТВ - метил-трет-бутиловый эфир
NaBH4 - боргидрид натрия
NaHCO3 - гидрокарбонат натрия
NaOH - гидроксид натрия
RT - комнатная темпаратура
ТГФ - тетрагидрофуран
TFA - трифторуксусная кислота
HCl - соляная кислота
Описание синтеза некоторых аминов
амин 1)
Синтез экзо/эндо-октагидро-4,7-метано-инден-5-иламина
a1) N,N'-диоксид бис-(6-хлор-3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)-диазена и изомеры
В смесь 167 г дициклопентадиена, 160 мл ледяной уксусной кислоты и 160 мл этанола прибавляли 167 г изоамилнитрита и затем по каплям при перемешивании при -10°C 420 мл 15%-ного раствора хлористого водорода в этаноле. Перемешивали следующие 3 часа при комнатной температуре. После прибавления 500 мл диизопропилового эфира перемешивали еще 10 минут и отфильтровывали кристаллы. Почти бесцветные кристаллы, т.пл. 177-178°С.
b1) октагидро-4,7-метано-инден-5-иламин
Суспензию из 10 г N,N'-диоксида бис-(6-хлор-3а,4,5,6,7, 7а-гексагидро-1Н-4,7-метано-инден-5-ил)-диазена, 60 мл метанола и никеля Ренея гидрировали 10 часов при 100°С под давлением Н2 100 ат. Катализатор отфильтровывали, растворитель упаривали на роторном испарителе под уменьшенным давлением, смешивали полукристаллический остаток с водой и сильно подщелачивали путем прибавления 10 н NaOH. После от 3- до 4-кратного экстрагирования метил-трет-бутиловым эфиром и высушивания органической фазы над сульфатом натрия растворитель отгоняли и масло перегоняли в вакууме. Т.кип.5мм 86-91°С. или
а2) 3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-иламин и 3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-иламин
20 г экзо-5-изотиоцианато-5,6-дигидроэндодициклопентадиена (Maybridge international) растворияли в 60 мл муравьиной кислоты и 27 часов кипятили с обратным холодильником. Летучие компоненты удаляли в вакууме, добавляли 50 мл 20%-ного водного раствора NaOH и трижды экстрагировали по 100 мл CH2Cl2. Сушили над MgSO4 и растворитель удаляли в вакууме. Получили 13,4 г бледно-желтого масла.
Rf (CH2Cl2/MeOH/HOAc/H2O 32:8:1:1)=0,57; MS(ES+):150 (М+Н)+
b2) трет-бутиловый эфир (3а,4,5,6,7,7а-гексагидро-1H-4,7-метано-инден-5-ил) карбаминовой кислоты и трет-бутиловый эфир (3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)карбаминовой кислоты
12,8 г смеси 3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-иламина и 3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-иламина растворяли в 200 мл ТГФ и при RT смешивали с раствором 18,7 г ди-трет-бутилдикарбоната в 200 мл ТГФ. Затем прибавляли по каплям 12 мл триэтиламина и перемешивали 2 часа при RT. Летучие компоненты удаляли в вакууме и остаток хроматографировали на силикагеле с DIP. Получили 15 г бесцветного масла, которое кристаллизовали из н-гептана; т.пл. 94°С.
Rf(DIP) = 0,68 MS (CI+):250 (M+H)+
с2) трет-бутиловый эфир (октагидро-4,7-метано-инден-5-ил)-
карбаминовой кислоты
500 мг смеси трет-бутилового эфира (3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)карбаминовой кислоты и трет-бутилового эфира (3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-ил)-карбаминовой кислоты растворяли в 20 мл метанола и 2 мл уксусной кислоты и гидрировали с помощью 200 мг 10%-ного Pd/C (50% воды) под атмосферой водорода (1 бар) в течение 6 часов. Катализатор отфильтровывали и летучие компоненты удаляли в вакууме. Получили 470 мг смолообразного аморфного твердого вещества.
Rf(DIP)=0,70 MS (CI+):252 (М+Н)+
d2) трифторацетат октагидро-4,7-метано-инден-5-иламина
460 мг трет-бутилового эфира (октагидро-4,7-метано-инден-5-ил)-карбаминовой кислоты растворяли в 5 мл трифторуксусной кислоты и 24 часа перемешивали при RT. Затем летучие компоненты удаляли в вакууме и получили 390 мг бледно-желтого пенообразного продукта.
Rf(ЭА/НЕР/МеОН/СН2Cl2/насыщенный водный раствор NH3 10:5:5:5:1)=0,30
MS (CI+):152 (M+H)+
или
а3) октагидро-4,7-метано-инден-5-иламин
3,3 г смеси 3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-иламина и 3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-иламина (пример амина 1, а2) растворяли в 30 мл метанола и восстанавливали под атмосферой водорода в присутствии 0,5 г Pd/C (10%). Через 4 часа катализатор отфильтровывали и промывали метанолом. Фильтрат упаривали в вакууме и получали 3 г желаемого продукта в виде масла. MS(ES+):152 (М+Н)+
Амин 2) Синтез эндо/экэо-октагидро-4,7-метано-инден-5-иламина
Предварительно насыщенный при 10° С МНз раствор 15 г трицикло[5,2,1,02,6]декан-8-она в 60 мл метанола после добавления никеля Ренея гидрировали в автоклаве при 90°С и давлении водорода 100 бар свыше 10 часов. После фильтрования катализатора и перегонки растворителя при уменьшенном давлении с помощью 10 н NaOH сильно подщелачивали и экстрагировали 2-3 раза этилацетатом или диизопропиловым эфиром. Объединенные органические фазы сушили и фракционировали в вакууме. Т. кип.6-7мм 86-88°С.
Амин 3)
Синтез эндо/эндооктагидро-4,7-метано-инден-5-иламина
a) оксим 1,3а,4,6,7,7а-гексагидро-4,7-метано-инден-5-она
10 г N,N'-диоксида бис-(6-хлор-3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)диазена из амина 1, а1) суспендировали в 75 мл изоамилового спирта и при перемешивании медленно нагревали до кипения. После полного растворения охлаждали на ледяной бане до комнатной температуры и прибавляли 25 мл осушенного этанола, 12,5 мл ледяной уксусной кислоты и 6 г цинковой пыли. Кипятили в течение часа, охлаждали, цинк отфильтровывали и этанол отгоняли. Остаток перемешивали в 300 мл простого эфира и выдерживали в течение ночи. Затем эфир декантировали от осадка и промывали трижды раствором карбоната натрия и дважды водой. После высушивания над сульфатом магния фильтровали и затем фильтрат упаривали. Последующей перегонкой в вакууме получено 3,3 г масла, которое сразу использовали дальше.
b) октагидро-4,7-метано-инден-5-иламин
2,2 г оксима 1,3а,4,6,7,7а-гексагидро-4,7-метано-инден-5-она растворяли в 50 мл метанола и прибавляли около 10% никеля Ренея, растворенного в 50% воды. Через 20 часов гидрировали при 100 барах и 100°С, катализатор отфильтровывали и растворитель отгоняли. Остаток извлекали простым эфиром и 6 н гидроокисью натрия, фазы разделяли, водную фазу трижды экстрагировали эфиром, объединенные органические фазы сушили сульфатом магния, фильтровали и фильтрат упаривали. Оставалось 1,8 г бесцветного масла, которое очищали перегонкой с шариковым дефлегматором. Получили 0,96 г желаемого амина в виде масла.
MS (CI+):152,2 (М+Н)+
Амин 4)
Синтез экзо/экзооктагидро-4,7-метано-инден-5-иламина
a) октагидро-4,7-метано-инден-5-ол
25 г трицикло[5.2.1.0(2,6)]декан-8-она (Aldrich) растворяли в 100 мл метанола и при комнатной температуре при легком охлаждении и перемешивании порциями в течение 2 ч прибавляли 6,3 г твердого боргидрида натрия. Затем перемешивали еще 2 ч и выдерживали в течение ночи. При охлаждении затем прибавляли по каплям около 40 мл 2 н HCl и далее 20 мл воды. Смесь упаривали, остаток смешивали с этилацетатом и этилацетатную фазу промывали один раз водой и один раз раствором гидрокарбоната натрия. После высушивания сульфатом магния этилацетатную фазу фильтровали и упаривали. Оставалось 26 г масла, которое очищали перегонкой в вакууме. Получили 20,7 г маслянистой жидкости (т.кип.0.5 76°C).
b) 2-(октагидро-4,7-метано-инден-5-ил)изоиндол-1,3-дион
К раствору 1,66 г 11 октагидро-4,7-метано-инден-5-ола, 1,47 г фталимида и 2,62 г трифенилфосфина в 15 мл ТГФ при перемешивании добавляли 1,7 г диэтилазодикарбоксилата, разбавленного 5 мл ТГФ. После выдерживания в течение ночи реакционную смесь упаривали, остаток перемешивали с простым эфиром, осадок отсасывали и фильтрат упаривали. Остаток очищали через силикагель/толуол. Получили 1,36 г желтого масла.
MS (CI+):282,2 (M+Н)+
с) экзо/экзооктагидро-4,7-метано-инден-5-иламин
К раствору 1,12 г 2-(октагидро-4,7-метано-инден-5-ил)изоиндол-1,3-диона в 15 мл этанола прибавляли по каплям 0,4 г гидразингидрата и перемешивали 2 ч при 65°С. Затем при помощи конц. HCl устанавливали рН 1-2, смешивали с 10 мл этанола, осадок отфильтровывали и фильтрат упаривали. Остаток очищали препаративной ВЭЖХ на RP-18 с ацетонитрилом/водой (0,05% трифторуксусной кислоты). После сушки вымораживанием получили 567 мг продукта в виде трифторацетата. Обработкой гидроокисью натрия и этилацетатом получено 322 мг свободного амина.
MS (CI+):152,0 (М+Н)+
Примеры
Если не указано иное, в приведенных примерах речь идет о рацематах.
Пример 1: (экзо/эндо)-(3-хлррбензил)-(октагидро-4,7-метано-инден-5-ил)амин-гидрохлорид
Раствор 0,54 г экзо/эндооктагидро-4,7-метано-инден-5-иламина (амина 1) и 0,562 г 3-хлорбензальдегида в 20 мл толуола после прибавления небольшого каталитического количества п-толуолсульфокислоты нагревали до кипения 5 часов и после выдерживания в течение ночи при комнатной температуре отгоняли растворитель. Остаток растворяли в метаноле и прибавляли к охлажденному льдом желтому раствору при перемешивании маленькими порциями 0,181 г бораната натрия. Перемешивали несколько часов при комнатной температуре и сильно подкисляли с помощью пересыщенного метанольного раствора хлористого водорода. После кратковременного перемешивания осадок отфильтровывали и отгоняли растворитель из фильтрата. Остаток образует от бесцветного до слабо-желтого кристаллическое вещество, т.пл. 241°С.
Пример 2: (экзо/эндо)-(3-фторбензил)-(3а,4,5,6,7,7а-гекса-гидро-1Н-4,7-метано-инден-5-ил)амин и (экзо/эндо)-(3-фтор-бензил)-(3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-ил)амин
300 мг смеси из 3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-иламина и 3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-иламина (смотри амин 1, а2), 315 мкл 3-фторбензальдегида, а также 10 мг п-толуолсульфокислоты растворяли в 5 мл толуола (безводного) и 5 часов кипятили с обратным холодильником. Затем летучие компоненты удаляли в вакууме, остаток извлекали 20 мл МеОН, добавляли 152 мг NaBH4 и выдерживали 15 часов при RT. Реакционную смесь разбавляли затем 200 мл ЭА и дважды промывали по 50 мл насыщенного водного раствора NaHCO3. Сушили над MgSO4 и растворитель удаляли в вакууме. Препаративной ВЭЖХ на RP-18 с ацетонитрилом/водой (градиент 5:95-95:5) получено 150 мг бесцветного масла.
Rf(ЭА)=0,40; MS (CI+):258 (М+H)+
Пример 3: (экзо/эндо)-(3а,4,5,6,7,7а-гексагидро-1Н-4,7-метано-инден-5-ил)-(3-метоксибензил)амин и (экзо/эндо)-(3а,4,5,6,7,7а-гексагидро-3Н-4,7-метано-инден-5-ил)(3-метоксибензил)амин
Соединения примера 3 были синтезирован