Производное индола, содержащее пиперидиновый цикл
Иллюстрации
Показать всеИзобретение относится к новым соединениям, представленным следующей формулой (I), или к его фармакологически приемлемым солям:
где R1 и R2 представляют собой заместители, смежные друг с другом, и вместе с двумя углеродными атомами, к каждому из которых они присоединены, образуют группу, представленную следующей формулой:
1) , или
2) , , , , , , , , или
3) или
4) , , или
где атом водорода в каждой циклической группе может быть замещенным 1-4 заместителями, выбранными из следующей группы заместителей B1, R3 представляет собой атом водорода или метальную группу; и R6 представляет собой заместитель, выбранный из следующей группы А1 заместителей, группа А1 заместителей: (1) атом водорода, (2) С1-С6 алкоксигруппа; группа B1 заместителей: (1) атом водорода, (2) гидроксильная группа, (3) оксогруппа, (4) С1-С6 алканоильная группа, (5) С3-С8 циклоалкильная группа, (6) С1-С6 алкильная группа (где указанная С1-С6 алкильная группа может быть замещенной С1-С6 алкоксигруппой), (7) С1-С6 алкоксигруппа, (8) С1-С6 алкоксииминогруппа, (9) С5-С6 циклоалкильная группа, образованная двумя С1-С3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (10) тетрагидропиранильная группа, образованная двумя С1-С3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным атомом углерода. Изобретение также относится к фармацевтической композиции. Технический результат - получение новых биологически активных соединений и фармацевтической композиции на их основе, обладающих ингибирующей активностью по отношению к серотониновым 1А рецепторам. 2 н. и 32 з.п. ф-лы, 12 табл., 4 ил.
Реферат
Настоящее изобретение относится к соединению, обладающему способностью связываться с серотониновым 1А рецептором, и к его применению в качестве фармацевтического препарата. Более конкретно, данное изобретение касается средства для лечения или профилактики симптомов со стороны нижних мочевых путей.
В периферической системе серотонин влияет на расслабление гладких мышц, агрегацию тромбоцитов и регуляцию деятельности желудочно-кишечного тракта. С другой стороны, в центральной нервной системе серотонин действует как нейротрансмиттер и глубоко связан с двигательной системой, перцептивной системой, физиологическими функциями, такими как регуляция температуры тела, сон, пищевое поведение, рвота, сексуальное поведение, нейроэндокринная система, познание и память или биоритм, и патологическими состояниями, такими как тревога, агрессия, обсессия, расстройство настроения, галлюцинация, шизофрения, аутизм или лекарственная зависимость (см., например, непатентный документ 1, непатентный документ 2).
Серотониновый рецептор классифицирован на 7 семейств в интервале от 5-НТ1 до 5-НТ7. 5-НТ1 состоит из 5 подтипов (5-НТ1A, 5-НТ1B, 5-НТ1C, 5-НТ1D, 5-НТ1E и 5-НТ1F).
Рецептор 5-НТ1А широко распределен в центральной нервной системе. В головном мозге данный рецептор распределен с высокой плотностью, особенно в церебральной лимбической системе, в основном в гиппокампе, перегородке, миндалевидном комплексе и ядрах шва. В спинном мозге он распределен с высокой плотностью в коре заднего рога, от которой отходят первичные афферентные волокна (слои I и II), внутренней части переднего рога, где локализованы мотонейроны (слои VIII-IX), и боковом промежуточном ядре, где находятся преганглионарные симпатические клетки (слой VII). В нерве сертониновый рецептор существует в качестве пресинаптического рецептора в клеточных телах серотонинового нерва (5-НТ1А соматодендрический ауторецептор) и в качестве постсинаптического рецептора на нерве, в котором иннервирует серотониновый нерв. Такой пресинаптический рецептор приводит к негативной регуляции с обратной связью с выделением серотонина.
Действие 5-НТ1А рецептора в живом организме и заболевания, в которые вовлечен рецептор, объяснены благодаря открытию агонистов и антагонистов, селективных по отношению к 5-НТ1А рецептору.
Примерами таких заболеваний являются депрессия и тревога. Считается, что пресинаптический 5-НТ1А рецептор важен при лечении депрессии. В качестве лекарственных средств в настоящее время используют селективный ингибитор обратного захвата серотонина (SSRI) и селективный ингибитор обратного захвата серотонина/норадреналина (SNRI). Указанные средства ингибируют поглощение указанных трансмиттеров в нервных клетках, повышая тем самым концентрацию трансмиттеров в синаптической щели и в результате десенсибилизируя рецептор, что и делает их эффективными. Недавно стало известно, что (-) пиндолол (который проявляет аффинность к адреналину β и 5НТ1А рецептору обладает антагонистическим действием в отношении 5НТ1А рецептора) промотирует начало фармакологических эффектов SSRI, тем самым увеличивая степень его эффективности у пациентов, подверженных депрессии. Это может происходить потому, что блокировка пресинаптического 5-НТ1А рецептора увеличивает выделение серотонина на нервных окончаниях, в результате чего усиливается десенсибилизация рецептора (см., например, непатентный документ 3).
Согласно исследованию Barros M. et al. с использованием мартышек предполагается возможность применения антагониста 5-НТ1А рецептора при тревожном расстройстве. Используя в качестве показателя страх и тревожное поведение мартышки при виде чучела хищного животного, исследовали эффект антагониста 5-НТ1А рецептора на тревогу. Результаты показали, что средство обладает анксиолитическим эффектом (см., например, непатентный документ 4). Указанные результаты говорили о возможности применения антагониста 5-НТ1А рецептора в качестве средства для профилактики или лечения депрессии или тревожного расстройства.
Предполагалось также, что 5-НТ1А рецептор связан с познавательной способностью, памятью и обучаемостью. Антагонист глутаматного рецептора типа NMDA или рассечение свода головного мозга вызывает расстройство познавательной способности. Такое расстройство познавательной способности лечат с использованием антагониста 5-НТ1А рецептора (см., например, непатентный документ 5 и непатентный документ 6). Yasuno F. et al. вводили человеку антагонист 5-HT1A рецептора, меченный 11C ([11C]WAY-100635). После этого они проверяли позитронной эмиссионной томографией взаимосвязь между памятью и участком, приходящимся на долю 5-НТ1А рецептора (см., например, непатентный документ 7). В результате была найдена негативная корреляция между улучшением памяти и способностью [11C]WAY-100635 связываться с гиппокампальным постсинаптическим 5-НТ1А рецептором. В соответствии с данным результатом предполагается, что постсинаптические 5-НТ1А рецепторы, распределенные по гиппокампу, оказывают негативное действие на память. Указанные результаты исследования предполагают возможность того, что антагонист 5-НТ1А рецептора эффективен при расстройстве познавательной способности или нарушении памяти или обучаемости.
Кроме того, в последние годы сообщалось (см., например, непатентный документ 8) о связи 5-НТ1А рецептора с рефлексом мочеиспускания.
Различные субъективные симптомы, вызываемые мочеиспускательной дисфункцией, в общем называют симптомами со стороны нижних мочевых путей. Такие симптомы со стороны нижних мочевых путей в широком плане разделены на симптомы, касающиеся накопления мочи, такие как учащенное мочеиспускание, сильная потребность в мочеиспускании или недержание мочи, и симптомы со стороны опорожнения мочевого пузыря, такие как затрудненное мочеиспускание или анурез. Недержание мочи дополнительно классифицируют на недержание мочи при напряжении, неудержание мочи, недержание при переполнении мочевого пузыря, рефлекторное недержание, экстрауртральное недержание или тому подобное. Недержание мочи, имеющее как симптом недержания при напряжении, так и симптом неудержания, называют смешанным недержанием мочи. В материалах международного общества International Continence Society (ICS) за 2001 г. дана следующая характеристика "Чрезмерно активный мочевой пузырь - это медицинское состояние, относящееся к симптомам частоты и повелительного позыва, с неудержанием мочи или без него, при появлении в отсутствие локальных патологических или метаболических факторов, которые были бы причиной указанных симтомов". Таким образом, патологическое состояние, устанавливаемое главным образом на основании субъективных симптомов, определено как чрезмерно активный мочевой пузырь.
Примеры причины симптомов, касающихся резервуарного накопления мочи, могут включать нейрогенный мочевой пузырь, вызываемый энцефалопатией (включая цереброваскулярное нарушение, болезнь Паркинсона, опухоль головного мозга, рассеянный склероз и т.п.), старческой деменцией, миелопатией или болезнью позвоночника, нестабильный мочевой пузырь, доброкачественную гиперплазию предстательной железы, рак предстательной железы, некроз мочевого пузыря, интерстициальный цистит мочевого пузыря, раздражение мочевого пузыря, вызываемое хроническим циститом или хроническим простатитом, цистоспазм, энурез (включая ночной энурез), никтурию и психогенную дизурию.
В исследованиях, касающихся рефлекса мочеиспускания у крыс, агонист 5-НТ1А рецептора способствует рефлексу мочеиспускания (см., например, непатентный документ 8), тогда как антагонист 5-НТ1А рецептора подавляет рефлекс мочеиспускания при измерении с использованием ритмического сжатия мочевого пузыря или цистометрограммы. Кроме того, в случае применения частичного агониста 5-НТ1А рецептора эффект подавления рефлекса мочеиспускания снижается в зависимости от степени агонистического действия указанного средства (см., например, непатентный документ 9). С учетом указанных результатов ожидается, что антагонист 5-НТ1А рецептора будет новым, основанным на новом механизме действия средством для лечения симптомов, касающихся накопления мочи (включая повышенную частоту мочеиспускания, острый позыв к мочеиспусканию и недержание мочи и т.д.) (см., например, непатентный документ 10).
Кроме описанных выше, существует широкий круг заболеваний, к которым причастен 5-НТ1А рецептор. Примеры таких заболеваний могут включать нейропсихическое расстройство (например, обсессивно-компульсивное расстройство (см., например, непатентный документ 11), пограничное личностное расстройство (см., например, непатентный документ 12), посттравматическое стрессовое расстройство (см., например, непатентный документ 13), паническое расстройство, шизофрению (см., например, непатентный документ 14), генитальную недостаточность (см., например, непатентный документ 14), алкогольную и/или кокаиновую зависимость (см., например, непатентный документ 15 и непатентный документ 16), нарушение сна (см., например, непатентный документ 14), боль (см., например, непатентный документ 14), мигрень (см., например, непатентный документ 17), расстройство зрительного внимания (см., например, непатентный документ 18), нестабильность температуры (см., например, непатентный документ 14), рвоту (см., например, непатентный документ 19), желудочно-кишечное расстройство (см., например, непатентный документ 14), расстройство приема пищи (см., например, непатентный документ 14), гипертензию (см., например, непатентный документ 20), нейродегенеративное заболевание (см., например, непатентный документ 21 и непатентный документ 22) (например, церебральную ишемию, болезнь Альцгеймера и т.д.), дискинезию, вызванную болезнью Паркинсона (см., например, непатентный документ 23), и симптомы, связанные с отказом от заглатывания никотина или курения (см., например, непатентный документ 24).
Соответственно, ожидается, что антагонист 5-НТ1А рецептора окажется средством для профилактики или лечения указанного широкого круга заболеваний. Хотя уже и были проведены активные исследования по созданию такого антагониста 5-НТ1А рецептора, такого средства на рынке еще нет. Поэтому создание превосходного антагониста 5-НТ1А рецептора было желательным.
Уже было много сообщений, касающихся соединений, обладающих антагонистическим эффектом против 5-НТ1А рецептора. Однако для применения в качестве средства для лечения симптомов со стороны нижних мочевых путей известно лишь несколько соединений, описанных в патентном документе 1 и патентном документе 2.
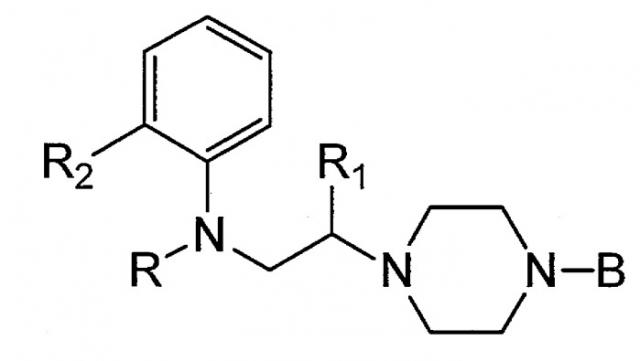
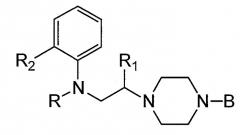
Соединением, описанным в патентном документе 1, является соединение, представленное следующей ниже формулой, или его фармакологически приемлемая соль:
где R представляет собой атом водорода или т.п.; R1 представляет собой атом водорода или т.п.; R2 представляет собой атом галогена или т.п. и В представляет собой моноциклическую арильную группу или т.п. Структурной особенностью данного соединения является то, что он содержит N-фениламиноалкильную группу в качестве пиперазиновой боковой цепи.
Таким образом, с точки зрения химической структуры соединение, описанное в патентном документе 1, совершенно отличается от представленного формулой (I) соединения по настоящему изобретению, отличающегося тем, что "оно содержит незамещенную или монозамещенную карбамоильную группу в положении 6 на индольном скелете и содержит метоксигруппу в арильной группе арилалкильной боковой цепи, отходящей от атома азота в пиперидиновом цикле, в ортоположении относительно алкильной боковой цепи".
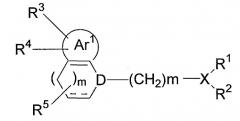
Патентный документ 2 является наиболее близким к настоящему изобретению известным уровнем техники. В данном документе раскрыто средство для лечения симптомов со стороны нижних мочевых путей, содержащее соединение, представленное следующей формулой, его соль или его гидрат:
где цикл Ar1 представляет собой бензольный цикл или т.п.; D представляет собой атом азота или т.п.; R3 и R4 являются одинаковыми или различными и представляют собой атомы водорода или т.п.; R5 представляет собой атом водорода или т.п.; R1 и R2 представляют собой атомы водорода или т.п. или связаны друг с другом с образованием цикла, содержащего Х; и m представляет собой 0 или целое число от 1 до 6.
Соединение, описанное в патентном документе 2, идентично описанному в патентном документе 3 соединению, представленному формулой (I), или соединению, описанному в примерах. Структурной особенностью данного соединения является то, что "оно имеет индольный или индолиновый скелет, содержащий циклический амин, который может быть замещенным арилалкильной группой или тому подобным в качестве боковой цепочечной структуры".
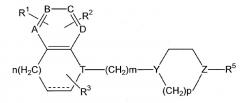
Среди соединений, раскрытых в патентном документе 3, конкретные примеры соединений, близких к соединению по настоящему изобретению, представленному формулой (I), могут включать соединения, представленные следующей формулой:
где каждый из R1 и R3 представляет собой атом водорода; R2 представляет собой карбамоильную группу; R5 представляет собой арилалкильную группу, которая может быть замещенной; n и m представляют собой 0; p представляет собой 2; каждый из T и Z представляет собой атом азота и Y представляет собой метиновую группу. Ближайшим соединением является соединение, описанное в примере 337. Однако указанные раскрытые соединения ограничены соединениями, "которые имеют индольный или индолиновый скелет, содержащий циклический амин, который может быть замещенным арилалкильной группой или тому подобным в качестве боковой цепи". Нет описаний с предложением соединения по настоящему изобретению, представленного формулой (I), "которое содержит незамещенную или монозамещенную карбамоильную группу в положении 6 на индольном скелете и содержит метоксигруппу в арильной группе арилалкильной боковой цепи, отходящей от атома азота в пиперидиновом цикле, в ортоположении относительно алкильной боковой цепи".
Таким образом, соединение, описанное в патентном документе 2, отличается от соединения по настоящему изобретению, представленного формулой (I), с точки зрения химической структуры и, следовательно, не имеет химической структуры, характерной для соединения по настоящему изобретению.
Кроме того, в патентном документе 2 описаны методики испытания на связывание с [3H]-8-гидроксидипропиламинотетралином (пример 1 испытания), испытания антагониста 5-HT1A рецептора (пример 2 испытания) и испытания, относящегося к антагонистическому действию против вызванной агонистом 5-HT1A рецептора гипотермии у крысы (пример 3 испытания). Однако в документе не раскрыты ни испытуемые соединения, ни конкретные результаты (фармакологические эффекты). Поэтому невозможно на основе таких описаний понять настоящее изобретение во всей его полноте.
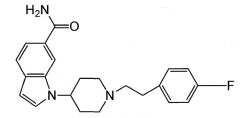
Среди соединений, описанных в патентном документе 3 и патентном документе 2, наиболее близким к соединению по настоящему изобретению, представленному формулой (I), является соединение, описанное в примере 337, которое представлено следующей формулой:
Как описано позже в результатах фармакологических исследований, фармакологический эффект данного соединения характеризуется тем, что соединение обладает аффинностью к 5-НТ1А, но его антагонистическое действие против рецептора слабо.
С другой стороны, соединение по настоящему изобретению, представленное следующей формулой (I):
отличается тем, что оно содержит незамещенную или монозамещенную карбамоильную группу в положении 6 на индольном скелете и содержит метоксигруппу в арильной группе арилалкильной боковой цепи, отходящей от атома азота в пиперидиновом цикле, в ортоположении относительно алкильной боковой цепи, благодаря чему обладает повышенным антагонизмом к 5-НТ1А рецептору.
Таким образом, соединение по настоящему изобретению обладает эффектами, которые совершенно отличны от эффектов соединений, описанных в патентном документе 3 и патентном документе 2.
Задачей настоящего изобретения является создание соединения, обладающего аффинностью к 5-НТ1А рецептору и проявляющего антагонизм к рецептору, используемый для терапевтических целей.
Непатентный документ 1: Peroutka S.J., 5-Hydroxytryptamine receptor subtypes, Annu. Rev. Neurosci. 1988; 11: p.45-60;
непатентный документ 2: H.Matsui, and three others, Neurotransmitter Today, 19(2), 1997, p.131-146;
непатентный документ 3: Farde L., and four others, PET-Determination of robalzotan (NAD-299) induced 5-HT(1A) receptor occupancy in the monkey brain, Neuropsychopharmacology, 2000 Apr.; 22(4): p.422-9;
непатентный документ 4: Barros M., and seven others, Anxiolytic-like effects of the selective 5-HT1A receptor antagonist WAY 100635 in non-human primates, Eur. J. Pharmacol., 2003 Dec. 15; 482(1-3): p.197-203;
непатентный документ 5: Harder JA, Ridley RM. The 5-HT1A antagonist, WAY 100635, alleviates cognitive impairments induced by dizocilpine (MK-801) in monkeys. Neuropharmacology. 2000 Feb. 14; 39(4): p.547-52:
непатентный документ 6: Harder JA, and four others, The 5-HT1A antagonist, WAY 100635, ameliorates the cognitive impairment induced by fornix transection in the marmoset. Psychopharmacology (Berl.). 1996 Oct.; 127(3): 245-54;
непатентный документ 7: Yasuno F., and nine others, Inhibitory effect of hippocampal 5-HT1A receptors on human explicit memory, Am. J. Psychiatry. 2003 Feb.; 160(2): p.334-40;
непатентный документ 8: Lecci A., and three others, Involvement of 5-hydroxytryptamine1A receptors in the modulation of micturition reflexes in the anesthetized rat, J. Pharmacol. Exp. Ther., 1992 Jul.; 262(1): p.181-9;
непатентный документ 9: Testa R., and nine others, Effect of several 5-hydroxytryptamine(1A) receptor ligands on the micturition reflex in rats: comparison with WAY 100635, J. Pharmacol. Exp. Ther., 1999 Sep.; 290(3): p.1258-69;
непатентный документ 10: Andersson KE, Pehrson R., CNS involvement in overactive bladder: pathophysiology and opportunities for pharmacological intervention, Drugs, 2003; 63(23): p.2595-611;
непатентный документ 11: Bourin M., and another, The future of antidepressants, Biomed Pharmacother., 1996; 50(1): p.7-12;
непатентный документ 12: Hansenne M., and seven others, 5-HT1A dysfunction in borderline personality disorder, Psychol. Med. 2002 Jul.; 32(5): p.935-41;
непатентный документ 13: Wilson MS., and another, Effects of fluoxetine on the 5-HT1A receptor and recovery of cognitive function after traumatic brain injury in rats, Am. J. Phys. Med. Rehabil., 2002 May; 81(5): p.364-72;
непатентный документ 14: Fletcher A., and two others, Silent 5-HT1A receptor antagonists: utility as research tools and therapeutic agents, Trends Pharmacol. Sci., 1993 Dec.; 14(12): p.441-8;
непатентный документ 15: Zhou FC., and three others, Additive reduction of alcohol drinking by 5-HT1A antagonist WAY 100635 and serotonin uptake blocker fluoxetine in alcohol-preferring P rats, Alcohol. Clin. Exp. Res., 1998 Feb.; 22(1): p.266-9;
непатентный документ 16: Carey RJ., and two others, 5-HT1A agonist/antagonist modification of cocaine stimulant effects: implications for cocaine mechanisms. Behav Brain Res., 2002 Apr. 15; 132(1): p.37-46;
непатентный документ 17: Boers PM., and three others, Naratriptan has a selective inhibitory effect on trigeminovascular neurones at central 5-HT1A and 5-HT(1B/1D) receptors in the cat: implications for migraine therapy, Cephalalgia., 2004 Feb.; 24(2): p.99-109;
непатентный документ 18: Balducci C., and four others, Reversal of visual attention dysfunction after AMPA lesions of the nucleus basalis magnocellularis (NBM) by the cholinesterase inhibitor donepezil and by a 5-HT1A receptor antagonist WAY 100635, Psychopharmacology (Berl.), 2003 Apr.; 167(1): p.28-36;
непатентный документ 19: Gupta YK., and another, Involvement of 5-HT1A and 5-HT2 receptor in cisplatin induced emesis in dogs, Indian J. Physiol. Pharmacol., 2002 Oct.; 46(4): p.463-7;
непатентный документ 20: Dabire H., Central 5-hydroxytryptamine (5-HT) receptors in blood pressure regulation, Therapie., 1991 Nov.-Dec.; 46(6): p.421-9;
непатентный документ 21: Kruger H., and two others, Effects of ionotropic glutamate receptor blockade and 5-HT1A receptor activation on spreading depression in rat neocortical slices, Neuroreport., 1999 Aug. 20; 10(12): p.2651-6;
непатентный документ 22: Suchanek B., and two others, The 5-HT1A receptor agonist BAY x 3702 prevents staurosporine-induced apoptosis, Eur. J. Pharmacol., 1998 Aug. 14; 355(1): p.95-101;
непатентный документ 23: Bibbiani F., and two others, Serotonin 5-HT1A agonist improves motor complications in rodent and primate parkinsonian models, Neurology., 2001 Nov. 27; 57(10): p.1829-34;
непатентный документ 24: Kurt Rasmussen, and sixteen others, The Novel 5-Hydroxytryptamine1A Antagonist LY426965: Effects on Nicotine Withdrawal and Interactions with Fluoxetine, J. of Pharmacol. Experimental. Therapeutics., 294: 688-700: (2000);
патентный документ 1: международная публикация WO99/06384;
патентный документ 2: JP-A-2002-114684;
патентный документ 3: международная публикация WO98/43956.
Как указано выше, можно ожидать, что соединение, обладающее способностью связываться с 5-НТ1А рецептором и также проявляющее антагонистический эффект против указанного рецептора, будет средством для лечения симптомов со стороны нижних мочевых путей, основанным на новом механизме действия. Однако соединение, которое обладает высокой способностью связываться с 5-НТ1А рецептором и проявляет антагонизм к данному рецептору и которое способно оказывать превосходное клиническое действие в лечении или профилактике симптомов со стороны нижних мочевых путей и, в частности, симптомов, касающихся накопления мочи, все еще не найдено.
Средство для решения проблем
При указанных обстоятельствах авторы настоящего изобретения провели интенсивные исследования. В результате они нашли, что соединение, описанное ниже, которое обладает способностью связываться с 5-НТ1А рецептором и оказывает антагонистическое действие против данного рецептора, полезно в качестве средства для лечения или профилактики симптомов со стороны нижних мочевых путей и, в частности, повышенной частоты мочеиспускания или недержания мочи, что в конечном счете и завершилось настоящим изобретением.
Таким образом, настоящее изобретение характеризуется следующими отличительными признаками 1)-34):
1) Соединение, представленное следующей формулой (I), или его фармакологически приемлемлемая соль:
где R1 и R2 представляют собой заместители, смежные друг с другом, и вместе с двумя углеродными атомами, к каждому из которых они присоединены, образуют:
(1) 5-7-членную неароматическую карбоциклическую группу,
(2) 5-7-членную неароматическую гетероциклическую группу,
(3) 6-членную ароматическую карбоциклическую группу или
(4) 5- или 6-членную ароматическую гетероциклическую группу,
которая может быть замещенной 1-4 заместителями, выбранными из следующей группы заместителей B1;
R3 представляет собой атом водорода или метильную группу; и
R6 представляет собой заместитель, выбранный из следующей группы А1 заместителей,
группа А1 заместителей: (1) атом водорода, (2) атом галогена, (3) цианогруппа, (4) гидроксильная группа, (5) нитрогруппа, (6) карбоксильная группа, (7) C3-C8 циклоалкильная группа, (8) C2-C6 алкенильная группа, (9) C2-C6 алкинильная группа, (10) C1-C6 алкилтиогруппа, (11) C1-C6 алкоксикарбонильная группа, (12) C1-C6 алкилсульфонильная группа, (13) C1-C6 алкильная группа (где описанная выше C1-C6 алкильная группа может быть замещенной 1-3 заместителями, выбранными из группы, состоящей из атома галогена, гидроксильной группы и C1-C6 алкоксигруппы), (14) C1-C6 алкоксигруппа (где описанная выше C1-C6 алкоксигруппа может быть замещенной 1-3 атомами галогена), (15) аминогруппа (где описанная выше аминогруппа может быть замещенной заместителем, выбранным из группы, состоящей из C1-C6 алкильной группы, формильной группы, C1-C6 алканоильной группы и C1-C6 алкилсульфонильной группы) и (16) карбамоильная группа (где описанная выше карбамоильная группа может быть замещенной одной или двумя C1-C6 алкильными группами),
группа В1 заместителей: (1) атом водорода, (2) атом галогена, (3) цианогруппа, (4) гидроксильная группа, (5) нитрогруппа, (6) оксогруппа, (7) карбоксильная группа, (8) C3-C8 циклоалкильная группа, (9) C2-C6 алкенильная группа, (10) C2-C6 алкинильная группа, (11) C1-C6 алкилтиогруппа, (12) C1-C6 алкоксикарбонильная группа, (13) C1-C6 алкилсульфонильная группа, (14) C1-C6 алкильная группа (где описанная выше C1-C6 алкильная группа может быть замещенной атомом галогена, гидроксильной группой или C1-C6 алкоксигруппой), (15) C1-C6 алкоксигруппа (где описанная выше C1-C6 алкоксигруппа может быть замещенной 1-3 атомами галогена), (16) аминогруппа (где описанная выше аминогруппа может быть замещенной заместителем, выбранным из группы, состоящей из C1-C6 алкильной группы, формильной группы, C1-C6 алканоильной группы и C1-C6 алкилсульфонильной группы), (17) карбамоильная группа (где описанная выше карбамоильная группа может быть замещенной одной или двумя C1-C6 алкильными группами), (18) C1-C6 алкоксииминогруппа, (19) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (20) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
2) соединение по описанному выше пункту 1) или его фармакологически приемлемая соль, где R1 и R2 представляют собой заместители, смежные друг с другом, и вместе с двумя углеродными атомами, к каждому из которых они присоединены, образуют группу, представленную следующей формулой:
где атом водорода в каждой циклической группе может быть замещенным 1-4 заместителями, выбранными из следующей группы В1 заместителей,
группа В1 заместителей: (1) атом водорода, (2) атом галогена, (3) цианогруппа, (4) гидроксильная группа, (5) нитрогруппа, (6) оксогруппа, (7) карбоксильная группа, (8) C3-C8 циклоалкильная группа, (9) C2-C6 алкенильная группа, (10) C2-C6 алкинильная группа, (11) C1-C6 алкилтиогруппа, (12) C1-C6 алкоксикарбонильная группа, (13) C1-C6 алкилсульфонильная группа, (14) C1-C6 алкильная группа (где описанная выше C1-C6 алкильная группа может быть замещенной атомом галогена, гидроксильной группой или C1-C6 алкоксигруппой), (15) C1-C6 алкоксигруппа (где описанная выше C1-C6 алкоксигруппа может быть замещенной 1-3 атомами галогена), (16) аминогруппа (где описанная выше аминогруппа может быть замещенной заместителем, выбранным из группы, состоящей из C1-C6 алкильной группы, формильной группы, C1-C6 алканоильной группы и C1-C6 алкилсульфонильной группы), (17) карбамоильная группа (где описанная выше карбамоильная группа может быть замещенной одной или двумя C1-C6 алкильными группами), (18) C1-C6 алкоксииминогруппа, (19) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (20) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
3) соединение по описанному выше пункту 1) или его фармакологически приемлемая соль, которое представлено формулой (I-a-1), формулой (I-a-2), формулой (I-a-3) или (I-a-4):
где R3 представляет собой атом водорода или метильную группу; R4a и R5a представляют собой заместители, выбранные из следующей группы В1 заместителей; R6 представляет собой заместитель, выбранный из следующей группы А1 заместителей; R11a представляет собой гидроксильную группу, R12a представляет собой атом водорода или C1-C6 алкильную группу или R11a и R12a представляют собой карбонильную группу или группу формулы C=N-OR8c (где R8c представляет собой C1-C6 алкильную группу) вместе с углеродными атомами, к которым присоединены R11a и R12a; Xa представляет собой метиленовую группу, где атом водорода указанной выше метиленовой группы может быть замещен заместителем, выбранным из следующей группы В1 заместителей, или атом кислорода; и na представляет собой целое число от 1 до 3,
группа А1 заместителей: (1) атом водорода, (2) атом галогена, (3) цианогруппа, (4) гидроксильная группа, (5) нитрогруппа, (6) карбоксильная группа, (7) C3-C8 циклоалкильная группа, (8) C2-C6 алкенильная группа, (9) C2-C6 алкинильная группа, (10) C1-C6 алкилтиогруппа, (11) C1-C6 алкоксикарбонильная группа, (12) C1-C6 алкилсульфонильная группа, (13) C1-C6 алкильная группа (где описанная выше C1-C6 алкильная группа может быть замещенной 1-3 заместителями, выбранными из группы, состоящей из атома галогена, гидроксильной группы и C1-C6 алкоксигруппы), (14) C1-C6 алкоксигруппа (где описанная выше C1-C6 алкоксигруппа может быть замещенной 1-3 атомами галогена), (15) аминогруппа (где описанная выше аминогруппа может быть замещенной заместителем, выбранным из группы, состоящей из C1-C6 алкильной группы, формильной группы, C1-C6 алканоильной группы и C1-C6 алкилсульфонильной группы) и (16) карбамоильная группа (где описанная выше карбамоильная группа может быть замещенной одной или двумя C1-C6 алкильными группами),
группа В1 заместителей: (1) атом водорода, (2) атом галогена, (3) цианогруппа, (4) гидроксильная группа, (5) нитрогруппа, (6) оксогруппа, (7) карбоксильная группа, (8) C3-C8 циклоалкильная группа, (9) C2-C6 алкенильная группа, (10) C2-C6 алкинильная группа, (11) C1-C6 алкилтиогруппа, (12) C1-C6 алкоксикарбонильная группа, (13) C1-C6 алкилсульфонильная группа, (14) C1-C6 алкильная группа (где описанная выше C1-C6 алкильная группа может быть замещенной атомом галогена, гидроксильной группой или C1-C6 алкоксигруппой), (15) C1-C6 алкоксигруппа (где описанная выше C1-C6 алкоксигруппа может быть замещенной 1-3 атомами галогена), (16) аминогруппа (где описанная выше аминогруппа может быть замещенной заместителем, выбранным из группы, состоящей из C1-C6 алкильной группы, формильной группы, C1-C6 алканоильной группы и C1-C6 алкилсульфонильной группы), (17) карбамоильная группа (где описанная выше карбамоильная группа может быть замещенной одной или двумя C1-C6 алкильными группами), (18) C1-C6 алкоксииминогруппа, (19) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (20) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
4) соединение по описанному выше пункту 3) или его фармакологически приемлемая соль, где R11a и R12a образуют карбонильную группу, вместе с атомами углерода, к которым R11a и R12a присоединены;
5) соединение по описанному выше пункту 3) или 4) или его фармакологически приемлемая соль, где R4a и R5a представляют собой заместители, выбранные из следующей группы В2 заместителей, и R6 представляет собой заместитель, выбранный из следующей группы А2 заместителей,
группа А2 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) атом галогена, (4) цианогруппа, (5) C1-C6 алкоксигруппа, (6) аминогруппа, где атом азота может быть замещенным C1-C6 алкильной группой, и (7) C1-C6 алкокси-С1-C6 алкильная группа,
группа В2 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) атом галогена, (4) гидроксильная группа, (5) C1-C6 алкоксигруппа, (6) C1-C6 алкокси-С1-C6 алкильная группа, (7) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (8) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
6) соединение по любому из описанных выше пунктов 3)-5) или его фармакологически приемлемая соль, где R4a и R5a представляют собой заместители, выбранные из следующей группы В5 заместителей, и R6 представляет собой заместитель, выбранный из следующей группы А4 заместителей,
группа А4 заместителей: (1) атом водорода и (2) C1-C6 алкоксигруппа,
группа В5 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) C1-C6 алкокси-С1-C6 алкильная группа, (4) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (5) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
7) соединение по любому из описанных выше пунктов 3)-6) или его фармакологически приемлемая соль, где Xa представляет собой атом кислорода;
8) соединение по описанному выше пункту 1) или его фармакологически приемлемая соль, которое представлено формулой (I-b-1), формулой (I-b-2), формулой (I-b-3) или формулой (I-b-4):
где R4a и R5a представляют собой заместители, выбранные из следующей группы В5 заместителей, и R6 представляет собой заместитель, выбранный из следующей группы А4 заместителей,
группа А4 заместителей: (1) атом водорода и (2) C1-C6 алкоксигруппа,
группа В5 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) C1-C6 алкокси-С1-C6 алкильная группа, (4) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (5) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
9) соединение по описанному выше пункту 3) или его фармакологически приемлемая соль, где R11a представляет собой гидроксильную группу и R12a представляет собой атом водорода или C1-C6 алкильную группу;
10) соединение по описанному выше пункту 9) или его фармакологически приемлемая соль, где R4a и R5a представляют собой заместители, выбранные из следующей группы В2 заместителей, и R6 представляет собой заместитель, выбранный из следующей группы А2 заместителей,
группа А2 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) атом галогена, (4) цианогруппа, (5) C1-C6 алкоксигруппа, (6) аминогруппа, где атом азота может быть замещенным С1-С6 алкильной группой, и (7) C1-C6 алкокси-С1-C6 алкильная группа,
группа В2 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) атом галогена, (4) гидроксильная группа, (5) C1-C6 алкоксигруппа, (6) C1-C6 алкокси-С1-C6 алкильная группа, (7) C5-C6 циклоалкильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, и (8) тетрагидропиранильная группа, образованная двумя C1-C3 алкильными группами, присоединенными к одному и тому же углеродному атому, вместе с атомом кислорода и указанным выше атомом углерода;
11) соединение по описанному выше пункту 9) или 10) или его фармакологически приемлемая соль, где Xa представляет собой атом кислорода;
12) соединение по описанному выше пункту 3) или его фармакологически приемлемая соль, где R11a и R12a вместе образуют группу формулы =N-OR8c (где R8c представляет собой C1-C6 алкильную группу);
13) соединение по описанному выше пункту 12) или его фармакологически приемлемая соль, где R4a и R5a представляют собой заместители, выбранные из следующей группы В3 заместителей, и R6 представляет собой заместитель, выбранный из следующей группы А2 заместителей,
группа А2 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) атом галогена, (4) цианогруппа, (5) C1-C6 алкоксигруппа, (6) аминогруппа, где атом азота может быть замещенным С1-С6 алкильной группой, и (7) C1-C6 алкокси-С1-C6 алкильная группа,
группа В3 заместителей: (1) атом водорода, (2) C1-C6 алкильная группа, (3) атом галогена, (4) гидроксильная группа, (5) C1-C6 алкоксигруппа и (6) C1-C6 алкокси-С1-C6 алкильная группа;
14) соединение по описанному выше пункту 12) или 13) или его фармакологически приемлемая соль, где Xa представляет собой атом кислорода;
15) соединение по описанному выше пункту 1) или его фармакологически приемлемая соль, которое представлено формулой (I-c-1) или формулой (I-c-2):
где R3 представляет собой атом водорода или метильную группу и R4d, R5d и R6 представляют собой заместители, выбранные из следующей группы А1 заместителей,
группа А1 заместителей: (1) атом водорода, (2) атом галогена, (3) цианогруппа, (4) гидроксильная группа, (5) нитрогруппа, (6) карбоксильная группа, (7) C3-C8 циклоалкильная группа, (8) C2-C6 алкенильная группа, (9) C2-C6 алкинильная группа, (10) C1-C6 алкилтиогруппа, (11) C1-C6 алкоксикарбонильная группа, (12) C1-C6 алкилсульфонильная группа, (13) C1-C6 алкильная группа (где описанная выше C1-C6 алкильная группа может быть замещенной 1-3 заместителями, выбранными из группы, состоящей из атома галогена, гидроксильной группы и C1-C6 алкоксигруппы), (14) C1-C6 алкоксигруппа (где описанная выше C1-C6 алкоксигруппа может быть замещенной 1-3 атомами галогена), (15) аминогруппа (где описанная выше аминогруппа может быть замещенной заместителем, выбранным из группы, состоящей из C1-C6 алкильной группы, формильной группы, C1-C6 алканоильной группы и C1-C6 алкилсульфонильной группы) и (16) карбамоильная группа (где описанная выше карбамоильная группа может быть замещенной одной или двумя C1-C6 алкильными группами);
16) соединение по описанному выше пункту 15) или его фармакологически приемлемая соль, где R4d и R5d представляют собой заместители, выбранные из следующей группы В4 заместителей, и R6 представляет собой