Мицеллы белка молочной сыворотки
Иллюстрации
Показать всеИзобретение относится к пищевой промышленности и касается растворимых мицелл сывороточного белка, имеющих размер менее 1 мкм и представляющих собой сферические агломераты денатурированного сывороточного белка, при этом сывороточные белки локализуются таким образом, что их гидрофильные части ориентированы в сторону наружной части агломерата, а гидрофобные части - в сторону внутренней «сердцевины» указанных мицелл, а также растворимых мицелл сывороточного белка в виде концентрата и порошка и их применения в пригодных к употреблению продуктах и способах производства этих продуктов. Изобретение может быть использовано в качестве эмульгаторов, жирозаменителей, заменителей мицеллярного казеина или пенообразующего агента и позволяет получать продукты, обогащенные белком, с отбеливающим/опалесцирующим эффектом, со сниженной жирностью, придавать им кремообразную текстуру, сливочное вкусовое ощущение во рту. 8 н. и 30 з.п. ф-лы, 20 ил., 14 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение касается мицелл белка молочной сыворотки (далее по тексту - мицелл сывороточного белка), в частности применения концентратов и порошков указанных мицелл в широком перечне пищевой продукции.
Уровень техники
Белок составляет неотъемлемую часть рационов питания многих людей. Он используется не только из-за его питательной ценности, но и из-за его способности придавать требуемую текстуру и стабилизировать пищевые продукты. Например, в жиросодержащих продуктах жир должен оставаться стабильным в течение всего срока хранения продукта во избежание разделения на фазы.
Для этой цели используются эмульгаторы, которые стабилизируют образовавшуюся эмульсию благодаря присущему им свойству способствовать растворению липофильной или гидрофобной части в неводной фазе, а полярной или гидрофильной части - в воде, т.е. указанные молекулы облегчают эмульгирование одной фазы в другой фазе. В дополнение к этому, эмульгаторы предупреждают также агрегацию и коалесценцию уже сформировавшихся капель. В качестве эмульгаторов используются природные вещества, такие как гидроколлоиды, фосфолипиды (лецитин) или гликолипиды, но, с другой стороны, могут использоваться также и синтетические агенты, такие как стеарил-2-лактилат или моно-, диацилглицериды и др.
Одним из основных недостатков этих агентов является то, что они в некоторых случаях приводят к значительному удорожанию стоимости готового продукта и не способствуют повышению его питательной ценности. В некоторых случаях такого рода материалы не показывают также адекватной стабилизирующей способности из-за конкуренции с белками на границе раздела фаз.
Поэтому белок все чаще используется и как эмульгатор, и как частичный заменитель жира.
US 6767575 В1 раскрывает способ производства продукта сывороточных белков в форме агрегатов, который предусматривает денатурацию сывороточных белков путем подкисления и тепловой обработки. Полученные таким способом белковые агрегаты используются в пищевой промышленности.
GB 1079604 описывает улучшенный способ производства сыра, в котором сывороточные белки подвергаются тепловой обработке при оптимальном значении рН с целью получения нерастворимых сывороточных белков, которые затем добавляются в сырое молоко для сыра.
WO 93/07761 касается получения сухого белкового продукта из микрочастиц, который может использоваться в качестве жирозаменителя.
US 5750183 раскрывает способ производства белковых микрочастиц, которые пригодны для применения в качестве жирозаменителя, не содержащего жира.
Белковый жирозаменитель раскрывается также в WO 91/17665, в котором белок присутствует в виде денатурированного сывороточного белка из микрочастиц, способного диспергироваться в воде.
Помимо пищевых продуктов, белки присутствуют также во многих фармацевтических и косметических композициях.
Однако одной из проблем, связанных с производством продуктов, содержащих в большинстве случаев глобулярные белки, в частности белки молочной сыворотки, является их ограниченная технологичность в обработке в условиях промышленного пищевого производства. В действительности белковые молекулы при тепловой обработке или в кислотном, либо щелочном окружении, или в присутствии солей теряют свою нативную структуру и перестраиваются в различные произвольные структуры, такие как, например, гели.
Производство гелеобразных (желированных) водных композиций белков молочной сыворотки является предметом изобретения ЕР 1281322.
Elofsson et al. в "International Dairy Journal", 1997, p.601-608, описывает способ холодного желирования концентратов белков молочной сыворотки.
Равным образом Kilara et al. в "Journal of Agriculture and Food Chemistry", 1998, p.1830-1835, описывает влияние рН на агрегацию сывороточных белков и образование ими гелей.
Этот эффект гелеобразования является причиной ограничения в рамках не только технологичности в обработке (например, засорение машин, используемых в производстве белоксодержащих продуктов), но и в рамках формирования текстуры, которая может быть неприемлемой в большинстве сфер применения белка.
Поэтому в целях расширения сферы применения белков крайне желательно контролировать их денатурацию.
В материалах 2-й Международной конференции по молочной сыворотке, состоявшейся в октябре 1997 г. в Чикаго, США (Proceedings of the Second International Whey Conference, Chicago, October 1997), о которой сообщается в бюллетенях Международной Молочной Федерации, 1998, 189-196, Britten М. обсуждает вопросы тепловой обработки сывороточных белков с точки зрения улучшения их функциональных свойств. Описан способ производства дисперсии сывороточных белков в форме микрочастиц при 95°C.
Erdman в "Journal of American College of Nutrition", 1990, p.398-409, указывает на то, что качество белка в форме микрочастиц не страдает в случае применения высокого усилия сдвига и нагрева.
ЕР 0603981 также описывает стабильную к нагреву эмульсию масло-в-воде, содержащую белки.
Sato et al. в US 5 882 705 получил мицеллярный сывороточный белок путем тепловой обработки раствора гидролизованного сывороточного белка. Этот мицеллярный белок характеризуется неправильной формой.
Таким образом, задачей изобретения является расширение сферы использования белков в промышленных производственных процессах и обеспечение пригодных для потребления продуктов на белковой основе.
Раскрытие изобретения
Указанная цель соответственно достигается с помощью отличительных признаков самостоятельных пунктов формулы изобретения. Зависимые пункты формулы развивают далее основную идею настоящего изобретения.
Таким образом, в первом аспекте изобретения обеспечивается пригодный для потребления продукт, содержащий мицеллы сывороточного белка.
В частности, настоящее изобретение касается продукта типа майонеза с повышенной кислотностью, содержащего растворимые мицеллы сывороточного белка.
В другом аспекте изобретение относится к такому продукту, как суп или соус, содержащему растворимые мицеллы сывороточного белка и имеющему содержание соли от 0,01% до 3%, предпочтительно - от 0,1% до 2,5%.
Способ производства пригодного для употребления продукта по любому из пунктов формулы 1-28, включающий стадии:
(а) смешивания мицелл сывороточного белка, их концентрата или порошка с прочими ингредиентами продукта и
(б) обработки смеси,
также является частью настоящего изобретения.
В следующем аспекте настоящее изобретение касается обезвоженного пищевого продукта, содержащего порошок мицелл сывороточного белка и сухие пищевые ингредиенты.
Соответственно обеспечивается также способ производства пригодного для употребления продукта по любому из пунктов формулы 29-34, включающий стадии:
(а) смешивания порошка мицелл сывороточного белка с прочими сухими ингредиентами продукта или
(б) совместной сушки раствора мицелл сывороточного белка с прочими ингредиентами продукта.
Описание фигур
Настоящее изобретение описывается ниже со ссылкой на некоторые предпочтительные варианты его воплощения, представленные на прилагаемых к описанию фигурах, из которых:
Фиг.1 показывает результат эксперимента, демонстрирующего влияние рН и тепловой обработки на мицеллизацию (мицеллообразование) β-лактоглобулина.
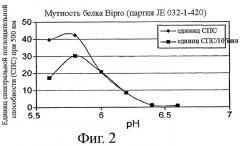
Фиг.2 демонстрирует возможность определения рН мицеллизации на примере выпускаемого промышленностью белкового препарата (Bipro®, партия JE032-1-420) на основе измерений мутности при 500 нм.
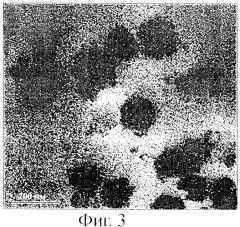
Фиг.3 представляет собой ТЕМ (трансмиссионная электронная микроскопия) микрофотографию мицелл сывороточного белка (2 мас.%, WPI 95 (изолят белка молочной сыворотки), Lactalis) при рН 7,4. Масштабная шкала: 200 нм.
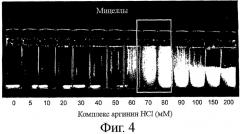
Фиг.4 демонстрирует результат эксперимента по оценке влияния ионной силы (комплекса аргинин НСl) на образование белковых мицелл при постоянном рН, равном 7,0.
Фиг.5 демонстрирует объемную стабильность (FVS) пены, стабилизированной 1 мас.%, мицелл β-лактоглобулина (от Davisco) при рН 7,0 в присутствии 60 мМ аргинина НСl, по сравнению с не подвергавшимся мицеллизации β-лактоглобулином.
Фиг.6 демонстрирует гидродинамический диаметр (на основе эквивалентной интенсивности) сывороточного белка, полученного путем тепловой обработки 1 мас.% дисперсии β-лактоглобулина при 85°С, 15 мин, при рН от 2 до 8. Мицеллы сывороточного белка получены при рН 4,25 (положительно заряженные зета-потенциал около +25 мВ) и при рН 6,0 (отрицательно заряженные зета-потенциал около -30 мВ). Z-усредненный гидродинамический диаметр мицелл составил 229,3 нм при рН 4,25 и 227,2 нм при рН 6,0. Представлены соответствующие микрофотографии, полученные с помощью ТЕМ с применением негативного окрашивания. Масштабная шкала: 1 мкм.
Фиг.7 демонстрирует схематическое изображение структуры мицеллы сывороточного белка.
Фиг.8 представляет собой SEM (сканирующая электронная микроскопия) микрофотографию порошка мицелл сывороточного белка, полученного распылительной сушкой дисперсии с содержанием белка 20% после микрофильтрации.
Фиг.9 представляет собой негативно окрашенную ТЕМ-микрофотографию дисперсии мицелл сывороточного белка, полученной при содержании белка 4%.
Фиг.10 представляет собой негативно окрашенную ТЕМ-микрофотографию дисперсии мицелл сывороточного белка, полученной при содержании белка 20% после микрофильтрации.
Фиг.11 демонстрирует теплоустойчивость дисперсии мицелл сывороточного белка, полученной при содержании белка 10% после микрофильтрации при рН 7,0 в присутствии NaCl после тепловой обработки при 85°С, 15 мин.
Фиг.12 демонстрирует теплоустойчивость дисперсии мицелл сывороточного белка, полученной при содержании белка 4% при рН 7,0 в присутствии NaCl после тепловой обработки при 85°С, 15 мин.
Фиг.13 представляет собой негативно окрашенную ТЕМ-микрофотографию 4%-й дисперсии мицелл сывороточного белка, полученной путем диспергирования порошка чистых мицелл сывороточного белка при 50°C в деионизированной воде.
Фиг.14 представляет собой диаграмму, показывающую распределение по размерам мицелл, полученных способом по изобретению с использованием 4% изолята сывороточного белка Prolacta 90, обработанного при рН 5,9.
Фиг.15 представляет собой SEM-микрофотографию, показывающую внутреннюю структуру на разрезе гранулы порошка, полученного распылительной сушкой, которая показана на фиг.8.
Фиг.16 представляет собой негативно окрашенную ТЕМ-микрофотографию 4% дисперсии мицелл сывороточного белка, полученной путем диспергирования полученного сублимационной сушкой порошка чистых мицелл сывороточного белка при комнатной температуре в деионизированной воде. Масштабная шкала: 0,5 микрометра.
Фиг.17 демонстрирует схематично изображенный процесс покрытия WPM (мицеллы сывороточного белка) сульфатированным бутил-олеатом (SBO) при увеличении соотношения смешивания при рН 3,0. Серые кружочки: WPM с положительным поверхностным зарядом. Черные головки с хвостиками: отрицательно заряженные головные и гидрофобные хвостовые части SBO.
Фиг.18 представляет собой фотографию концентрата мицелл сывороточного белка, полученного выпариванием 20% дисперсии белка, в которую были добавлены 4% NaCl.
Фиг.19 представляет собой полученную микроскопией в проходящем свете микрофотографию полутонкого среза порошка мицелл сывороточного белка после окрашивания толуидиновым синим. Масштабная шкала: 50 микрон.
Фиг.20 представляет собой SEM-микрофотографию разреза полой частицы порошка мицелл сывороточного белка. Слева: внутренняя структура. Справа: детальное изображение мицеллы сывороточного белка, составляющей матрицу частицы порошка. Масштабная шкала: 10 и 1 микрон, соответственно.
Осуществление изобретения
На фиг.7 схематически показаны мицеллы по настоящему изобретению, в которых сывороточные белки локализованы таким образом, что их гидрофильные части ориентированы в сторону наружной части агломерата, а гидрофобные части - в сторону внутренней "сердцевины" мицеллы. Такая энергетически благоприятная конфигурация придает указанным структурам высокую стабильность в гидрофильном окружении.
Специфическую структуру мицелл можно видеть на фигурах, в частности на фиг.3, 9, 10, 13 и 15, на которых мицеллы состоят преимущественно из сферических агломератов денатурированного сывороточного белка. Мицеллы характеризуются, в частности, правильной сферической формой.
Вследствие их двойственного характера (гидрофильного и гидрофобного) указанное денатурированное состояние белка обусловливает, по-видимому, взаимодействие между гидрофобной фазой (например, каплей жира или воздуха) и гидрофильной фазой. Поэтому мицеллы сывороточного белка обладают отличными эмульгирующими и пенообразующими свойствами.
Кроме того, мицеллы, полученные способом по изобретению, характеризуются распределением по размерам в чрезвычайно узком диапазоне (см. фиг.14), так что более 80% образовавшихся мицелл имеют размер менее 1 микрона, предпочтительно - от 100 до 900 нанометров (нм), более предпочтительно - от 100 до 770 нм, наиболее предпочтительно - от 200 до 400 нм.
Средний диаметр мицелл можно определять с помощью трансмиссионной электронной микроскопии (ТЕМ). Для этого жидкие образцы мицелл инкапсулируют в пробирки с агаровым гелем. Фиксация достигается при погружении в раствор 2,5% глутаральдегида в 0,1 М буфере какодилата с рН 7,4, а вторичная фиксация - при погружении в раствор 2% тетроксида осмия в том же буфере, при этом оба раствора содержат 0,04% рутения красного. После дегидратации в этаноле возрастающей концентрации (70, 80, 90, 96, 100%-й этанол) образцы заливают смолой Spurr (смола с низкой вязкостью) в соотношении смола:этанол=1:1, 2:1 (100%-й этанол). После полимеризации смолы (70°С, 48 часов) на ультрамикротоме Leica ultracut UCT готовят полутонкие и ультратонкие срезы. Затем ультратонкие срезы, контрастированные водным раствором уранилацетата и цитрата свинца, изучают под трансмиссионным электронным микроскопом (Philips СМ12, 80 кВ).
Не желая останавливаться на теории, авторы изобретения выдвинули предположение, что в процессе мицеллообразования по способу изобретения мицелла достигает "максимального размера" благодаря ее общему электростатическому заряду, отталкивающему дополнительные белковые молекулы, так что мицелла больше не может увеличиваться в размере. Это, по-видимому, и является причиной наблюдаемого распределения по размерам в столь узком диапазоне (ср. фиг.14).
Вышеописанные мицеллы можно получать способом, подробно описанным ниже.
В качестве сывороточного белка, пригодного для использования в способе по изобретению, могут служить любые выпускаемые промышленностью изоляты или концентраты белков молочной сыворотки, т.е. белки молочной сыворотки, полученные способом производства таких белков, известным из уровня техники, а также фракции белков молочной сыворотки, выделенные из них, или такие белки, как β-лактоглобулин (β-LG), α-лактальбумин и сывороточный альбумин. В частности, в качестве сывороточного белка можно использовать сладкую сыворотку, являющуюся побочным продуктом сыроделия; кислую сыворотку, являющуюся побочным продуктом производства кислотного казеина; нативную молочную сыворотку, полученную при микрофильтрации молока, или сычужную сыворотку, являющуюся побочным продуктом производства сычужного казеина. Сывороточный белок может быть получен из одного источника или смесей любых источников. Предпочтительно, чтобы сывороточный белок не подвергался стадии гидролиза перед мицеллообразованием. Так, сывороточный белок не должен подвергаться ферментативной обработке до мицеллизации. В настоящем изобретении важно использовать в способе мицеллообразования белок молочной сыворотки, а не его гидролизаты.
Настоящее изобретение не ограничивается изолятами сывороточного белка только из коровьего молока, а включает также изоляты сывороточного белка из молока всех видов млекопитающих, например овечьего, козьего, кобыльего молока и молока верблюдиц. Способ по настоящему изобретению применим также к минерализованному, деминерализованному или слабо минерализованному сывороточному продукту. Под "слабо минерализованным" подразумевается сывороточный продукт, из которого удалены методом диализа или диафильтрации свободные минералы, но в котором остались минералы, связанные с ним природной минерализацией после производства, например, концентрата или изолята сывороточного белка. Эти "слабо минерализованные" сывороточные продукты не подразумевают предварительного обогащения специфическими минералами.
Сывороточные белки являются отличным источником незаменимых аминокислот (АА) (45%). По сравнению с казеином (содержащим 0,3 г цистеина/100 г белка) белки сладкой сыворотки содержат в 7 раз больше цистеина, а белки кислой сыворотки в 10 раз больше цистеина. Цистеин - это аминокислота, лимитирующая скорость синтеза глутатиона (GSH), т.е. трипептида, состоящего из глутамата, цистеина и глицина, который выполняет первостепенные важные функции в защите организма от стресса. Потребности в указанных аминокислотах могут возрасти в случае стресса и у пожилых людей. Так, была показана полезность дополнения перорально принимаемых препаратов глутатиона сывороточным белком с целью повышения уровней GSH у ВИЧ-инфицированных больных (Eur. J. Clin. Invest. 2001; 31,171-178).
Другие полезные для здоровья преимущества, обеспечиваемые сывороточными белками, включают ускорение роста и формирования мышечной ткани, а также поддержание мышечной массы у детей, взрослых и пожилых людей, усиление иммунной функции, улучшение когнитивной функции, регулирование уровня глюкозы крови, что делает их пригодными для диабетиков, регулирование массы тела и чувства сытости, противовоспалительные действия, заживление ран и регенерация кожи, снижение кровяного давления и др.
Сывороточные белки характеризуются улучшенным коэффициентом эффективности белка (PER=118) по сравнению, например, с казеином (PER=100). PER -это мера качества белка, которое оценивается путем определения того, в какой степени тот или иной белок содействует приросту массы тела. PER можно рассчитать по следующей формуле:
PER=прирост массы тела (г) / масса потребленного белка (г).
| Параметры: | PER | % от казеина |
| казеин | 3,2 | 100 |
| яичный белок | 3,8 | 118 |
| белок молочной сыворотки | 3,8 | 118 |
| соевый белок | ||
| (белок цельных бобов) | 2,5 | 78 |
| пшеничный глютен | 0,3 | 9 |
В способе по изобретению сывороточные белки могут присутствовать в водном растворе в количестве от 0,1 мас.% до 12 мас.%, предпочтительно - в количестве от 0,1 мас.% до 8 мас.%, более предпочтительно - в количестве от 0,2 мас.% до 7 мас.%, еще более предпочтительно - в количестве от 0,5 мас.% до 6 мас.%, наиболее предпочтительно - в количестве от 1 мас.% до 4 мас.%, в пересчете на общую массу раствора.
Водный раствор продукта сывороточного белка в том виде, в каком он присутствует до стадии мицеллизации, может содержать также дополнительные соединения, такие как побочные продукты соответствующих способов производства сыворотки, другие белки, камеди или углеводы. Раствор может содержать также другие пищевые ингредиенты (жир, углеводы, растительные экстракты и др.). Количество таких дополнительных соединений предпочтительно не превышает 50 мас.%, более предпочтительно - 20 мас.%, наиболее предпочтительно - 10 мас.%, от общей массы раствора.
Сывороточный белок может использоваться в очищенном виде или в виде продукта-сырца. Согласно предпочтительному варианту воплощения изобретения содержание двухвалентных катионов в сывороточном белке для получения концентрата мицелл сывороточного белка может составлять ниже 2,5%, более предпочтительно - ниже 2%, еще более предпочтительно - ниже 0,2%. Наиболее предпочтительно, чтобы сывороточные белки были полностью деминерализованы.
В соответствии с настоящим открытием рН и ионная сила являются важными факторами в способе по изобретению. Так, в случае образцов, подвергнутых интенсивному диализу, из которых удалены практически все или сведены к минимуму свободные катионы, такие как Са, K, Na, Mg, было установлено, что при проведении тепловой обработки в течение периода времени от 10 секунд до 2 часов при рН ниже 5,4 образуется сгусток, в то время как при рН выше 6,8 образуется растворимый сывороточный белок (см. фиг.1). Поэтому только в этом довольно узком диапазоне рН можно получить мицеллы сывороточного белка диаметром менее 1 мкм. Эти мицеллы будут иметь общий отрицательный заряд. Такую же форму мицелл можно получить также при рН ниже изоэлектрической точки, т.е. при рН от 3,5 до 5,0, более предпочтительно - при рН от 3,8 до 4,5, который обеспечивает образование положительно заряженных мицелл (см. фиг.6).
Таким образом, согласно одному из вариантов воплощения изобретения для получения положительно заряженных мицелл мицеллизацию сывороточных белков можно проводить в не содержащем солей растворе при значении рН, установленном на уровне от 3,8 до 4,5 в зависимости от содержания минералов в белковом источнике.
Образующиеся при этом мицеллы предпочтительно будут иметь общий отрицательный заряд. Так, в предпочтительном варианте рН устанавливается на уровне от 6,3 до 9,0, если содержание двухвалентных катионов в сухом порошкообразном сывороточном белке составляет от 0,2% до 2,5%.
Если говорить более конкретно, то для получения отрицательно заряженных мицелл рН устанавливается в диапазоне от 5,6 до 6,4, более предпочтительно - от 5,8 до 6,0 при низком содержании двухвалентных ионов (например, ниже 0,2% исходного сухого сывороточного белка). рН может повышаться до 8,4 в зависимости от содержания минералов в источнике сывороточного белка (концентрате или изоляте). В частности, рН может составлять от 7,5 до 8,4, предпочтительно - от 7,6 до 8,0, для получения отрицательно заряженных мицелл в присутствии больших количеств свободных минералов, и рН может составлять от 6,4 до 7,4, предпочтительно - от 6,6 до 7,2, для получения отрицательно заряженных мицелл в присутствии умеренных количеств свободных минералов. Основное правило гласит, что чем выше содержание кальция и/или магния в исходном сухом сывороточном белке, тем выше рН мицеллизации.
В целях стандартизации условий мицеллообразования сывороточного белка наиболее предпочтительной является деминерализация любым из известных методов деминерализации (диализом, ультрафильтрацией, методом обратного осмоса, ионным обменом, хроматографией и др.) любого источника жидких нативных сывороточных белков с концентрацией белка, варьирующей от концентрации белка в сладкой сыворотке, пермеате от микрофильтрации молока или в кислой сыворотке (содержание белка 0,9%) до концентрации белка в концентрате с содержанием белка 30%. Диализ может проводиться против воды (дистиллированной, деионизированной или умягченной), но поскольку такой метод диализа позволяет удалять только ионы, слабо связанные с сывороточными белками, то более предпочтительным является метод диализа против кислоты при рН ниже 4,0 (органической или неорганической), позволяющий лучше контролировать ионный состав сывороточных белков. При проведении такого диализа рН мицеллообразования сывороточного белка будет ниже 7,0, более предпочтительно - от 5,8 до 6,6.
Перед тепловой обработкой водного раствора сывороточного белка его рН в большинстве случаев регулируется путем добавления кислоты, предпочтительно пищевого качества, такой как, например, соляная кислота, фосфорная кислота, уксусная кислота, лимонная кислота, глюконовая кислота или молочная кислота. Если содержание минералов высокое, то рН в большинстве случаев регулируется путем добавления раствора щелочи, предпочтительно пищевого качества, такой как гидроксид натрия, гидроксид калия или гидроксид аммония.
Альтернативно, если стадия регулирования рН не требуется, можно регулировать ионную силу сывороточно-белкового продукта при одновременном поддержании рН постоянным. В этом случае ионную силу можно регулировать с помощью органических или неорганических ионов таким путем, который позволяет проводить мицеллизацию при постоянном значении рН, равном 7. На фиг.4 показан вариант воплощения настоящего изобретения, в котором мицеллообразование может происходить при постоянном значении рН, равном 7,0, в то время как ионная сила будет варьироваться за счет добавления от 70 до 80 мМ комплекса аргинин НСl.
Буфер можно также добавлять к водному раствору сывороточного белка во избежание значительного изменения значения рН в ходе тепловой обработки сывороточного белка. В принципе буфер может выбираться из любой буферной системы пищевого качества, например уксусной кислоты и ее солей, таких как, например, ацетат натрия или ацетат калия; фосфорной кислоты и ее солей, таких как, например, NaH2PO4, Na2HPO4, KН2РО4, K2НРО4, или лимонной кислоты и ее солей и др.
Регулирование рН и/или ионной силы водного раствора обеспечивает, согласно настоящему изобретению, контролируемый способ получения мицелл размером от 100 до 900 нм, предпочтительно - от 100 до 700 нм, наиболее предпочтительно - от 200 до 400 нм. Предпочтительно относительное количество мицелл среднего размера от 100 до 700 нм составляет более 80% при осуществлении способа по изобретению (см. фиг.14).
Для получения мицелл правильной формы важно также, чтобы сывороточный белок не подвергался стадии гидролиза перед мицеллообразованием.
На второй стадии способа исходный водный раствор сывороточного белка подвергается тепловой обработке. В рамках этого было установлено, что для получения мицелл сывороточного белка важно, чтобы температура составляла от примерно 70°C до ниже 95°C, предпочтительно - от 80°C до примерно 90°С, более предпочтительно - примерно от 82°C до 89°C, еще более предпочтительно - примерно от 84°C до 87°C, наиболее предпочтительно - около 85°C. Установлено также, что в промышленном масштабе важно, чтобы температура была предпочтительно ниже 95°C, более предпочтительно - от 80°С до 90°C, наиболее предпочтительно - около 85°С.
По достижении требуемой температуры водный раствор сывороточного белка выдерживается при этой температуре в течение минимум 10 секунд и максимум 2 часов. Предпочтительно период времени, в течение которого водный раствор сывороточного белка выдерживается при требуемой температуре, колеблется от 12 до 25 минут, более предпочтительно - от 12 до 20 минут, наиболее предпочтительно - составляет около 15 минут.
Тепловая обработка может достигаться также в микроволновой печи или в аналогичном оборудовании, обеспечивающем микроволновой нагрев с соотношением время/количество, равным 10 с/10 мл, для 4 мас.% белкового раствора, нагреваемого в аппарате мощностью 1500 Вт до температуры кипения (98°С при высоте 833 м). Может применяться также и непрерывный способ при установке дополнительных 8 или более магнетронов вокруг стеклянной трубки, потенциально удлиненной трубчатым выдерживателем для увеличения времени инкубации.
Как показано на фиг.2, наличие помутнения служит показателем мицеллообразования. В настоящем изобретении мутность, измеряемая спектральной поглощательной способностью (СПС) при 500 нм, составляет по меньшей мере 3 единицы СПС для 1% белкового раствора, но может достигать и 16 единиц СПС в том случае, когда выход при мицеллизации превышает 80% (см. фиг.2).
С целью дополнительной иллюстрации эффекта мицеллообразования с физико-химической точки зрения 1 мас.% дисперсия белка Bipro® подвергали тепловой обработке при 85°С, 15 мин, при рН 6,0 и рН 6,8 в MilliQ-воде. Гидродинамический диаметр образовавшихся после тепловой обработки агрегатов измеряли методом динамического светорассеяния. Истинную молекулярную массу агрегатов определяли методом статического светорассеяния с использованием так называемой диаграммы Дебая. Поверхностную гидрофобность исследовали с помощью гидрофобного ANS (1-анилино-8-нафталенсульфоновая кислота) зонда, а свободные доступные SH-группы - методом с DTNB (дитиобис(нитробензол)) с использованием цистеина в качестве стандартной аминокислоты. В заключение изучали морфологию агрегатов с применением ТЕМ с негативным фоновым окрашиванием. Результаты представлены в табл.1.
| Таблица 1. | ||||||
| Физико-химические свойства агрегатов растворимого сывороточного белка, образовавшихся при тепловой обработке (85°C, 15 мин) 1 мас.% белковой дисперсии вприсутствии или в отсутствие NaCl | ||||||
| рН | Гидродинамический диаметр (нм) | Молекулярная масса Mw (×106 г·моль-1) | Морфология | ζ-потенциал (мВ) | Гидрофобность поверхности белка (мкг·ммоль-1 ANS) | Доступные SH-группы (нмолей SH·мг-1 белка) |
| 6,0 | 120,3±9,1 | 27,02±8,09 | Сферические мицеллы Линейные агрегаты | -31,8±0,8 | 105,4 | 3,5±0,4 |
| 6,8 | 56,2±4,6 | 0,64±0,01 | -27,9±1,2 | 200,8 | 6,8±0,5 |
Из табл.1 видно, что мицеллы сывороточного белка, образовавшиеся при рН 6,0, обусловливают снижение удельной ANS поверхностной гидрофобности белка на множитель 2 по сравнению с не подвергавшимся мицеллизации сывороточным белком, тепловая обработка которого проводилась при тех же режимах, но при рН 6,8. О мицеллообразовании можно судить также по очень высокой молекулярной массе (27×106 г·моль-1) белковых мицелл по сравнению с молекулярной массой белка, не подвергавшегося мицеллизации (0,64×106 г·моль-1), что указывает на очень конденсированное состояние вещества внутри мицеллы (низкое количество воды). Заслуживает интереса и тот факт, что ζ-потенциал мицелл еще более отрицателен, чем потенциал не подвергавшихся мицеллизации белков, даже если образование последних происходило при более щелочном рН, чем мицелл. Это является результатом более гидрофильной поверхности мицелл, подвергающейся действию растворителя. И, наконец, необходимо отметить, что реактивность SH-групп мицелл намного ниже, чем реактивность этих групп в белке, не подвергавшемся мицеллизации, что объясняется различным рН тепловой обработки.
Установлено, что выход мицелл в ходе конверсии нативного сывороточного белка в мицеллы снижается при увеличении начальной концентрации белка перед регулированием рН и тепловой обработкой. Например, при использовании в качестве исходного белка сывороточно-белкового изолята Prolacta 90 (партия 673 от Lactalis) выход мицелл сывороточного белка в процессе мицеллизации снижается с 85% (когда начальная концентрация белка составляла 4%) до 50% (когда начальная концентрация белка составляла 12%). Для максимизации выхода мицелл сывороточного белка (>85% начального содержания белка) лучше начинать с водного раствора сывороточного белка с концентрацией белка ниже 12%, предпочтительно - ниже 4%. В зависимости от предполагаемого конечного применения мицелл концентрация белка регулируется перед тепловой обработкой для достижения оптимального выхода мицелл сывороточного белка.
Мицеллы сывороточного белка, полученные способом по изобретению, имеют средний размер менее 1 мкм, предпочтительно - от 100 до 900 нм, более предпочтительно - от 100 до 700 нм, наиболее предпочтительно - от 200 до 400 нм.
В зависимости от требуемого применения мицелл их выход до концентрирования составляет по меньшей мере 35%, предпочтительно - по меньшей мере 50%, более предпочтительно - по меньшей мере 80%, а остаточное содержание растворимых агрегатов или растворимого белка - предпочтительно ниже 20%. Средний размер мицелл характеризуется индексом полидисперсности ниже 0,200. Наблюдения показали, что мицеллы сывороточного белка способны к образованию агрегатов при рН около 4,5, однако без признаков макроскопического разделения на фазы спустя по меньшей мере 12 часов при 4°C.
Чистоту мицелл сывороточного белка, полученных способом по настоящему изобретению, можно определить по количеству остаточных растворимых белков. Для этого мицеллы отделяют центрифугированием при 20°C и 26900g в течение 15 мин. Супернатант используют для определения количества белка в кварцевых кюветах при 280 нм (длина пути прохождения света 1 см). Полученные значения выражаются в % от начального значения перед тепловой обработкой.
Относительное количество мицелл=(количество исходных белков - количество растворимых белков) / (количество исходных белков).
Преимущество способа изобретения состоит в том, что полученные этим способом мицеллы сывороточного белка не подвергались воздействию какого-либо механического усилия, приводящего к уменьшению размера частиц в ходе их образования, в отличие от традиционных способов. Указанный способ индуцирует спонтанную мицеллизацию сывороточных белков в процессе тепловой обработки в отсутствие усилия сдвига.
Мицеллы сывороточного белка можно использовать в их нативном виде в любой композиции, например в питательных композициях, косметических композициях, фармацевтических композициях и др. Согласно настоящему изобретению мицеллы сывороточного белка используются в пригодных для употребления продуктах.
Кроме того, мицеллы сывороточного белка могут служить носителем для активного компонента. Указанный компонент может выбираться из кофе, кофеина, экстрактов зеленого чая, растительных экстрактов, витаминов, минералов, биоактивных агентов, соли, сахара, подсластителей, ароматических веществ, жирных кислот, масел, белковых гидролизатов, пептидов и др. и смесей перечисленного.
Помимо этого мицеллы сывороточного белка (чистые или смешанные с активным компонентом), использующиеся в настоящем изобретении, могут иметь покрытие из эмульгатора, такого как, например, фосфолипиды, или из других агентов, таких как белок, пептид, белковый гидролизат или камедь, такая как камедь акации, с целью модулирования функциональности и вкуса мицелл сывороточного белка. Если в качестве покрытия используется белок, то он может выбираться из любых белков, изоэлектрическая точка которых значительно выше или ниже изоэлектрической точки белков молочной сыворотки. Такими белками являются, например, протамин, лактоферрин и некоторые белки риса. Если в качестве покрытия используется белковый гидролизат, то он предпочтительно является гидролизатом таких белков, как протамин, лактоферрин, белки риса, казеин, белок молочной сыворотки, пшеничный, соевый белки или смеси перечисленного. Предпочтительно покрытием служит эмульгатор, выбираемый из сульфатированного бутил-олеата, сложных эфиров моно- и диглицеридов диацетилвинной кислоты, лимоннокислых эфиров моноглицеридов, стеароил-лактилатов и смесей перечисленного. На фиг.17 схематически изображен процесс образования покрытия из сульфатированного бутил-олеата. Покрытие может наноситься любым известным из уровня техники способом. Кроме того, совместная распылительная сушка, которая описывается ниже, может также приводить к образованию покрытия на мицеллах сывороточного белка.
Показано, что мицеллы сывороточного белка идеально подходят для применения в качестве эмульгатора, жирозаменителя, заменителя мицеллярного казеина или пенообразующего агента, поскольку они способны стабилизировать жир и/или воздух в водной системе в течение длительного периода времени.
Стабильность пены показана на фиг.5, которая сравнивает применение не подвергавшегося мицеллизации сывороточного белка с мицеллами сывороточного белка, использующимися в настоящем изобретении.
Так, мицеллы сывороточного белка могут применяться в качестве эмульгатора: для этой цели они идеально подходят, поскольку обладают нейтральным вкусом и при их использовании побочные привкусы и запахи не возникают.
В дополнение к этому, мицеллы сывороточного белка по настоящему изобретению могут служить также отбеливающим агентом, так что с помощью одного соединения можно решить несколько задач. Поскольку молочная сыворотка представляет собой сырье, всегда имеющееся в изобилии, ее использование снижает стоимость продукта за счет сокращения затрат на эмульгатор, наполнитель, отбеливатель или пенообразующий агент и в то же время повышает питательную ценность продукта.
Таким образом, мицеллы сывороточного белка, получаемые способом изобретения, могут использоваться для производства любого вида пригодного к употреблению продукта, требующего стабилизации эмульсии или пены, например, такой, ко