Производные дифенилазетидинона, содержащие эти соединения лекарственные средства и их применение
Иллюстрации
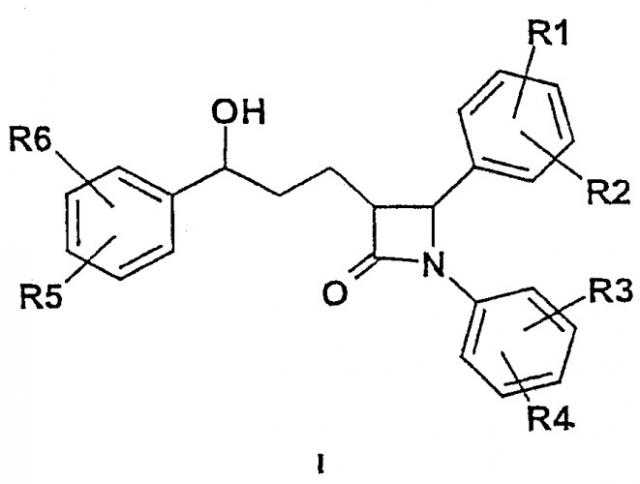
Показать всеНастоящее изобретение относится к производным дифенилазетидинона общей формулы I
в которой R1, R2, R3, R4 независимо друг от друга (С0-С30)-алкилен-L, причем один или несколько С-атомов алкиленового остатка могут быть замещены -О-, -(С=O)- или -NH-, кроме того, R1-R6 могут представлять собой Н, F;
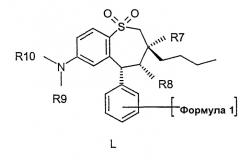
L представляет
а также их фармацевтически переносимые соли. Соединения формулы I проявляют гиполипидемическое действие и могут быть использованы в терапевтических целях. Описаны также лекарственное средство и его применение. 4 н. и 3 з.п. ф-лы.
Реферат
Изобретение относится к замещенным дифенилазетидинонам, их физиологически переносимым солям, а также к физиологически функциональным производным.
Дифенилазетидиноны (как, например, эзитимиб), а также их применение для лечения гиперлипидемии, артериосклероза и гиперхолестеринемии уже были описаны [ср. Drugs of the Future, 2000, 25(7): 679-685].
Задачей данного изобретения является получение новых соединений, проявляющих гиполипидемическое действие, пригодное для использования в терапевтических целях.
В первую очередь задача состояла в поиске новых соединений, которые по сравнению с соединениями, описанными в уровне техники, всасывались бы очень незначительно. Под очень незначительной всасываемостью понимается интестинальная всасываемость менее 10%, предпочтительно меньше или равная 5%.
Новые соединения должны в первую очередь иметь более незначительную всасываемость, чем эзитимиб.
При уменьшенной всасываемости фармацевтические активные вещества, как правило, проявляют заметно меньшие побочные действия.
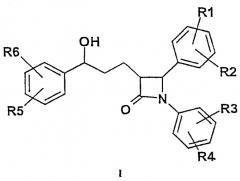
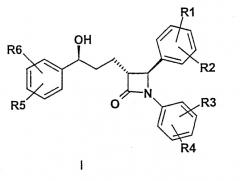
Изобретение относится к соединениям формулы I,
где означает
R1, R2, R3, R4, R5, R6 независимо друг от друга (C0-C30)-алкилен-L, причем один или несколько атомов C алкильного остатка могут быть замещены -О-, -(C=O)-, -CH=CH, С≡С, -N((C1-C6)алкил)- или -NH-;
H, F, Cl, Br, I, CF3, NO2, CN, COOH, COO(C1-C6)алкил, CONH2, CONH(C1-C6)алкил, CON[(C1-C6)алкил]2, (C1-C6)-алкил, (C2-C6)-алкенил, (C2-C6)-алкинил, O-(C1-C6)-алкил, причем в алкильных остатках один, несколько или все водороды могут быть замещены фтором; SO2-NH2, SO2NH(C1-C6)-алкил, SO2N[(C1-C6)-алкил]2, S-(C1-C6)-алкил, S-(CH2)n-фенил, SO-(C1-C6)-алкил, SO-(CH2)n-фенил, SO2-(C1-C6)-алкил, SO2-(CH2)n-фенил, причем n может быть n=0-6, а фенильный остаток может быть до двух раз замещен F, Cl, Br, OH, CF3, NO2, CN, OCF3, O-(C1-C6)-алкилом, (C1-C6)-алкилом, NH2;
NH2, NH-(C1-C6)-алкил, N((C1-C6)-алкил)2, NH(C1-C7)-ацил, фенил, O-(CH2)n-фенил, причем n может быть n=0-6, причем фенильное кольцо может быть от одного до трех раз замещено F, Cl, Br, I, OH, CF3, NO2, CN, OCF3, О-(C1-C6)-алкилом, (C1-C6)-алкилом, NH2, NH(C1-C6)-алкилом, N((C1-C6)-алкил)2, SO2-CH3, COOH, COO-(C1-C6)-алкилом, CONH2;
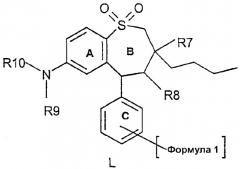
L представляет собой
R7 - метил, этил, пропил, бутил;
R8 - H, OH, NH2, NH-(C1-C6)-алкил;
R9 - метил, этил, пропил, бутил;
R10 - метил, этил, пропил, бутил;
причем всегда по крайней мере один из остатков R1-R6 должен иметь значение (C0-C30)-алкилен-L, причем один или несколько атомов C алкильного остатка может быть замещен -О-, -(C=O)-, -CH=CH-, -C≡C-, -N((C1-C6)-алкил)- или -NH-,
а также их фармацевтически переносимые соли.
Предпочтительны соединения формулы I, где по крайней мере один из остаток R1-R6 имеет значение (C0-C30)-алкилен-L, причем один или несколько атомов C алкильного остатка может быть замещен -О-, -(C=O)- или -NH-.
Особенно предпочтительны соединения формулы I, в которых один из остатков R1 или R3 имеет значение (C0-C30)-алкилен-L, причем один или несколько атомов C алкильного остатка могут быть замещены -O-, -(C=О)- или -NH-. Исключительно предпочтительны соединения формулы I, в которых один из остатков R1 или R3 имеет значение -(CH2)0-1-NH-(C=O)0-1-(C3-C25)-алкилен-(C=O)0-1-NH-L, причем один или несколько атомов C алкильного остатка могут быть замещены атомом О.
Связывание одного из остатков R1-R6 с остатком L происходит предпочтительно в мета-положении кольца C группы L.
Фармацевтически переносимые соли благодаря своей высокой растворимости в воде по сравнению с исходными или основными соединениями особенно подходят для медицинских применений. Эти соли должны иметь фармацевтически переносимый анион или катион. Подходящими фармацевтически переносимыми, кислотно-аддитивными солями соединений согласно изобретению являются соли неорганических кислот, как соляная кислота, бромоводородная, фосфорная, метафосфорная, азотная, сульфо- и серная кислоты, а также органические кислоты, как, например, уксусная кислота, бензосульфо-, бензойная, лимонная, этансульфо-, фумаровая, глюконовая, гликолевая, изотионовая, молочная, лактобионовая, малеиновая, яблочная, метансульфо-, янтарная кислоты, п-толуолсульфокислота, винная и трифторуксусная кислоты. Для медицинских целей особенно предпочтительно применяется хлорид. Подходящими фармацевтически переносимыми основными солями являются соли аммиака, соли щелочных металлов (как соли натрия и калия) и соли щелочно-земельных металлов (как соли магния и кальция).
Соли с фармацевтически непереносимым анионом в рамках настоящего изобретения также рассматриваются как полезные промежуточные продукты для получения или очистки фармацевтически переносимых солей и/или для применения в нетерапевтических целях, например для применения in vitro.
Используемое здесь понятие "физиологически функциональное производное" означает любое физиологически переносимое производное соединения согласно изобретению, например сложный эфир, который при употреблении млекопитающим, как, например, человеком, является способным (прямо или косвенно) образовывать такое соединение или его активный метаболит.
Другим аспектом настоящего изобретения являются пролекарства соединений согласно изобретению. Такие пролекарства могут быть метаболизированы in vivo до соединения согласно изобретению. Сами эти пролекарства могут быть как активными, так и неактивными.
Соединения согласно изобретению могут также находиться в различных полиморфных формах, например, как аморфные и кристаллические полиморфные формы. Все полиморфные формы соединений согласно изобретению включены в объем изобретения и представляют собой объект изобретения.
В дальнейшем все ссылки на "соединение(я) по формуле (I)" означают соединение(я) формулы (I), как описано выше, а также их соли, сольваты и физиологически функциональные производные.
Соединения формулы I и их фармацевтически переносимые соли и физиологически функциональные производные представляют идеальное лекарственное средство для лечения нарушений липидного обмена, в частности гиперлипидемии. Соединения формулы I пригодны также для воздействия на уровень сывороточного холестерина, а также для профилактики и лечения артериосклеротических проявлений.
Соединение(я) могут применяться также в комбинации с другими активно действующими веществами.
Количество соединения по формуле (I), которое необходимо для достижения желаемого биологического эффекта, зависит от ряда факторов, например выбранного конкретного соединения, способа введения, вида применения и клинического состояния пациента. В целом, дневная доза находится в интервале 0,1-100 мг (в основном от 0,1 мг до 50 мг) в день на килограмм веса тела, например 0,1-10 мг/кг/день. Таблетки или капсулы могут, например, содержать от 0,01 до 100 мг, обычно от 0,02 до 50 мг. В случае фармацевтически переносимых солей указанные количественные данные относятся к весу ионов дифенилазетидинона, содержащихся в соли. Для профилактики или терапии вышеназванных состояний соединения по формуле (I) могут применяться самостоятельно, однако предпочтительно они применяются с переносимыми носителями в форме фармацевтических композиций. Носитель должен быть, естественно, переносимым, в том смысле, что он совместим с другими составными частями композиции и не наносит вред здоровью пациента. Носителем может быть твердое вещество или жидкость, или то и другое, и предпочтительно вместе с соединением готовиться в виде отдельной единичной дозы, например в виде таблетки, которая может содержать от 0,05% до 95 вес.% активного вещества. Могут иметь место также другие фармацевтически активные вещества, включая другие соединения по формуле (I). Фармацевтические композиции согласно изобретению могут быть получены по одному из известных фармацевтических методов, которые в основном состоят в том, что составные части смешиваются с фармакологически переносимыми носителями и/или вспомогательными веществами.
Фармацевтическими композициями, относящимися к изобретению, являются такие, которые годятся для орального и перорального (например, сублингвального) применения, хотя самые подходящие способы введения в каждом отдельном случае зависят от вида и тяжести состояния и от вида каждого применяемого соединения формулы (I). К области изобретения относятся также дражированные лекарственные формы и дражированные лекарственные формы пролонгированного действия. Предпочтительны лекарственные формы, устойчивые к кислоте и желудочному соку. Подходящие устойчивые к желудочному соку покрытия охватывают ацетатфталат целлюлозы, фталат поливинилацетата, фталат гидроксипропилметилцеллюлозы и анионные полимеры метакриловой кислоты и метилметакрилата.
Подходящие для орального применения фармацевтические соединения могут предлагаться как, отдельные единицы, как, например, капсулы, облатки, сосательные таблетки или таблетки, которые в каждом случае содержат определенное количество соединения по формуле (I); как порошок или гранулят; как раствор или суспензия в водной или неводной жидкости; или как эмульсия "масло в воде" или "вода в масле". Эти композиции могут, как уже указывалось, готовиться по любому подходящему фармацевтическому методу, который включает стадию, на которой активное вещество и носитель (который может состоять из одной или нескольких составных частей) приводятся в контакт. Обычно композиции получают равномерным и гомогенным смешением активного вещества с жидким и/или измельченным твердым носителем, после чего продукт, если необходимо, формуется. Например, таблетку можно получить тем, что порошок или гранулят соединения прессуют или формуют, при необходимости с одним или несколькими дополнительными компонентами. Прессованные таблетки могут получаться путем таблетирования соединения в свободно-текучей форме, как, например, порошок или гранулят, при необходимости смешанного со связующим, мягчителем, инертным разбавителем и/или одним (несколькими) поверхностно-активным/диспергирующим средством в подходящем устройстве. Формованные таблетки могут получаться формованием порошкообразного соединения, увлажненного инертным жидким разбавителем в подходящем устройстве.
Фармацевтические композиции, подходящие для перорального (сублингвального) введения, включают сосательные таблетки, которые содержат соединение по формуле (I) с вкусовой добавкой, обычно сахарозой и гуммиарабиком или трагантом, и пастилки, которые содержат соединение в инертной основе, как желатин и глицерин или сахароза и гуммиарабик.
Другими подходящими активными веществами для комбинированных препаратов являются все антидиабетические средства, которые названы в Красном списке 2001, глава 12. Они могут комбинироваться с относящимися к изобретению соединениями формулы I, в первую очередь, для синергетического улучшения действия. Применение комбинации действующих веществ может происходить либо раздельным введением активно действующего вещества пациенту или в форме комбинированного препарата, в котором присутствуют несколько активных веществ в одной фармацевтической готовой форме.
Антидиабетические средства включают инсулин и производные инсулина, как, например, Lantus® или HMR 1964, производные GLP-1, как, например, те, которые опубликованы в заявке WO 98/08871, поданной Novo Nordisk A/S, а также орально действующие гипогликемические действующие вещества.
Гипогликемические действующие вещества для орального применения включают преимущественно сульфонилмочевину, бигуадин, меглитиниды, оксадиазолидиндионы, тиазолидиндионы, ингибиторы глюкозидазы, антагонисты глюкагона, агонисты GLP-1, активаторы калиевого канала, как, например, те, что опубликованы в заявках WO 97/26265 и WO 99/03861 фирмы Novo Nordisk A/S, инсулинсенсибилизирующие вещества, ингибиторы энзимов печени, которые принимают участие в стимуляция глюконеогенеза и/или гликогенолиза, модуляторы поглощения глюкозы, соединения, изменяющие жировой обмен, как антигиперлипидемически действующие вещества и антилипидемически действующие вещества, соединения, которые уменьшают прием пищевых продуктов, агонисты PPAR и PXR и вещества, воздействующие на АТФ-зависимый калиевый канал бета-клеток.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором ГМГ-КоА-редуктазы, как симвастатин, флювастатин, правастатин, ловастатин, аторвастатин, церивастатин, розувастатин.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором всасываемости холестерина, как, например, эзитимиб, тиквезид, памаквезид. В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с агонистом PPAR-гамма, как, например, розиглитазоном, пиоглитазонон, JTT-501, GI 262570.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с агонистом PPAR-альфа, как, например, GW 9578, GW 7647.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации со смесью агонистов PPAR альфа/гамма, как, например, GW 1536, AVE 8042, AVE 8134, AVE 0847.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с фибратом, как, например, фенофибрат, клофибрат, безафибрат.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором MTP, как, например, Bay 13-9952, BMS-201038, R-103757.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором всасываемости желчной кислоты, как, например, HMR 1453.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором CETP, как, например, Bay 194789.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с полимерным адсорбером желчной кислоты, как, например, холестирамин, колесолвам.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с индуктором LDL-рецептора, как, например, HMR1171, HMR1586.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором ACAT, как, например, авасимиб.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с антиоксидантом, как, например, OPC-14117.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором липопротеин-липазы, как, например, NO-1886.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором АТФ-цитрат-лиазы, как, например, SB-204990.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором сквален-синтетазы, как, например, BMS-188494.
В одной из форм выполнения изобретения соединения формулы I применяется в комбинации с антагонистом липопротеинов, как, например, CI-1027 или никотиновая кислота.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с ингибитором липазы, как, например, орлистат.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с инсулином.
В одной из форм выполнения изобретения соединения формулы I применяются в комбинации с сульфонилмочевиной, как, например, толбутамид, глибенкламид, глипицид или гликлацид.
В одной форме выполнения изобретения соединения формулы I применяются в комбинации с бигуанидом, как, например, метформин.
Еще в одной форме выполнения изобретения соединения формулы I применяются в комбинации с меглитинидом, как, например, репаглинид.
В одной форме выполнения изобретения соединения формулы I применяются в комбинации с тиазолидиндионом, как, например, троглитазон, циглитазон, пиоглитазон, розиглитазон или соединениями, опубликованными в заявке WO 97/41097, поданной Dr. Reddy's Research Foundation, в частности 5-[[4-[(3,4-дигидро-3-метил-4-оксо-2-хиназолинилметокси]фенил]метил]-2,4-тиазолидиндион.
В одной форме выполнения изобретения соединения формулы I применяются в комбинации с ингибитором α-глюкозидазы, как, например, миглитол или акарбоза.
В одной форме выполнения изобретения соединения формулы I применяются в комбинации с активным веществом, действующим на АТФ-зависимый калиевый канал бета-клеток, как, например, толбутамид, глибенкламид, глипицид, глиацид или репаглинид.
В одной форме выполнения изобретения соединения формулы I применяются в комбинации с более чем одним из ранее названных соединений, например, в комбинации с сульфонилмочевиной и метформином, сульфонилмочевиной и акарбозой, репаглинидом и метформином, инсулином и сульфонилмочевиной, инсулином и метформином, инсулином и троглитазоном, инсулином и ловастатином, и т.д.
В другой форме выполнения изобретения соединения формулы I применяются в комбинации с агонистами CART, агонистами NPY, агонистами MC4, агонистами орексина, агонистами H3, агонистами TNF, агонистами CRF, антагонистами CRF BP, агонистами урокортина, агонистами β3, агонистами MSH (меланоцит-стимулирующий гормон), агонистами CCK, ингибиторами повторного поглощения серотонина, смешанными серотонин- и норадренергическими соединениями, агонистами 5HT, агонистами бомбезина, антагонистами галанина, гормонами роста, соединениями, выделяющим гормон роста, агонистами TRH, разъединяющими протеин модуляторами 2 или 3, агонистами лептина, агонистами DA (бромокриптин, допрексин), ингибиторами липазы/амилазы, модуляторами PPAR, модуляторами RXR или агонистами TR-β.
В одной форме выполнения изобретения другим действующим веществом является лептин.
В одной форме выполнения изобретения другим действующим веществом является дексамфетамин или амфетамин.
В одной форме выполнения изобретения другим действующим веществом является фенфлюрамин или дексфенфлюрамин.
Еще в одной форме выполнения изобретения другим действующим веществом является субитрамин.
В одной форме выполнения изобретения другим действующим веществом является орлистат.
В одной форме выполнения изобретения другим действующим веществом является мациндол или фентермин.
В одной форме выполнения изобретения соединения формулы I применяются в комбинации с балластными веществами, преимущественно нерастворимыми балластными веществами, как, например, Caromax®. Комбинация с Caromax® может происходить в одном готовом препарате или при раздельном введении соединения формулы I и Caromax®. Caromax® может при этом подаваться также с пищевыми продуктами, как, например, в хлебобулочных изделиях или хлопьях мюсли. Комбинация соединения формулы I с Caromax® проявляется, наряду с улучшением действия, в частности, снижением LDL-холестерина (липопротеины низкой плотности), по сравнению с отдельными активно действующими веществами, а также улучшенной переносимостью.
Подразумевается, что каждая подходящая комбинация соединения согласно изобретению с одним или несколькими вышеназванными соединениями и, при желании, одним или несколькими другими фармакологически действующими веществами подпадает под защиту настоящего изобретения.
Далее, предметом изобретения являются как стереоизомерные смеси формулы I, так и чистые стереоизомеры формулы I, а также как диастереомерные смеси формулы I, так и чистые диастереомеры. Разделение смеси осуществляется хроматографическим способом.
Предпочтительными являются рацемические, а также чисто энантиомерные соединения формулы I со следующей структурой:
Далее, предпочтительны соединения формулы I, где остаток L имеет следующее значение:
Предметом изобретения является, далее, способ получения соединения общей формулы I, отличающийся тем, что получение соединения формулы I проходит аналогично следующей реакционной схеме.
R4" означает (C0-C30)-алкилен, причем один или несколько атомов C алкильного остатка может быть замещен -O-, -(C=O)-, -CH=CH-, -C≡C-, ((C1-C6)-алкил)- или -NH-.
Альтернативно происходит связывание с L-группой через кольцо A или кольцо C.
Следующие примеры служат более детальному разъяснению изобретения, не ограничиваясь продуктами, описанными в примерах, и формами исполнения.
Пример I
5-{4-[3-(3-гидрокси-3-фенилпропил)-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензиламино}пентановая кислота-[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амид (1)
100 мг 5-бромпентановая кислота-[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амида и 70 мг 1-(4-аминометилфенил)-3-(3-гидрокси-3-фенилпропил)-4-(4-метоксифенил)азетидин-2-она растворяют в 5 мл диметилформамида и нагревают от 2 до 3 ч при перемешивании до 80°C. После окончания реакции (контроль по тонкослойной хроматографии (ТСХ) или ВЭЖХ-MS) растворитель удаляют в вакууме и остаток чистят с помощью хроматографии. Так получают продукт 1 с молекулярным весом 929,24 (C55H68N4O7S); MS(FAB): 929 (M+H+).
Пример II
[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амид и 4-[1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)-4-оксоазетидин-2-ил]бензиламид гександикарбоновой кислоты (8)
a) 1-(2-оксо-4-фенилоксазолидин-3-ил)-5-фенилпентан-1,5-дион (2)
10 г бензоилмасляной кислоты и 12,5 мл триэтиламина растворяют в 55 мл дихлорметана. Через 5 мин при комнатной температуре в течение 30 мин добавляют 6,2 мл пивалоилхлорида и перемешивают 2 ч. Затем добавляют 5,9 г 4-фенил-оксазолидин-2-она в 6 мл диметилформамида и 0,9 г 4-(диметиламино)пиридина. Нагревают около 7 ч с обратным холодильником (ТСХ-контроль). После окончания реакции прибавляют 15 мл 2-н серной кислоты, перемешивают в течение короткого времени и затем фазы разделяют. Органическую фазу промывают 5-процентным раствором гидрокарбоната, после сушки, концентрирования и перекристаллизации из смеси этилацетат/н-гептан получают продукт с молекулярным весом 337,4 (C20H19NO4); MS (DCI+): 338 (M+H+). При применении оптически активного/обогащенного энантиомерными формами 4-фенил-оксазолидин-2-она получают тем же способом оптически активный/обогащенный энантиомерными формами продукт 2.
b) 3-(5-гидрокси-5-фенилпентаноил)-4-фенил-оксазолидин-2-он (3)
К раствору 1,5 мл комплекса бордиметилсульфида в 25 мл дихлорметана медленно прибавляют в течение примерно 3 ч в атмосфере аргона при температуре между 0° и -5°C 5 г 1-(2-оксо-4-фенил-оксазолидин-3-ил)-5-фенилпентан-1,5-диона в 20 мл дихлорметана. Перемешивают 2 ч при той же температуре и контролируют тонкослойной хроматографией. После окончания превращения добавляют при 0°C 2 мл метанола и 1,5 мл 35-процентного раствора перекиси водорода, а также 1,1 мл 3 н. серной кислоты и перемешивают 15 мин при комнатной температуре. После разделения фаз органические фазы моют последовательно: 2 н. серной кислотой, 5-процентным раствором бисульфита натрия, 10-процентным раствором поваренной соли и затем сушат и концентрируют. После хроматографии (SiO2, этилацетат/н-гептан=1:1) получают продукт с молекулярным весом 339,4 (C20H21NO4); MS (DCI+): 322 (M+H+-H2O); (ESI+): 403 (M+Na++CH3CN), 362 (M+Na+). Добавлением к реакционной смеси оптически активного 1-метил-3,3-дифенилтетрагидропирроло[1,2-c][1,3,2]оксазаборола (S или R, 0,75 мл) при температуре от 0°до -5°C перед введением 1-(2-оксо-4-фенилоксазолидин-3-ил)-5-фенилпентан-1,5-диона аналогичным способом получают продукт 3 в форме, обогащенной диастереомерами.
c) 4-[1-(4-фторфениламино)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)-5-фенил-5-триметилсиланилоксипентил]бензонитрил (4)
3,3 г 3-(5-гидрокси-5-фенилпентаноил)-4-фенилоксазолидин-2-она и 3,93 г 4-[(4-фторфенилимино)метил]бензонитрила растворяют в 55 мл дихлорметана, охлаждают до -10°C и медленно смешивают с 8,5 мл диизопропилэтиламина. В течение 30 мин прибавляют 5,3 мл хлортриметилсилана так, чтобы температура оставалась ниже 5°C. Через один час охлаждают до -30°C и добавляют 1,1 мл тетрахлорида титана при температуре ниже -25°C и перемешивают затем в течение ночи при этой температуре. После окончания превращения по каплям добавляют 4 мл ледяного уксуса при -25°C, затем перемешивают 15 мин, добавляют при 0°C 50 мл 7-процентной винной кислоты и перемешивают 1 ч, добавляют затем 25 мл 20-процентного раствора бисульфита натрия и перемешивают дальнейшие 45 мин. После разделения фаз органические фазы промывают приблизительно 40 мл воды, сушат и концентрируют примерно до 15 мл. Затем добавляют 2,7 мл бистриметилсилилацетамида и нагревают 30 мин с обратным холодильником. После охлаждения до комнатной температуры концентрируют и после кристаллизации остатка из смеси этилацетат/н-гептан получают продукт с молекулярным весом 635,8 (C37H38FN3О4Si); MS (ESI+): 636 (M+H+).
d) 4-[1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)-4-оксоазетидин-2-ил]бензонитрил (5)
2,7 г 4-[1-(4-фторфениламино)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)-5-фенил-5-триметилсиланилоксипентил]бензонитрила нагревают в 30 мл трет-бутилметилэфира с 1,6 мл бистриметилсилилацетамида и 0,2 г тригидрата тетрабутиламмонийфторида 3 ч с обратным холодильником. После выстаивания в течение ночи прибавляют 0,2 мл ледяного уксуса, перемешивают 15 мин и сильно концентрируют. Для это добавляют 15 мл смеси изопропанол/2 н. серная кислота = 10:1 и перемешивают 1 ч при комнатной температуре. После обрабатывают небольшим количеством твердого гидрокарбоната натрия, снова сильно концентрируют, собирают остаток в этилацетате и промывают водой. Остаток сухих органических фаз чистят с помощью фильтрации через колонки (SiO2, этилацетат/н-гептан=1:1). Получают продукт с молекулярным весом 400,5 (C25H21FN2О2); MS (DCI+): 401 (M+H+), 383 (M+H+-H2O).
e) 4-(4-аминометилфенил)-1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)азетидин-2-он (6)
930 мг 4-[1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)-4-оксоазетидин-2-ил]бензонитрила растворяют в 100 мл этанола, смешивают с 4 мл концентрированного аммиака и гидрируют 20 ч при комнатной температуре и 20 бар водорода с использованием никеля Рэнея. Отсасывают от катализатора, концентрируют в вакууме и получают после хроматографии (SiO2, дихлорметан/метанол=10:1) продукт с молекулярным весом 404,5 (C25H25FN2О2); MS (DCI+): 405 (M+H+), 387 (M+H+-H2O).
f) 5-[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]пентановая кислота (7)
2 г 5-(3-аминофенил)-3-бутил-7-диметиламино-3-этил-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-4-ола, 3,4 г гександикарбоновой кислоты, 1,04 г дициклогексилкарбодиимида и 640 мг бензотриазол-1-ола перемешивают в 80 мл тетрагидрофурана в течение ночи при комнатной температуре. Концентрируют, собирают остаток этилацетатом, отфильтровывают от избыточной мочевины и промывают водой. Остаток осушенных органических фаз чистят с помощью фильтрации на колонне (SiO2, дихлорметан/метанол=20:1). Получают продукт с молекулярным весом 558,7 (C30H42N2O6S); MS (ESI+): 559 (M+H+).
g) [3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амид и 4-[1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)-4-оксоазетидин-2-ил]бензиламид гександикарбоновой кислоты (8)
83 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)азетидин-2-она, 115 мг 5-[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]пентановой кислоты, 45 мг дициклогексилкарбодиимида и 35 мг бензотриазол-1-ола перемешивают в 5 мл тетрагидрофурана в течение ночи при комнатной температуре. Концентрируют в вакууме и после хроматографии (SiO2, дихлорметан/метанол=20:1) получают продукт с температурой плавления 150°C и молекулярным весом 945,2 (C55H65FN4O7S); MS (ESI+): 945 (M+H+).
Пример III
[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амид и 4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензиламид гександикарбоновой кислоты (12)
a) 4-[5-(4-фторфенил)-1-(4-фторфениламино)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)-5-триметилсиланилоксипентил]бензонитрил (9)
Получение аналогично примеру II с применением 3-[5-(4-фторфенил)-5-гидроксипентаноил]-4-фенилоксазолидин-2-она.
Продукт с молекулярным весом 653,8 (C37H37F2N3О4Si); MS (ESI+): 654 (M+H+).
b) 4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензонитрил (10)
Получение аналогично примеру II, с применением 4-[5-(4-фторфенил)-1-(4-фторфениламино)-2-(2-оксо-4-фенилоксазолидин-3-карбонил)-5-триметилсиланилоксипентил]бензонитрила; продукт с молекулярным весом 418,5 (C25H20F2N2O2); MS (ESI+):419(M+H+).
c) 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-он (11)
Получение аналогично примеру II; с применением 4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензонитрила.
Продукт с молекулярным весом 422,5 (C25H24F2N2O2); MS (ESI+): 423 (M+H+).
d) [3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амид и 4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензиламид гександикарбоновой кислоты (12)
Получение аналогично примеру II; продукт с молекулярным весом 963,2 (C55H64F2N4О7S); MS (ESI+): 963 (M+H+).
Пример V
[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенил]амид и 4-[3-(3-гидрокси-3-фенилпропил)-2-(4-метоксифенил)-4-оксоазетидин-1-ил]бензиламид гександикарбоновой кислоты (15)
Получение аналогично примеру III, исходя из 1-(4-аминометилфенил)-3-(3-гидрокси-3-фенилпропил)-4-(4-метоксифенил)азетидин-2-она.
Продукт с молекулярным весом 957,2 (C56H68N4О8S); MS(ESI+): 957 (M+H+).
Пример VI
[2-(2-{[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]метокси}этокси)этокси]-[N-{4-[1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)-4-оксоазетидин-2-ил]бензил}]-ацетамид (16)
Получение аналогично примеру II, исходя из 83 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-(3-гидрокси-3-фенилпропил)азетидин-2-она и 130 мг [2-(2-{[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]метокси}этокси)этокси] уксусной кислоты.
Хроматография: SiO2, дихлорметан/метанол=20:1; продукт с температурой плавления 120°C и молекулярным весом 1021,3 (C57H67FN4O10S); MS (ESI+): 1021 (M+H+).
Пример VII
(3-бутил-3-этил-5-[3-(2-{2-[(4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)метокси]этокси}ацетиламино)фенил]-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (18)
a) (2-{[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]метокси}этокси)уксусная кислота (17)
К 965 мг раствора 10 г диоксаоктандикарбоновой кислоты, 188 мг гидроксибензотриазола и 287 мг дициклогексилкарбодиимида в 10 мл тетрагидрофурана (ТГФ) добавляют по каплям в течение 2 ч 500 мг 5-(3-амино-фенил)-3-бутил-7-диметиламино-3-этил-1,1-диоксо-2,3,4,5-тетрагидро-1H-1-бензо[b]тиепин-4-ола в 8 мл ТГФ. Перемешивают при комнатной температуре в течение 12 ч. Реакционный раствор концентрируют, собирают 2 н. соляной кислотой и экстрагируют этилацетатом. Органические фазы сушат над сульфатом магния, концентрируют и чистят с помощью ВЭЖХ (Merk-Hibar-Lichrospher 100-RP-18, вода (0,1 % трифторуксусной кислоты)/ацетонитрил (0,1% трифторуксусной кислоты)=80/20->10/90). Получают продукт 17.
C30H41N2O8S1 (590,74); MS (ESI): 592 (M+H).
b) (3-бутил-3-этил-5-[3-(2-{2-[(4-{1-(4-фторфенил)-3-[3-(4-фторофенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)метокси]этокси}ацетиламино)фенил]-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)-диметиламмоний; трифторацетат (18)
Раствор 100 мг 4-(4-аминометилфенил)-1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]азетидин-2-она, 209 мг (2-{[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)-фенилкарбамоил]метокси}этокси)уксусной кислоты, 93 мкл диизопропилкарбодиимида, 65 мг гидроксибензотриазола в 2 мл метиленхлорида перемешивают 12 ч при комнатной температуре. Добавляют воду и экстрагируют метиленхлоридом. Органические фазы сушат над сульфатом магния, концентрируют и разделяют на ВЭЖХ (Knauer Eurospher-100-10-C18, вода (0,1 % трифторуксусной кислоты)/ацетонитрил (0,1% трифторуксусной кислоты)=80/20->10/90). Получают продукт 18.
C57H63F5N4O11S1 (1109,23); MS (ESI): 977 (M+H-H2O).
Аналогично примеру VII получают следующие примеры (VIII-XXIV):
Пример VIII
(3-бутил-3-этил-5-[3-(2-{2-[(3-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)метокси]этокси}ацетиламино)фенил]-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (19)
C57H65F5N4О11S1 (1109,23); MS (ESI): 977 (M+Н-H2O).
Пример IX
3-бутил-3-этил-5-{3-[2-(2-{2-[(4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил}бензилкарбамоил)метокси]этокси}этокси)ацетиламино]фенил}-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (21)
a) [2-(2-{[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]метокси}этокси)этокси]уксусная кислота (20)
C32H46N2O3S1 (634,3); MS (ESI): 635 (M+H).
b) (3-бутил-3-этил-5-{3-[2-(2-{2-[(4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)метокси]этокси}этокси)ацетиламино]фенил}-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)-диметиламмоний; трифторацетат (21)
C59H69F5N4O12S1 (1153,28); MS (ESI): 1039 (M+H).
Пример X
(3-бутил-3-этил-5-{3-[2-(2-{2-[(3-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)метокси]этокси}этокси)ацетиламино]фенил}-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (22)
C59H69F5N4O12S1 (1153,28); MS (ESI): 1040 (M + H).
Пример XI
(3-бутил-3-этил-5-{3-[11-(4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)ундеканоиламино]фенил}-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (24)
a) 11-[3-(3-бутил-7-диметиламино-3-этил-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-5-ил)фенилкарбамоил]ундекановая кислота (23)
C36H54N2O6S1 (642,91); MS (ESI): 643 (M + H).
b) (3-бутил-3-этил-5-{3-[11-(4-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)ундеканоиламино]фенил}-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (24)
C63H77F5N4O9S1 (1161,39); MS (ESI): 1047 (M+H).
Пример XII
(3-бутил-3-этил-5-{3-[11-(3-{1-(4-фторфенил)-3-[3-(4-фторфенил)-3-гидроксипропил]-4-оксоазетидин-2-ил)бензилкарбамоил)ундеканоиламино]фенил}-4-гидрокси-1,1-диоксо-2,3,4,5-тетрагидро-1H-бензо[b]тиепин-7-ил)диметиламмоний; трифторацетат (25)
C63H77F5N4O9S1